Prof. S. Winawer (président, USA)
Prof. M. Classen (co-président, Allemagne)
Prof. R. Lambert (co-président, France)
Prof. M. Fried (Suisse)
Prof. P. Dite (République Tchèque)
Prof. K.L. Goh (Malaisie)
Prof. F. Guarner (Espagne)
Prof. D. Lieberman (USA)
Prof. R. Eliakim (Israel)
Prof. B. Levin (USA)
Prof. R. Saenz (Chili)
Prof. A.G. Khan (Pakistan)
Prof. I. Khalif (Russie)
Prof. A. Lanas (Espagne)
Prof. G. Lindberg (Suède)
Prof. M.J. O’Brien (USA)
Prof. G. Young (Australie)
Dr. J. Krabshuis (France)
Prof. R. Smith (USA)
Prof. W. Schmiegel (Allemagne)
Prof. D. Rex (USA)
Prof. N. Amrani (Maroc)
Prof. A. Zauber (USA)
1. Introduction
Le Cancer colorectal (CCR) est un problème mondial avec une incidence annuelle d’environ 1 million de cas et une mortalité annuelle de plus de 500.000. Le nombre absolu de cas va augmenter pendant les décennies à venir du fait du vieillissement et de l’expansion des populations dans les pays développés ou en voie de développement.
Le Cancer colorectal est la seconde cause de mortalité par cancer chez les hommes et les femmes. La plupart des cancers colorectaux résultent d’adénomes sporadiques et de la transformation maligne d’un polype adénomateux bénin, mais quelques uns résultent d’adénomes familiaux ou de syndromes de l’intestin irritable. Le terme « polype » fait référence à une masse discrète qui fait saillie dans le lumen intestinal. La prévalence rapportée des polypes adénomateux sur la base des données de dépistage par colonoscopie varie de 18 à 36%.
Le risque de cancer colorectal varie selon les pays et même à l’intérieur d’un pays. Il diffère également entre les individus selon leur alimentation, leur mode de vie et des facteurs héréditaires.
Lors d’un dépistage d’un cancer colorectal, la tumeur que l’on rencontre le plus souvent est l’adénome. Après résection, les patients doivent suivre un programme de surveillance comme tous ceux qui ont un cancer identifié et traité. .
Ces recommandations pratiques veulent aider à dépister les hommes et femmes asymptomatiques susceptibles d’avoir des polypes adénomateux ou un cancer. Le dépistage doit être mené au sein d’un programme qui inclut la prévention primaire (alimentation, mode de vie), un diagnostic porté à temps par colonoscopie (partout où c’est possible et selon les diverses étapes de la cascade) là où le dépistage a révélé une pathologie et un traitement approprié (polypectomie, chirurgie).
Le dépistage du cancer colorectal pose un véritable défi à cause des taux particulièrement bas de dépistage dans les pays à risque élevé de cancer colorectal. Il est complexe à cause de ses options multiples. Il requiert du patient un effort considérable (analyse de sang occulte dans les selles, préparation à la colonoscopie); il demande aussi une sédation et des personnels de santé compétents (colonoscopie). Pour qu’un programme de dépistage soit couronné de succès, de nombreux facteurs doivent intervenir prises de conscience et recommandations par les médecins et les services de santé primaire, compliance du patient, couverture financière, stratification du risque, diagnostic et traitement portés à temps et suivi approprié. Si l’une de ces étapes manque ou se révèle de mauvaise qualité, c’est l’ensemble qui échoue.
2. Méthodologie et Revue de la Littérature
Les Recommandations pratiques de l’Organisation Mondiale de Gastroentérologie résument ce qui est reconnu et a été publié dans des articles systématiques, des recommandations basées sur l’évidence et des essais cliniques de haute qualité; cette information est ensuite configurée et regroupée afin de rendre les Recommandations aussi pertinentes et accessibles que possible globalement. D’ordinaire cela revient à construire et élaborer différentes approches pour arriver aux mêmes buts –chaque approche étant différente car prenant en compte les ressources locales, les préférences culturelles et les politiques spécifiques. Les Recommandations de l’Organisation Mondiale de Gastroentérologie ne sont pas des articles systématiques basés sur une étude systématique et exhaustive de tout ce qui est basé sur l’évidence et de toutes les recommandations disponibles. Un texte global essaie de faire la distinction entre les différentes régions et des épidémiologies diverses et il est ensuite traduit en différentes langues afin de faciliter son utilisation et sa compréhension. .
Cette Recommandation pratique a été élaborée par le Groupe de Travail après une recherche bibliographique visant à recenser les nouveautés et changements depuis la première publication de l’Organisation sur le sujet du dépistage du cancer colorectal en 2002. (http://omge.org/globalguidelines/statement03/statement3.htm).
L’évidence disponible a été recherchée à l’aide d’une syntaxe précise pour chaque plate-forme utilisée. Les Recommandations pertinentes ont été obtenues sur la plateforme de l’United States National Guideline Clearinghouse à l’adresse www.ngc.org et sur les sites Internet des principales sociétés de médecine intéressées par la gastroentérologie et le cancer. Des recherches complémentaires ont été conduites sur Medline et Embase sur Dialog DataStar depuis 2003. Une recherche faite sur la Cochrane Library a permis de recenser 18 articles systématiques pertinents et 12 protocoles. Les membres du groupe de travail ont eu à travailler dans les différentes sections selon leur degré d’expertise et leurs préférences. En fin de compte, des experts internationaux furent consultés et le document préliminaire entier fut édité par le président du groupe de travail et le responsable de la documentation.
3. Epidémiologie du cancer colorectal
3.1 L’importance du cancer colorectal
Dans la base Globocan 2002, base du Centre International de Recherche sur le Cancer (IARC CIRC), il est estimé que le cancer colorectal représente 550.000 nouveaux cas dont 278.000 décès chez l’homme et 473.000 nouveaux cas dont 255.000 chez la femme. En 2002, le cancer colorectal représentait 9,4 % de l’ensemble des cancers pour les deux sexes et il était plus fréquent en Amérique du Nord, Australie, Nouvelle-Zélande et certaines parties de l’Europe. Cela a conduit à penser que le cancer colorectal pouvait être considéré comme une pathologie liée au style de vie occidental. .
3.2 Evolutions temporelles de l’incidence et de la mortalité
Les taux de mortalité par âge pour le cancer colorectal chez l’homme et la femme dans les pays occidentaux sont restés stables au long du XX° siècle et pourraient maintenant commencer à diminuer. Mais à l’inverse des changements rapides sont en train de se produire dans des pays jusque là considérés comme étant à risque faible.
En Europe, les taux de mortalité par âge ont augmenté dans les régions du sud et de l’est de l’Europe, au contraire de celles au nord ou au centre du continent. Ces dernières années, les taux de mortalité tendent systématiquement à être plus favorables aux femmes qu’aux hommes. .
Aux Usa, selon les registres du Surveillance Epidemiology and End Results (SEER) entre 1973 et 1989 le taux d’incidence par âge du cancer du colon a augmenté de 11% chez les hommes blancs et de 39 % chez les noirs alors que l’incidence globale du cancer du rectum a baissé de 5 % chez les blancs mais augmenté de 27 % chez les noirs. Chez les femmes, le taux d’incidence du cancer du colon a baissé de 3 % chez les blanches et augmenté de 26 % chez les noires alors que le cancer du rectum avait baissé respectivement de 7 et 10 %. Depuis 1990, le taux par âge du cancer du colon a décliné. Il se peut que la pratique de prévention par polypectomie ait joué un rôle. .
Au Japon, les taux de mortalité par âge du cancer colorectal qui étaient bas au milieu du XX° siècle ont été multipliés par trois dans les deux sexes entre 1955-1974 et 1975-1984.
Avec le vieillissement de la population mondiale, on s’attend à une augmentation considérable du nombre de cas. .
3.3 Risques familiaux et génétiques du cancer colorectal
Fig. 1 Facteurs de risques familiaux et cancer colorectal
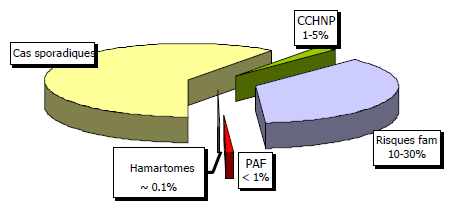
Risque moyen. Le risque de cancer colorectal augmente avec l’âge et l’histoire familiale. Le cancer colorectal est rare avant 50 ans mais après ce seuil son incidence augmente fortement. Les patients sans antécédent familiaux son considérés comme ayant un risque moyen. .
Risque familial non syndromique. Le cancer colorectal est peut-être le cancer familial le plus fréquent chez l’homme. On estime entre 5 et 10 % ceux attribués à une origine familiale. Ceux qui ont comme origine une variation génétique représentent seulement 1 à 5 % de l’ensemble des cancers colorectaux. Entre 10 et 30% des patients ont une histoire familiale de cancer colorectal .sans pour autant de signe héréditaire certain. Le caractère familial est reconnu et augmente le risque. Les parents au premier degré de patients ayant un cancer colorectal ont un risque deux à trois fois supérieur à celui d’une population témoin. En outre le risque augmente d’autant que le patient est proche de parents présentant un tel cancer, et que l’âge augmente. Les malades souffrant de cancer colorectal présentent aussi un risque important de développer un autre cancer. En conclusion, le risque de cancer colorectal augmente chez les personnes avec une histoire familiale de cancer colorectal non syndromique ou chez ceux avec des antécédents d’adénome avant 60 ans. (Tableau 1).
Tableau 1 Risque familial de cancer colorectal

RR, risque relatif; IC : intervalles de confiance.
Adapté de : Burt RW (Gastroenterol Clin North Am 1996;25:793–803) et Johns LE, Houlston RS (Am J Gastroenterol 2001;96:2992–3003).
Risque familial syndromique. Polypose adénomateux familial. Il est autosomique dominant. Un tiers des nouveaux cas est causé par une mutation de novo. .
Le cancer colique héréditaire non sur polypose (CCHNP) ou syndrome de Lynch. Le CCHNP avec transmission autosomique dominante est la forme la plus habituelle de cancer colorectal familial. Un groupe de consensus a établi une liste de critères (critères Amsterdam II) qui suggère la présence de phénotypes CCHNP. (Tableau 2). .
Tableau 2 Critères Amsterdam II pour le cancer colique héréditaire non sur polypose (CCHNP).

D’autres syndromes familiaux moins fréquents peuvent être :
- Une polypose juvénile
- Un syndrome de Peutz–Jeghers
- Un syndrome de Cowden
Facteurs de risque cliniques dans une maladie inflammatoire de l’intestin. Il existe un risque accru de développer un cancer colorectal chez les patients présentant une maladie inflammatoire de l’intestin. L’incidence cumulée du cancer augmente approximativement 8 à 10 ans après le début de la maladie et augmente à 15 % sur 30 ans. Les facteurs de risque incluent une longue durée de la maladie, son étendue, l’âge précoce de l’apparition et la présence de cholangite primaire sclérosante ou une pathologie sténotique. Une thérapie pharmacologique inappropriée (éventuellement) ou l’absence de surveillance appropriée peut aussi se révéler un risque supplémentaire. .
4. Tests de dépistage et évidence, 1: tests dans les selles, sang occulte et ADN
Du sang ou d’autres composants tissulaires peuvent être détectés dans les selles bien avant le développement des symptômes cliniques du cancer colorectal. Pour cette raison une recherche de sang dans les selles peut permettre une détection précoce du cancer et un dépistage du cancer colorectal chez les personnes sans symptômes. La méthode la plus habituelle est la détection de sang occulte dans les selles. Plusieurs études randomisées ont prouvé que cela réduisait la mortalité du cancer colorectal de 15-33% dans des cohortes voire même de 45% selon le type et la fréquence des tests.
Test du sang occulte: Le test au guaiac est le plus fréquemment utilisé pour détecter du sang occulte dans les selles (test de RSOS). Il détecte l’activité peroxydase de l’hème intacte, mais cela le rend susceptible de réagir à d’autres peroxydases dans les selles, telles que celles provenant de certains fruits, légumes et de viandes rouges. Des restrictions et régimes alimentaires sont donc nécessaires pour éviter des résultats faux positifs.
Plusieurs problèmes existent relativement au test de sang occulte dans le dépistage du cancer colorectal. La sensibilité du test est seulement de 50-60% quand il n’est fait qu’une fois, mais peut monter à 90 % quand il est répété tous les deux ans sur une longue période de temps. Quoique la sensibilité puisse être augmentée par réhydratation, cela conduit à une variabilité de réactions qui invalide la méthode en tant que procédure de dépistage. Une sensibilité faible conduit à un nombre élevé de résultats faux négatifs et provoque un effet d’assurance erronée. La majorité des cancers identifiés par recherche de sang occulte dans les selles sont faux positifs et ces patients seront soumis à des investigations diagnostiques inutiles, d’ordinaire des colonoscopies. Une autre difficulté pour la recherche de sang occulte dans les selles est qu’elle requiert une compliance du patient pendant de nombreuses années.
On tend actuellement à remplacer dans de nombreux pays le test de dépistage de sang occulte dans les selles par guaiac par des tests immunochimiques qui détectent l’hémoglobine en utilisant des techniques spécifiques. De tels tests évitent le recours aux régimes alimentaires. Leur facilité d’utilisation varie, quelques uns le sont davantage et sont mieux acceptés par les patients. La limite de sensibilité de ces tests immunochimiques demande encore à être validée.
Tests d’analyse d’ADN dans les selles comme dépistage du cancer colorectal. On a suggéré que l’identification d’ADN anormal dans les selles soit une méthode de diagnostic précoce de cancer colorectal avec mutation du gène APC. . Il reste cependant à déterminer l’association optimale des marqueurs moléculaires, et la faisabilité de tels tests quand ils seraient appliqués à l’ensemble de la population. Une étude a comparé un panel de 21 mutations en comparaison avec des tests de sang occulte pratiqués chez 2.507 sujets. La sensibilité du panel ADN était de 52 % en comparaison avec 13 % dans le cas du guaiac et la spécificité était similaire (94.4% vs. 95.2%). Les résultats avec le test au guaiac étaient extrêmement bas.
Plusieurs petites études complémentaires ont té conduites montrant une sensitivité de 65% et une spécificité de 95%. Une nouvelle version avec de moindres mutations a conduit la sensibilité au dessus de 80%.
5. Tests de dépistage et évidence, 2: endoscopie et colonographie par tomodensitométrie
Cette section décrit les procédures endoscopiques et radiographiques utilisées pour diagnostiquer un cancer colorectal et l’évidence qui régit leur emploi.
5.1 Procédures endoscopiques de dépistage
La Sigmoidoscopie flexible permet un examen direct de la surface interne du gros intestin jusqu’à 60 cm environ de la marge anale. Cette technique peut détecter des polypes colorectaux et des cancers et elle est aussi utilisée pour enlever des polypes ou prélever des tissus pour examen histologique. La sigmoidoscopie flexible peut être conduite même par des non médecins ; elle prend moins de temps que la colonoscopie, la préparation intestinale est plus facile et plus rapide ; la morbidité est négligeable là où la polypectomie n’est pas requise; et aucune sédation ou anesthésie n’est exigée. Toutefois, l’inconvénient évident est que l’examen du colon gauche manque les lésions du côté droit. Alors que la spécificité de ce qui est découvert dans une procédure endoscopique est très haute (98–100%, peu de faux positifs), la sensibilité est basse pour la globalité du colon et varie de 35% à 70% en raison du nombre significatif d’adénomes situés sur le côté droit en l’absence de tumeur distale et sont donc manqués lors d’une sigmoidoscopie flexible.
La sigmoidoscopie est utilisée dans le dépistage d’individus asymptomatiques pour une détection et une prévention précoces des cancers. Des études de cas ont clairement montré que la sigmoidoscopie permet une diminution de la mortalité par cancer de 60–70%. Des complications majeures surviennent dans un cas sur 10.000.
La Colonoscopie permet la détection et l’exérèse des polypes et des biopsies pour rechercher des cancers du colon. La spécificité et la sensibilité de la colonoscopie lors de la recherche de polypes ou de cancers sont hautes (au moins 95% en ce qui concerne les gros polypes, voir ci-après). Le taux d’échec dans la détection des polypes, sur la base d’études, est de 15–25% dans le cas d’adénomes inférieurs à 5 mm de diamètre et de 0–6% pour ceux de 10 mm ou plus.
Il n’existe aucune étude prospective randomisée qui ait examiné l’impact de la colonoscopie sur l’incidence ou la mortalité. Cependant des suivis à long terme de patients après polypectomies réalisées aux USA par le United States National Polyp Study ont démontré une réduction d’environ 90% de l’incidence et de la mortalité du cancer colorectal, en utilisant des modèles mathématiques.
Idéalement, une procédure de dépistage devrait être simple, non onéreuse et susceptible d’être appliquée à l’ensemble de la population à risque. Bien que ces critères ne soient pas remplis par la colonoscopie, cette approche reste cependant « la norme d’or et les patients ayant un résultat positif après tout autre test de dépistage (recherche de sang occulte dans les selles, sigmoidoscopie, colonographie par tomodensitométrie devraient subir une colonoscopie si c’est possible. Là où ces ressources sont disponibles, la colonoscopie directe est devenue la procédure la plus courante dans le dépistage du cancer colorectal. Des complications majeures se produisent dans 1–2 cas sur 1000.
5.2 Procédures de dépistage radiographiques
Lavement baryté à double contraste. Bien que le lavement baryté à double contraste permette l’évaluation du colon entier, sa spécificité et sa sensibilité sont inférieures à celles de la colonoscopie et de la colonographie par tomodensitométrie. Même pour les polypes larges et les cancers il offre une sensibilité substantiellement plus basse (48%) que la colonoscopie avec plus de faux positifs que la colonoscopie (artefacts diagnostiqués comme polypes). Les patients avec un lavement baryté anormal doivent alors subir une colonoscopie. Cependant le lavement baryté à double contraste se pratique couramment, et le fait qu’il puisse permettre de détecter 50 % des polypes larges serait en faveur de son utilisation là où d’autres ressources ne sont pas possibles ni disponibles.
La colonographie par tomodensitométrie. On procède à un examen densitométrique en coupes très fines chevauchées à section mince de l’abdomen suivi par l’analyse et l’interprétation des images pour reconstruire la lumière colique en deux et trois dimensions (colonoscopie virtuelle), en mode reconstructions multiplanaires 2D (MPR) et en mode rendu surfacique endoscopique 3D.. La procédure requiert une insufflation du colon pour une tolérance maximum (approximativement 2 L d’air ou de dioxyde de carbone) et une préparation de l’intestin. L’ingestion de produit de contraste oral peut « marquer » le matériel fécal et le fluide (tagging fécal) qui peut alors être électroniquement effacé de l’image dur l’ordinateur.
Une méta-analyse des études utilisant la colonographie par tomodensitométrie dans la détection des polypes et cancers colorectaux a mis en valeur une sensibilité élevée (93%) et une haute spécificité (97%) en ce qui s’agit de polypes de taille supérieure à 10 mm. Cependant lorsqu’il s’agit de polypes dont la taille varie de médiane ou grande (6 mm or plus), la sensibilité moyenne descend à 86%, avec une spécificité de 86%. Si les polypes sont de toutes les tailles, les études ont montré une sensibilité trop hétérogène (variant de 45 à 97 %) et une spécificité également trop hétérogène (variant de 26 à 97 %). Alors que la sensibilité de la colonographie par tomodensitométrie est satisfaisante pour les cancers ou polypes larges, la détection des polypes d’une taille comprise entre 6–9-mm ne donne pas la même satisfaction. Un inconvénient important de la colonographie par tomodensitométrie dans le dépistage des patients à risque élevé est qu’elle ne repère pas les lésions plates..
Un inconvénient majeur de l’utilisation de cette technique comme procédure de dépistage est l’exposition répétée des patients à une radiation ionisante. Récemment une technologie multidétectrice ou multi-coupes a réduit la durée d’exposition et la dose de radiation tout en maintenant une haute résolution spatiale. Pour cette raison, on étudie en Europe la question de la colonographie à résonance magnétique.
En outre, la question n’a pas été tranchée de savoir quand soumettre les patients à une colonoscopie sur la base de la taille des polypes visualisés lors d’une colonographie par tomodensitométrie. Cela a un énorme impact sur le coût du dépistage. Un autre inconvénient est que l’examen requiert une préparation complète de l’intestin. Si les patients ont besoin d’une colonoscopie, ils doivent subir une seconde préparation sauf si on peut procéder aux deux examens le même jour. Enfin, des découvertes extra-intestinales peuvent conduire à des examens radiologiques ou chirurgicaux complémentaires et augmenter les coûts. Les complications majeures sont rares.
6. Rapport coût-efficacité du dépistage du cancer colorectal
Toutes les options standard du dépistage du cancer colorectal ont un bon rapport cout efficacité, comme ce peut être le cas ailleurs pour la mammographie et un meilleur rapport cout efficacité que d’autres formes de dépistage médical (par exemple du cholestérol dans l’hypertension). Une colonoscopie systématique de dépistage chez les parents au premier degré des patients atteint de cancer colorectal dès 40 ans, offre un bénéfice économique. En comparaison avec une poly chimiothérapie intensive, le dépistage présente un bon rapport cout efficacité..
7. Diverses étapes de la cascade du dépistage
7.1 Introduction
On passe en revue ici les différentes options de dépistage chez les hommes ou femmes de plus de 50 ans, qui sont à risque moyen ou élevé. Ces options prennent en compte la disponibilité de la colonoscopie, de la sigmoidoscopie flexible, de la recherche de sang occulte dans les selles et du lavement baryté. Là où les ressources diagnostiques sont sévèrement limitées, l’option la plus réaliste serait une recherche de sang occulte dans les selles par an ou tous les deux ans chez les hommes ou femmes à risque de plus de 50 ans.
Le type de coupes utilisées dépend des ressources de dépistage et des habitudes alimentaires de la population.
Des tests à la positivité moindre tels que Hemoccult II auront un impact financier moindre que d’autres avec des coupes plus sensibles tels que SENSA. Les tests immunochimiques sont les meilleurs, en ce qu’ils ne demandent que deux ou trois jours d’analyse et ne requièrent aucun régime alimentaire, mais ils se révèlent plus onéreux ce qui est un argument de poids là où les ressources financières ne sont pas importantes.
Le diagnostic peut s’établir par colonoscopie là où c’est possible ou par lavement baryté, si la colonoscopie n’est pas très facile à faire. Et donc, la décision d’identifier séparément les personnes à risque dépend de la disponibilité de la colonoscopie. Si son usage est restreint, alors les personnes à risque seront soumises au même dépistage que les personnes à risque moyen.
7.2 Cascade pour le dépistage du cancer colorectal
Ka cascade de dépistage du cancer colorectal consiste en un ensemble de recommandations. Elles seront appliquées selon le niveau des ressources disponibles, en commençant par 1 (ressources les plus élevées) et se terminant par 6 (ressources disponibles minimales). .
Niveau de cascade 1. Les recommandations qui suivent s’appliquent aux pays a niveau de vie relativement élevé (sur le plan financier, professionnel, technique) et où l’incidence du cancer colorectal et sa mortalité sont hautes (données du CIRC-IARC) et où cela tient une place importante dans les priorités de santé publique. .
Recommandations de dépistage pour les personnes à risque moyen. Colonoscopie pour hommes et femmes à risque moyen, à partir de 50 ans, et tous les dix ans, en l’absence de facteurs qui les placeraient dans un risque plus élevé. .
Recommandations de dépistage pour les personnes à risque élevé:
- — Les personnes avec une histoire familiale de cancer colorectal ou de polypes adénomateux.
— Les personnes avec un parent au premier degré (parent, fratrie ou enfant) avec un cancer du colon ou des polypes adénomateux diagnostiqués avant 60 ans, ou avec deux parents au premier degré ayant un cancer colorectal diagnostiqué quelque soit l’âge où le diagnostic a été porté devraient recevoir le conseil de subir un test de dépistage par colonoscopie à partir de 40 ans, ou 10 ans avant l’âge auquel le diagnostic a été porté dans leur famille, et cela tous les cinq ans.
— Les personnes ayant un parent au premier degré avec cancer du colon ou un polype adénomateux diagnostiqué après 60 ans, ou avec deux parents au second degré avec cancer colorectal devraient recevoir le conseil de subir un dépistage en tant que sujets à un risque moyen, mais à partir de 40 ans.
— Les personnes avec un parent au second degré (grands-parents, tante ou oncle) ou au troisième degré (arrière grands-parents ou cousin) souffrant d’un cancer colorectal devrait recevoir le conseil de subir un test de dépistage comme susceptibles de courir un risque moyen. .
- Polypose adénomateuse familiale. Les personnes sur lesquelles a été porté un diagnostic génétique de polypose adénomateuse familiale ou qui sont à risque d’en avoir une mais chez qui le test n’a pas été fait ou n’est pas possible, devraient subir annuellement une sigmoidoscopie, à partir de 10-12 ans pour savoir si elles montrent une malformation génétique. Un test génétique devrait être envisagé chez les patients avec polypose adénomateuse familiale et des parents à risque. Un conseil génétique devrait accompagner le test génétique et l’éventualité d’une colostomie. .
- Cancer colorectal héréditaire sans polypose. Les personnes avec un diagnostic génétique ou clinique de Cancer colorectal héréditaire sans polypose ou qui en courent un risque élevé, devraient subir une colonoscopie chaque 1-2 ans, à partir de 20-25 ans ou 10 ans plus tôt que l’âge auquel le cancer du colon le plus précoce a été diagnostiqué dans leur famille. quelque soit la première étape. Un test génétique du cancer colorectal héréditaire sans polypose devrait être proposé aux parents au premier degré des patients avec une altération des gènes MMR, gènes de réparation des mésappariements de l’ADN. Il devrait aussi être proposé lorsque la mutation familiale n’est pas encore connue, mais qu’un des trois premiers critères révisés de Bethesda est rencontré.
- Les personnes avec une histoire de syndrome de l’intestin inflammatoire ou de polype adénomateux ou de cancer colorectal sont candidates à un suivi plutôt qu’à un simple dépistage. Des recommandations ont été publiées quant à leur surveillance.
Niveau de cascade 2. Les recommandations sont les mêmes que pour le niveau 1, mais elles s’appliquent là où les possibilités de colonoscopie sont limitées.
Recommandations de dépistage pour des personnes à risque moyen. . Colonoscopie pour les hommes ou femmes à risque moyen à 50 ans, une fois dans leur vie, en l’absence de facteurs qui les placeraient dans un risque élevé. .
Recommandations de dépistage chez les personnes à risque élevé. . Les recommandations de dépistage chez les personnes à risque élevé sont les mêmes que dans la cascade 1.
Niveau de cascade 3. Les recommandations sont les mêmes que pour le niveau 1, mais elles s’appliquent là où les possibilités de colonoscopie sont plus limitées mais où les sigmoidoscopies flexibles sont possibles.
Recommandations de dépistage pour les personnes à risque moyen. Sigmoidoscopie flexible pour les hommes et femmes à risque moyen à partir de 50 ans, et tous les cinq ans, en l’absence de facteurs qui les placeraient en un risque élevé. Le diagnostic se confortera par la colonoscopie si sigmoidoscopie positive. .
Recommandations de dépistage pour les personnes à risque élevé. Elles sont les mêmes que dans le niveau 1. .
Niveau de cascade 4. Les recommandations sont les mêmes que pour le niveau 3, mais elles s‘appliquent là où les possibilités de sigmoidoscopie flexible et de colonoscopie sont plus limitées.
Recommandations de dépistage chez les personnes à risque moyen. Sigmoidoscopie flexible chez les hommes et femmes à risque moyen une fois dans leur vie, à 50 ans, en l’absence de facteurs qui les placeraient en risque élevé. Le diagnostic se confortera par la colonoscopie si sigmoidoscopie positive ou cancer avancé, selon la disponibilité de la colonoscopie. .
Recommandations de dépistage chez les personnes à risque élevé. Dans ce cas elles sont les mêmes qu’au niveau 1. .
Niveau de cascade 5. Les recommandations sont les mêmes que pour le niveau 4, mais elles s’appliquent là où le diagnostic par colonoscopie est sévèrement limité. .
Recommandations de dépistage chez les personnes à risque moyen. Sigmoidoscopie flexible chez les hommes et femmes à risque moyen une fois dans leur vie, à l’âge de 50 ans. Diagnostic par colonoscopie seulement en cas de cancer avancé. .
Recommandations de dépistage chez les personnes à risque élevé. Elles dépendent de la disponibilité de la colonoscopie.
Niveau de cascade 6. Les recommandations sont les mêmes que pour le niveau 1., mais elles s’appliquent là où les possibilités de colonoscopie et de sigmoidoscopie flexible sont sévèrement limitées. .
Recommandations de dépistage chez les personnes à risque moyen La recherche de sang fécal doit être faite annuellement à partir de 50 ans, chez les hommes et femmes à risque moyen, en l’absence de facteurs qui les placeraient dans un risque élevé. Le type de test utilisé dépend des possibilités de colonoscopie et des habitudes alimentaires de la population. Le diagnostic sera porté à l’aide de colonoscopie si elle peut être faite, sinon par lavement baryté. .
Recommandations de dépistage chez les personnes à risque élevé. La décision d’identifier séparément ces personnes en vue d’un dépistage spécifique (voir niveau 1) dépendra de la possibilité de procéder à une colonoscopie. Si cette technique n’est pas disponible, on les dépistera comme les personnes à risque moyen. .
7. 3 Nouveaux tests
La colonographie par tomodensitométrie et le test par ADN ne sont en général possibles que dans quelques pays dont les ressources sont élevées mais pas globalement. Cependant, là où elles existent, ces méthodes peuvent être utilisées pour les hommes ou femmes à risque moyen, à partir de 50 ans, qui ne souhaitent pas subir de dépistage avec des méthodes plus standard, afin d’élever le nombre de personnes ainsi soumis à dépistage dans ces pays. .
7.4 Recommandations pour action — installer un programme
Recommandations pour action — aspect général:
- Développer et répandre des programmes structurés de formation auprès des acteurs de santé et des leaders politiques ou des preneurs de décisions. Tous ces programmes devraient atteindre chacune des cibles ainsi définies de manière appropriée. .
- Développer des normes de qualité basées sur l’évidence pour l’ensemble du processus de dépistage.
- Développer et répandre des procédures cliniques non onéreuses et faciles à utiliser..
- Promouvoir le dépistage au plan national et local. .
- Promouvoir le dépistage du cancer colorectal comme faisant partie d’un ensemble exhaustif de prévention. .
Recommandations pour action — design du programme
Planifier le programme de dépistage:
- Une population cible devra être identifiée, avec âge et facteurs de risque par exemple familiaux chez des hommes ou de femmes asymptomatiques..
- La décision de développer un dépistage de cancer colorectal doit s’appuyer sur l’importance de cette pathologie au sein de la population à soumettre à dépistage.
- La stratégie de dépistage (test, intervalles, âge moyen) devra être basée sur l’évidence (recommandations pratiques et guidelines), sur la disponibilité des ressources, sur le niveau de risque et sur l’acceptation culturelle par la population. .
- Il faudra recevoir l’appui de groupes professionnels importants et bénéficier de l’aide de groupes de patients et de la presse. .
- Il faudra évaluer la faisabilité du programme proposé et s’assurer de l’attribution des ressources (financières, en personnel, techniques,…).
- Il sera nécessaire d’évaluer les besoins spécifiques que ce soit sur le plan culturel ou linguistique de la population. .
Développement du programme de dépistage:
- Identifier les cibles du développement d’un tel programme et s’assurer de la communication (formation) avec les personnels et acteurs de santé (médecins généralistes et autres) et la population visée. .
- Développer et répandre les Recommandations pratiques et guidelines relatives au dépistage, au diagnostic, au traitement et à la surveillance des patients de manière à favoriser la compliance du patient.
- Développer des méthodes pour inciter les patients à subir un dépistage initial et à se faire suivre ultérieurement. .
Contrôle du programme de dépistage:
- Gérer soigneusement les étapes suivantes: dépistage initial, dépistage subséquents et ultérieurs, suivi en cas de tests positifs. .
- Compliance avec les recommandations de surveillance.
- Des mesures de la qualité du programme doivent être mises en place ainsi que des évaluations régulières. .
- Etude globale, y compris les taux de détection, distribution du cancer par stade, détection des adénomes, complications et finalement effet sur l’incidence et la mortalité dans la population. .
8. Où obtenir de l’aide
8.1 IDCA
- http://omge.org/?idca The International Digestive Cancer Alliance (IDCA)
La mission de l’International Digestive Cancer Alliance est de promouvoir la prévention et la thérapie des cancers digestifs à travers le monde, dans le cadre d’une alliance internationale d’organisations qui partagent le même but.
8.2 International Agency for Research on Cancer (IARC) Centre International de Recherches sur le Cancer (CIRC)
- http://www.iarc.fr/IARCPress/index.php
Le CIRC appartient à l’Organisation Mondiale de la Santé. La majeure partie de son action et de sa recherche porte sur l’épidémiologie, la carcinogénèse environnementale et la formation. .
8.3 United States Centers for Disease Control and Prevention (CDC)
8.4 ACS American Cancer Society (ACS)
8.5 Union Internationale Contre le Cancer (International Union Against Cancer, UICC)
- http://www.uicc.org/
Etant la plus grande organisation indépendante à but non lucratif au monde, contre le cancer, l’UICC catalyse une action collective et un dialogue responsable. L’UICC regroupe un grand nombre d’organisations, y compris des associations de bénévoles, des centres de recherche et de traitement, des autorités sanitaires, des réseaux de patients, et des groupes de pression. .
9. Sites Web utiles, recommandations pratiques et références bibliographiques sélectionnées
9.1 Recommandations, consensus,
Abréviations: ACG, American College of Gastroenterology; ACS, American Cancer Society; AGA, American Gastroenterological Association; ASCRS, American Society of Colorectal Surgeons; ASGE, American Society of Gastrointestinal Endoscopy; BSG, British Society of Gastroenterology; DGVS, German Society for Digestive and Metabolic Diseases; FMSD, Finnish Medical Society Duodecim; ICSI, Institute for Clinical Systems Improvement; NCCN, National Comprehensive Cancer Network; NICE, National Institute of Clinical Excellence; NZGG, New Zealand Guidelines Group; SIGN, Scottish Intercollegiate Guidelines Network; SMH, Singapore Ministry of Health; WGO, World Gastroenterology Organisation.
9.2 Lectures complémentaires
- Lieberman DA, Weiss DG; Veterans Affairs Cooperative Study Group 380. One-time screening for colorectal cancer with combined fecal occult-blood testing and examination of the distal colon. N Engl J Med 2001;345:555–60 (PMID: 11529208).
- Barclay RL, Vicari JJ, Doughty AS, Johanson JF, Greenlaw RL. Colonoscopic withdrawal times and adenoma detection during screening colonoscopy. N Engl J Med 2006;355:2533–41 (PMID: 17167136).
- Sonnenberg A, Delcò F, Inadomi JM. Cost-effectiveness of colonoscopy in screening for colorectal cancer. Ann Intern Med 2000;133:573–84 (PMID: 11033584).
- Burt R, Neklason DW. Genetic testing for inherited colon cancer. Gastroenterology 2005;128:1696–1716 (PMID: 15887160).
- Faivre J, Dancourt V, Lejeune C, Tazi MA, Lamour J, Gerard D, et al. Reduction in colorectal cancer mortality by fecal occult blood screening in a French controlled study. Gastroenterology 2004;126):1674–80 (PMID: 15188160).
- Imperiale TF, Ransohoff DF, Itzkowitz SH, Turnbull BA, Ross ME. Fecal DNA versus fecal occult blood for colorectal-cancer screening in an average-risk population. N Engl J Med 2004;351:2704–14 (PMID: 15616205).
- Kronborg O, Jorgensen OD, Fenger C, Rasmussen M. Randomized study of biennial screening with a fecal occult blood test: results after nine screening rounds. Scand J Gastroenterol 2004;39:846–51 (PMID: 15513382).
- Parkin DM, Whelan SL, Ferlay J, et al., editors. Cancer incidence in five continents, vol. 8. Lyons: International Agency for Research on Cancer, 2002 (IARC Scientific Publications, no. 155) (PMID: 12812229).
- Winawer S, Fletcher R, Rex D, Bond J, Burt R, Ferrucci J, et al. Colorectal cancer screening and surveillance: clinical guidelines and rationale — update based on new evidence. Gastroenterology 2003;124:544–60 (PMID: 12557158).
- Winawer SJ, Zauber AG, Fletcher RH, Stillman JS, O’Brien MJ, Levin B, et al. Guidelines for colonoscopy surveillance after polypectomy: a consensus update by the US Multi-Society Task Force on Colorectal Cancer and the American Cancer Society. Gastroenterology 2006;130:1872–85 (PMID: 16697750).
- Young GP, St. John DJ, Winawer SJ, Rozen P; WHO (World Health Organization) and OMED (World Organization for Digestive Endoscopy). Choice of fecal occult blood tests for colorectal cancer screening: recommendations based on performance characteristics in population studies: a WHO (World Health Organization) and OMED (World Organization for Digestive Endoscopy) report. Am J Gastroenterol 2002;97:2499–507 (PMID: 12385430).
- Hewitson P, Glasziou P, Irwig L, Towler B, Watson E. Screening for colorectal cancer using the faecal occult blood test, Hemoccult. Cochrane Database Syst Rev 2007;(1):CD001216 (PMID: 17253456).
- Regula J, Rupinski M, Kraszewska E, Polkowski M, Pachlewski J, Orlowska J, et al. Colonoscopy in colorectal-cancer screening for detection of advanced neoplasia. N Engl J Med 2006;355:1863–72 (PMID: 17079760).
- Winawer SJ, Zauber AG, Ho MN, O’Brien MJ, Gottlieb LS, Sternberg SS, et al. Prevention of colorectal cancer by colonoscopic polypectomy. The National Polyp Study Workgroup. N Engl J Med 1993;329:1977–81 (PMID: 8247072).
- Winawer SJ, Stewart ET, Zauber AG, Bond JH, Ansel H, Waye JD, et al. A comparison of colonoscopy and double-contrast barium enema for surveillance after polypectomy. National Polyp Study Work Group. N Engl J Med 2000;342:1766–72 (PMID 10852998).
- Winawer SJ, Zauber AG, Gerdes H, O’Brien MJ, Gottlieb LS, Sternberg SS, et al. Risk of colorectal cancer in the families of patients with adenomatous polyps. National Polyp Study Workgroup. N Engl J Med 1996;334:82–7 (PMID: 8531963).
- Itzkowitz-Steven-H, Jandorf-Lina, Brand-Randall, Rabeneck-Linda, Schroy-Paul-C-3rd, Sontag-Stephen, Johnson-David, Skoletsky-Joel, Durkee-Kris, Markowitz-Sanford, Shuber- Anthony. Improved fecal DNA test for colorectal cancer screening. Clinical gastroenterology and hepatology Jan 2007 08 Dec 2006 , vol. 5, no. 1, p.111-7 PMID: 17161655
- Kim-David-H, Pickhardt-Perry-J, Taylor-Andrew-J, Leung-Winifred-K, Winter-Thomas-C, Hinshaw-J-Louis, Gopal-Deepak-V, Reichelderfer-Mark, Hsu-Richard-H, Pfau-Patrick-R. CT colonography versus colonoscopy for the detection of advanced neoplasia. N Engl J Med, 4 Oct 2007, vol. 357, no. 14, p. 1403-12, PMID: 17914041
- Allison JE, Sakoda LC, Levin TR, Tucker JP, Tekawa IS, Cuff T, Pauly MP, Shlager L, Palitz AM, Zhao WK, Schwartz JS, Ransohoff DF, Selby JV. Screening for colorectal neoplasms with new fecal occult blood tests: update on performance characteristics. J Natl Cancer Inst. 2007 Oct 3;99(19):1462-70. PMID: 17895475
Remerciements
Nous remercions le Centre International de Recherches sur le Cancer (CIRC) International Agency for Research on Cancer (IARC); www.iarc.fr fpour les données et tableaux aimablement fournis et aux Annals of Oncology (http://annonc.oxfordjournals.org/) pour les données publiées au Congrès de Oslo. .
10. Questions et commentaires
Le Comité des recommandations pratiques accueillera avec intérêt vos commentaires et vos questions. Pensez vous que certaines procédures comportent d’autres risques ? Merci de ne pas hésiter à cliquer sur l'icône ci-dessous pour nous faire connaître vos vues et votre expérience sur cette question.
guidelines@worldgastroenterology.org







