Prof. S. Winawer (Presidente, EE.UU.)
Prof. M. Classen (Vice Presidente, Alemania)
Prof. R. Lambert (Vice Presidente, Francia)
Prof. M. Fried (Suiza)
Prof. P. Dite (República Checa)
Prof. K.L. Goh (Malasia)
Prof. F. Guarner (España)
Prof. D. Lieberman (EE.UU.)
Prof. R. Eliakim (Israel)
Prof. B. Levin (EE.UU.)
Prof. R. Saenz (Chile)
Prof. A.G. Khan (Pakistán)
Prof. I. Khalif (Rusia)
Prof. A. Lanas (España)
Prof. G. Lindberg (Suecia)
Prof. M.J. O’Brien (EE.UU.)
Prof. G. Young (Australia)
Dr. J. Krabshuis (Francia)
Prof. R. Smith (EE.UU.)
Prof. W. Schmiegel (Alemania)
Prof. D. Rex (EE.UU.)
Prof. N. Amrani (Marruecos)
Prof. A. Zauber (EE.UU.)
1. Introducción
El cáncer colorrectal (CCR) es un problema mundial, con una incidencia anual de aproximadamente 1 millón de casos y una mortalidad anual de más de 500.000. El número absoluto de casos aumentará en las próximas dos décadas como resultado del envejecimiento y la expansión de las poblaciones, tanto en los países desarrollados como en los países en desarrollo.
El CCR es la segunda causa en frecuencia de mortalidad por cáncer entre hombres y mujeres. La mayoría de los CCR aparecen a partir de adenomas esporádicos, y unos pocos a partir de síndromes genéticos de poliposis o enfermedad inflamatoria intestinal (EII). El término “pólipo” se refiere a una masa discreta que protruye en la luz intestinal. Según los datos de tamizaje utilizando colonoscopía, la prevalencia descrita de los pólipos adenomatosos está en el rango de 18 a 36%.
El riesgo de CCR varía de un país a otro e inclusive dentro de un mismo país. El riesgo también varía entre los individuos según su dieta, estilo de vida y factores hereditarios.
El hallazgo neoplásico más común del tamizaje de cáncer colorrectal es el adenoma. Luego de su exéresis, los pacientes deben integrarse a un programa de vigilancia para su seguimiento, igual que la generalidad de pacientes con cáncer identificado y tratado.
Estas guías están dirigidas al tamizaje: el examen de hombres y mujeres asintomáticos con probabilidad de tener pólipos adenomatosos o cáncer. El tamizaje debe aplicarse dentro del marco de un programa que incluya: prevención primaria (dieta, estilo de vida), evaluación diagnóstica oportuna con colonoscopía (donde estuviera disponible y en concordancia con la cascada) en los individuos pesquisados positivos, y el tratamiento oportuno (polipectomía, cirugía).
El tamizaje del cáncer colorrectal constituye un desafío especial, como lo reflejan las bajas tasas de los tamizajes actuales en la mayoría de los países donde existe un alto riesgo de cáncer colorrectal. El tamizaje del cáncer colorrectal es complejo, ya que hay múltiples opciones, requiere un esfuerzo considerable del paciente (frotis de sangre oculta fecal, preparación para colonoscopía, etc.), y exige sedación y un socio en el sistema de salud para algunas pruebas (colonoscopía). Para que un programa de pesquisa tenga éxito, deben darse múltiples acontecimientos, comenzando con el conocimiento y la recomendación del médico de atención primaria, la aceptación del paciente, la cobertura financiera, la estratificación de riesgos, las pruebas de pesquisa, el diagnóstico oportuno, el tratamiento oportuno y un seguimiento apropiado. Si hay una falla en cualquiera de esos pasos o si no se realizan con una alta calidad, el tamizaje fracasará.
2. Metodología y revisión bibliográfica
Las pautas de la OMGE resumen lo que se conoce y se ha publicado en las revisiones sistemáticas, pautas basadas en la evidencia y ensayos de alta calidad existentes, y esta información luego se configura para hacer que la pauta sea lo más pertinente y accesible mundialmente como sea posible. Habitualmente, esto implica armar diferentes enfoques para lograr los mismos fines — cada enfoque difiere porque intenta considerar los recursos locales, las preferencias culturales y las políticas. Las pautas de la OMGE no son revisiones sistemáticas basadas en una revisión sistemática y completa de toda la evidencia y las pautas disponibles. Una guía mundial intenta distinguir entre las áreas con diferentes recursos y diferentes epidemiologías, y luego se traduce esa guía a los diferentes idiomas para facilitar la pertinencia y el acceso.
Esta guía fue redactada por un equipo de revisión siguiendo una serie de búsquedas bibliográficas para establecer lo que ha cambiado desde la primera declaración de posición de la OMGE sobre el tema de pesquisa de cáncer colorrectal, publicado en 2002 (http://omge.org/globalguidelines/statement03/statement3.htm).
Para buscar la evidencia disponible se utilizó una sintaxis más precisa que sensible para cada plataforma investigada. Las pautas pertinentes fueron buscadas en la plataforma United States National Guideline Clearinghouse en www.ngc.org y en los sitios web de las principales sociedades médicas vinculadas a la gastroenterología y el cáncer. Se hicieron búsquedas adicionales en Medline y EMBASE en la plataforma Dialog-Datastar desde 2003 en adelante. Una búsqueda en la biblioteca Cochrane arrojó 18 revisiones sistemáticas y 12 protocolos pertinentes. Se asignaron secciones específicas a cada miembro del equipo de revisión según su especialización y preferencias. El bibliotecario del equipo dio apoyo a cada equipo de sección realizando búsquedas especiales para dar mayor respaldo y detalle. Finalmente, se consultaron expertos internacionales para cada sección redactada por el equipo de revisión, y el presidente del equipo de revisión y el bibliotecario redactaron y editaron el documento completo.
3. Epidemiología del cáncer colorrectal
3.1 La carga del cáncer colorrectal
En la base de datos Globocan 2002 de la Agencia Internacional para Investigación sobre Cáncer (IARC), se estima que la carga mundial de cáncer colorrectal es 550.000 nuevos casos incidentales y 278.000 muertes para los hombres, y 473.000 nuevos casos incidentales y 255.000 muertes para las mujeres. En 2002, el cáncer colorrectal comprendía 9.4% de la carga de cáncer mundial en ambos sexos y era más frecuente en América del Norte, Australia, Nueva Zelanda, y partes de Europa. Esto llevó a que se considerara al cáncer colorrectal como una enfermedad del estilo de vida occidental.
3.2 Tendencias temporales en incidencia y mortalidad
Las tasas de mortalidad por cáncer colorrectal normalizadas por edad (ASR) en hombres y mujeres en los países occidentales se mantuvieron estables durante todo el siglo XX, y tal vez ahora hayan comenzado a disminuir; por otra parte, se están observando rápidos cambios en países considerados de bajo riesgo anteriormente.
En Europa, las tasas de mortalidad normalizadas por edad han aumentado en Europa del este y meridional, mientras que se han nivelado en la mayoría de los países de Europa del norte y central. En los últimos años, las tendencias de mortalidad tienden a ser sistemáticamente más favorables para las mujeres que para los hombres.
En EEUU las tendencias de las tasas de incidencia de cáncer colorrectal en los registros de Vigilancia Epidemiológica y Resultados Finales (SEER) sugieren que entre 1973 y 1989, la incidencia de cáncer de colon normalizada por edad en hombres se elevó 11% en los blancos y 39% en negros, al tanto que la incidencia de cáncer rectal cayó 5% en blancos y se elevó 27% en los negros. En las mujeres, la incidencia del cáncer de colon bajó 3% en blancas y aumentó 26% en las mujeres negras, al tanto que las tasas de cáncer rectal cayeron 7% y 10%, respectivamente. Desde 1990, las tasas de incidencia de cáncer de colon normalizadas por edad han estado disminuyendo. La práctica de prevención mediante polipectomía puede haber incidido en esto.
En Japón, las tasas de mortalidad normalizadas por edad para cáncer colorrectal eran bajas a mediados del siglo XX y aumentaron multiplicándose aproximadamente por tres en ambos sexos en los períodos entre 1955–74 y 1975–84.
Con una población mundial en proceso de envejecimiento, se espera que haya un aumento considerable del número de casos.
3.3 Factores familiares y genéticos del cáncer colorrectal
Fig. 1 Factores de riesgo familiar y cáncer colorrectal
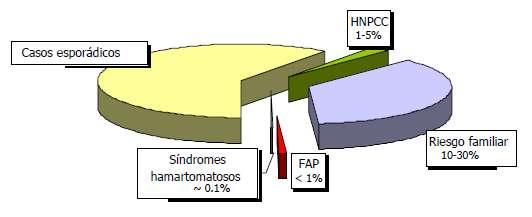
Riesgo promedio. El riesgo de CCR aumenta con la edad y los antecedentes familiares. El cáncer colorrectal es raro antes de los 50 años de edad, pero después de ese umbral, su incidencia aumenta drásticamente. Se considera que los individuos sin antecedentes familiares tienen un riesgo promedio.
Riesgo familiar no sindrómico. Tal vez el CCR sea el cáncer humano con mayor componente familiar. La proporción estimada de cánceres colorrectal que es atribuible a causas hereditarias varía de 5% a 30%. Los síndromes heredados con defectos genéticos conocidos, son responsables de 1–5% de todos los CCR. Entre 10% y 30% de los pacientes con CCR tienen antecedentes familiares de CCR pero no pertenecen a un síndrome hereditario conocido. Los acúmulos de casos familiares son comunes y aparentemente implican un mayor riesgo. Los parientes de primer grado de las personas con CCR tienen el doble o triple de riesgo de CCR en comparación con los testigos o comparado con la incidencia que se observa en las poblaciones. Además, el riesgo aumenta con la cantidad de parientes con CCR, cuanto más cercanos sean los parientes al paciente y con la edad de CCR en los miembros de la familia. Los individuos con antecedentes personales de cáncer colorrectal también tienen un mayor riesgo de presentar cáncer posteriormente. Por lo tanto, el riesgo de CCR aumenta en las personas con antecedentes familiares de CCR no sindrómico y en aquellos con antecedentes de adenomas en parientes cercanos menores de 60 años. (Tabla 1).
Tabla 1 Riesgo familiar de cáncer colorrectal

Un pariente de primer grado con un adenoma < 60 a 1.99 1.55 a 2.55
RR, riesgo relativo; IC, intervalos de confianza.
Adaptado de: Burt RW (Gastroenterol Clin North Am 1996;25:793–803) and Johns LE, Houlsan RS (Am J Gastroenterol 2001;96:2992–3003).
Riesgo familiar sindrómico. Poliposis adenomatosa familiar (FAP por sus siglas en inglés). La FAP es una entidad autosómica dominante. Un tercio de los casos nuevos son provocados por una mutación de novo.
Cáncer colorrectal no polipósico hereditario (HNPCC) o síndrome de Lynch. El HNPCC con transmisión autosómica dominante es la forma más común de cáncer colorrectal familiar sindrómico. Un grupo de consenso estableció una lista de criterios (los criterios de Amsterdam II) que sugieren la presencia del fenotipo HNPCC (Tabla 2).
Tabla 2 Criterios de Amsterdam II para cáncer colorrectal no polipósico hereditario (HNPCC)

Otros síndromes familiares menos comunes son:
- Poliposis juvenil (PJ)
- Síndrome de Peutz–Jeghers (PJ)
- Síndrome de Cowden
Factores clínicos de riesgo en la enfermedad intestinal inflamatoria. El aumento del riesgo de presentar cáncer colorrectal en pacientes con EII está bien establecido. La incidencia acumulada del cáncer comienza a aumentar aproximadamente 8–10 años después de la instalación de la enfermedad y aumenta a 15% a los 30 años. Los factores de riesgo incluyen la larga duración de la enfermedad, la extensión de la enfermedad, la juventud del paciente al aparecer la enfermedad, y la presencia de enfermedad estenótica o colangitis esclerosante primaria complicando el cuadro. También se pueden plantear la terapia farmacológica inadecuada (posiblemente) y falta de vigilancia adecuada.
4. Pruebas de tamizaje y evidencias, 1: Pruebas de heces, sangre oculta, y ADN
Los cánceres colorrectales pueden producir eliminación de sangre y otros componentes tisulares que se pueden detectar en las heces mucho antes de aparecer síntomas clínicos. Esto ha llevado a la búsqueda de análisis de materias fecales que permitan una detección temprana de cáncer y pesquisa de cáncer colorrectal en individuos asintomáticos. El método más común ha sido la detección de sangre oculta en heces. Varios estudios aleatorizados han demostrado que esto reduce la mortalidad de cáncer colorrectal en 15–33% en las cohortes y en 45% en los individuos que adhieren a las indicaciones, dependiendo del tipo de frotis y frecuencia de las pruebas.
Pruebas de sangre oculta: La prueba de frotis de guayaco es la prueba más común para detectar la presencia de sangre oculta en materias fecales. La prueba de guayaco reacciona con la actividad de peroxidasa del hem, pero esto hace que la prueba pueda tener reacción positiva con otras peroxidasas en las heces, tales como las presentes en ciertos frutos, hortalizas, y carnes rojas. Por lo tanto, hay que hacer restricciones en la dieta para evitar los resultados falso-positivos.
La prueba de sangre oculta en heces (FOBT) presenta varios problemas como prueba de pesquisa para cáncer colorrectal. La sensibilidad de la prueba es tan solo de 50–60% cuando se lo utiliza una vez, pero puede ascender a 90% cuando se la utiliza cada 1–2 años en un período de tiempo prolongado (sensibilidad programática). Si bien la sensibilidad puede estar aumentada durante la rehidratación, esto lleva a una variabilidad en la reacción que invalida el método como procedimiento de pesquisa. La baja sensibilidad lleva a un número alto de resultados falso-negativos y el efecto de una falsa tranquilidad. La mayoría de los casos identificados por pruebas de sangre fecal oculta son falso-positivos, y estos pacientes serán sometidos a investigaciones adicionales innecesarias, habitualmente colonoscopía. Otro problema del uso de FOBT para el tamizaje es que su efectividad requiere adherencia con las pruebas durante muchos años.
Las pruebas de sangre fecal oculta utilizando un frotis de guayaco actualmente están siendo reemplazadas en muchos países por las pruebas de inmunoquímica fecal (FIT o IFOBT), que detectan hemoglobina utilizando técnicas sensibles y específicas. Dichas pruebas obvian la necesidad de restricciones dietéticas. La simplicidad de las pruebas para el paciente varía; algunas son más sencillas y tienen muy buena adherencia. El punto de corte óptimo para la sensibilidad en las pruebas inmunoquímicas aun no ha sido validado.
Pruebas de ADN fecal para cáncer colorrectal. Se ha sugerido que la identificación de ADN anormal en muestras de heces puede dar un método posible para una detección temprana de cáncer colorrectal. Sin embargo, todavía están por determinarse los marcadores moleculares óptimos, y no se conoce aun la factibilidad de dichas pruebas aplicadas a la población general. Un estudio comparó un panel con 21 mutaciones contra sangre oculta fecal determinada por la prueba de frotis de guayaco estándar en 2507 sujetos. La sensibilidad del panel de ADN para cáncer colorrectal fue 52%, en comparación con 13% con la prueba de frotis de guayaco, y la especificidad fue similar (94.4% vs. 95.2%). Los resultados para la prueba de guayaco fueron extremadamente bajos.
Se han realizado varios estudios pequeños adicionales, dando una sensibilidad agregada de 65% y una especificidad de 95%. Una versión nueva con menos mutaciones ha llevado a la sensibilidad a más de 80%.
5. Pruebas de tamizaje y evidencias, 2: Endoscopía y colonografía TC
Esta sección describe los procedimientos endoscópicos y radiográficos usados como pesquisa para cáncer colorrectal y la evidencia que respalda su uso.
5.1 Procedimientos de tamizaje endoscópico
La sigmoidoscopía flexible permite el examen directo de la superficie interior del intestino grueso hasta una instancia de alrededor de 60 cm del margen anal. Esta técnica puede detectar los pólipos y cánceres colorrectales y también es utilizada para extraer pólipos o tomar muestras para examen histológico. Las ventajas de la sigmoidoscopía flexible son que el procedimiento puede ser realizado por examinadores médicos y no médicos; lleva menos tiempo que la colonoscopía; la preparación intestinal también es más fácil y rápida; la morbilidad es despreciable en los exámenes que no requieren polipectomía; y no se requiere sedación. Sin embargo, su desventaja obvia es que el examen del colon izquierdo solo hace perder las lesiones del lado derecho. Mientras que la especificidad de los hallazgos con procedimiento endoscópico es muy alta (98–100%, pocos falsos positivos), la sensibilidad es baja para el colon entero y varía de 35% a 70% debido a un número significativo de adenomas del lado derecho que aparecen en ausencia de tumores distales y que por lo tanto se pasan por alto con la sigmoidoscopía flexible.
La sigmoidoscopía está siendo utilizada para pesquisa en individuos asintomáticos para la detección del cáncer temprano y su prevención. Los estudios de control de casos han demostrado claramente que la sigmoidoscopía de pesquisa disminuye la mortalidad por cáncer de colon en 60–70% en el área examinada. Aparecen complicaciones mayores en 1 por 10.000 casos.
La colonoscopía permite la detección y extracción de pólipos y la biopsia de cáncer en todo el colon. La especificidad y la sensibilidad de la colonoscopía para detectar pólipos y cáncer son altos (por lo menos 95% de los pólipos grandes; ver abajo). Según los estudios de colonoscopías back-to-back, la frecuencia con la que no se diagnostican los pólipos es 15–25% para los adenomas menores de 5 mm de diámetro y 0–6% para los adenomas de 10 mm o más.
No hay estudios prospectivos aleatorizados que hayan examinado el impacto de la colonoscopía sobre la incidencia o la mortalidad. Sin embargo, el seguimiento a largo plazo de los pacientes post polipectomía en el Estudio Nacional de Pólipos de Estados Unidos demostró una reducción de aproximadamente 90% de la incidencia y mortalidad del cáncer colorrectal, utilizando modelos matemáticos.
Idealmente, un procedimiento de pesquisa debería ser una prueba simple y barata que pudiera aplicarse fácilmente a toda la población en riesgo. Si bien estos criterios no se cumplen en la colonoscopía, este abordaje es el “patrón oro”, y los pacientes con resultados positivo en cualquier otra prueba de pesquisa (FOBT, sigmoidoscopía, colonografía con tomografía computada) deberían ser derivados posteriormente para colonoscopía en caso de disponerse de ese recurso. En algunos países en los que se dispone de los recursos, la colonoscopía directa se ha convertido en el procedimiento más prevalente para el tamizaje de CCR. Las complicaciones mayores aparecen en 1–2 por 1000 casos.
5.2 Procedimientos de pesquisa radiográfica
Enema de bario con doble contraste. Si bien el enema baritado con doble contraste (DCBE) permite la evaluación de todo el colon, su sensibilidad y especificidad son inferiores a las de la colonoscopía y la colonografía por tomografía computada. Inclusive para los pólipos de gran tamaño y los cánceres, la DCBE ofrece una sensibilidad sustancialmente menor (48%) que la colonoscopía, y DCBE tiene más probabilidades de dar falsos positivos que la colonoscopía (artefactos diagnosticados como pólipos). Los pacientes con un enema baritado anormal deben hacerse una colonoscopía ulteriormente. Sin embargo, la DCBE está ampliamente disponible, y el hecho que puede detectar hasta 50% de los pólipos de gran tamaño avalaría el uso de este procedimiento en pacientes en ausencia de otros recursos.
Colonografía por tomografía computada (CTC). El barrido de tomografía computada helicoidal de sección fina del abdomen y pelvis, seguido de un procesamiento digital y de la interpretación de imágenes, puede mostrar reconstrucciones bidimensionales y tridimensionales de la luz del colon (“colonoscopía virtual”). El procedimiento requiere insuflación con aire para distender el colon al máximo de su tolerancia (aproximadamente 2 L de aire ambiente o dióxido de carbono) y preparación catártica del intestino. Mediante la ingesta de contraste oral se puede marcar el material fecal y el líquido, y luego puede restarse digitalmente de la imagen en la computadora.
Un meta análisis de estudios utilizando CTC para la detección de pólipos colorrectales y cáncer mostró una alta sensibilidad (93%) y alta especificidad (97%) para pólipos de 10 mm o mayores. Sin embargo, para pólipos combinados de tamaño grande y mediano (6 mm o mayores), la sensibilidad promedio disminuyó a 86%, con una especificidad de 86%.al incluir los pólipos de todos los tamaños, los estudios tenían una sensibilidad (entre 45-97%) y especificidad (entre 26–97%) demasiado heterogéneas. Si bien la sensibilidad de CTC para cáncer y pólipos grandes es satisfactoria, la detección de los pólipos en el rango de tamaño de 6–9 mm no es satisfactoria. Una desventaja importante de la CTC para el estudio de pacientes con mayor riesgo es que no se detectan las lesiones planas.
Una desventaja importante de CTC para su uso como procedimiento de pesquisa es la exposición repetida de los pacientes a radiación ionizante. Recientemente, la tecnología TC de multicorte o multidetección ha abreviado el tiempo de barrido y reducido la dosis de radiación, al tiempo que mantiene una alta resolución espacial. La colonografía de resonancia magnética está siendo estudiada en Europa por esta razón.
Además, el tema de cuándo derivar pacientes para colonoscopía sigue sin resolverse en base al tamaño del pólipo visualizado en la CTC. Esto incide enormemente en el costo del tamizaje. Otra desventaja es que el examen requiere una preparación completa de intestino. Si los pacientes necesitan colonoscopía tienen que ser sometidos a una segunda preparación del intestino a no ser que existan instalaciones para hacer ambos el mismo día. Finalmente, los hallazgos extra intestinales pueden llevar a una evaluación adicional radiológica y quirúrgica y aumentan los costos. Las complicaciones importantes son raras.
6. Costo-efectividad del tamizaje del CCR
Todas las opciones estándar para el tamizaje de CCR en individuos de riesgo promedio tienen buena relación costo/beneficio. Son tan costo/eficaces como la mamografía y más que otras formas de pesquisa médica (por ejemplo, para colesterol en hipertensión). La colonoscopía de pesquisa sistemática en parientes de primer grado de pacientes con CCR que comienzan a la edad de 40, demuestra un beneficio económico. En comparación con quimioterapia intensiva con múltiples drogas para cáncer avanzado, el tamizaje ahorra costos.
7. Cascadas – herramientas para el tamizaje
7.1 Introducción
En esta sección se hace una revisión de las diferentes opciones de pesquisa para los hombres y mujeres de 50 años y más con riesgo promedio y alto. Las opciones tienen en cuenta la disponibilidad de la colonoscopía, de la sigmoidoscopía flexible, FOBT, y enema baritado. Cuando los recursos de pesquisa están extremadamente limitados, la opción más realista sería los exámenes de sangre oculta fecal todos los años o cada dos años para los hombres y mujeres de riesgo promedio comenzando a los 50 años de edad.
El tipo de prueba en portaobjetos utilizado depende de los recursos de pesquisa y los hábitos dietéticos de la población.
La positividad inferior del test con Hemoccult II resulta menos gravoso para los recursos de colonoscopía que las pruebas más sensibles de frotis como el Hemoccult SENSA. Las pruebas inmunoquímicas son óptimas, ya que requieren solo dos días y no tres de análisis y no exigen restricciones dietéticas, pero son más costosas, lo que es un tema a considerar cuando los recursos financieros son bajos.
La evaluación diagnóstica puede hacerse ya sea por colonoscopía, si está disponible, o por enema baritado si la colonoscopía no está disponible fácilmente. Por lo tanto, la decisión de identificar por separado a los individuos que tengan un aumento del riesgo depende de los recursos colonoscópicos disponibles. Si estos son muy limitados, los individuos que tienen un aumento de riesgo pueden ser tamizados junto con los individuos con riesgo promedio.
7.2 Cascada de pesquisa del CCR
La cascada de pesquisa del CCR consiste en un conjunto de recomendaciones. Las recomendaciones se aplican a los diferentes niveles de recursos, comenzando con el 1 (recursos más elevados) y finalizando con el 6 (recursos disponibles mínimos).
Nivel de cascada 1. Las siguientes recomendaciones se aplican a los países con nivel relativamente elevado de recursos (financieros, profesionales, instalaciones) donde la incidencia y la mortalidad del cáncer colorrectal sean elevados (datos IARC) y donde sea una preocupación importante en relación con otras prioridades de la salud pública.
Recomendaciones para tamizar individuos con riesgo promedio. Colonoscopía para los hombres y mujeres con riesgo promedio, comenzando a los 50 años de edad y cada 10 años en ausencia de factores que los colocaría en riesgo aumentado.
Recomendaciones para tamizaje de individuos con riesgo aumentado:
— Individuos con antecedentes familiares de cáncer colorrectal o pólipos adenomatosos.
— A los individuos con un pariente de primer grado (padre, madre, hermano, o hijo) con cáncer de colon o pólipos adenomatosos diagnosticados antes de los 60 años de edad, o con dos parientes de primer grado a los que se les diagnosticó cáncer colorrectal a cualquier edad, debería recomendársele una colonoscopía de tamizaje que comience a los 40 años, o 10 años antes del diagnóstico más temprano en su familia, lo que ocurra primero, y que lo repita cada 5 años.
— Personas con un familiar de primer grado con CCR o pólipos adenomatosos diagnosticados a una edad de 60 ó más años o con 2 familiares de segundo grado con CCR, deben ser aconsejados de realizar tamizaje del mismo modo que una persona de riesgo medio, pero comenzando a los 40 años.
- — Las personas con un pariente de segundo grado (abuelos, tíos) o pariente de tercer grado (bisabuelo o primo) con cáncer colorrectal debería recomendársele hacerse un tamizaje como las personas de riesgo promedio.
- Poliposis adenomatosa familiar (FAP). A las personas que tienen un diagnóstico genético de poliposis adenomatosa familiar, o que están en riesgo de tener un FAP pero en quienes las pruebas genéticas no se han realizado o no son factibles, debería realizarse una sigmoidoscopía anual, comenzando a los 10–12 años de edad, para determinar si están expresando la anomalía genética. Deberían considerarse las pruebas genéticas en los pacientes con FAP que tengan parientes en riesgo. El asesoramiento genético debería orientar las pruebas genéticas y la consideración de colostomía.
- Cáncer colorrectal no polipósipo hereditario (HNPCC). Los individuos con un diagnóstico genético o clínico de cáncer colorrectal no polipósipo hereditario, o que tienen un aumento del riesgo de HNPCC, deberían hacerse una colonoscopía cada 1–2 años, comenzando a los 20–25 años de edad o 10 años antes de la edad más joven del diagnóstico de cáncer de colon en la familia, lo que ocurra primero. Debe ofrecerse pruebas genéticas para HNPCC a los parientes de primer grado de las personas con una mutación genética heredada de reparación mismatch (MMR). También habría que ofrecerla cuando la mutación familiar no se conoce todavía, pero se cumple uno de los primeros tres criterios de Bethesda modificado.
- Los individuos con antecedentes de enfermedad intestinal inflamatoria o antecedentes de pólipos adenomatosos o cáncer colorrectal son candidatos para vigilancia de seguimiento, más que pesquisa. Hay pautas publicadas para la vigilancia de estos individuos.
Nivel de cascada 2. Las recomendaciones son las mismas que para el nivel 1, pero se aplican cuando los recursos de colonoscopía son más limitados.
Recomendaciones para pesquisa de individuos con riesgo promedio. Colonoscopía para hombres y mujeres de riesgo promedio de 50 años una vez en la vida, en ausencia de factores que los colocarían en riesgo aumentado.
Recomendaciones para tamizaje de individuos con riesgo aumentado. Las recomendaciones para tamizaje de individuos con riesgo aumentado son las mismas que para la cascada 1.
Nivel de cascada 3. Las recomendaciones son las mismas que para el nivel 1, pero se aplican cuando los recursos de colonoscopía son más limitados y se dispone de sigmoidoscopio flexible.
Recomendaciones para tamizaje de individuos con riesgo promedio. Sigmoidoscopio flexible para hombres y mujeres de riesgo promedio, comenzando a la edad de 50, cada 5 años, en ausencia de factores que los colocarían en riesgo aumentado. Estudios diagnósticos con colonoscopía para los casos de sigmoidoscopía positiva.
Recomendaciones para tamizaje de individuos con riesgo aumentado. Las recomendaciones para tamizaje de individuos con riesgo aumentado son las mismas que para el nivel 1.
Nivel de cascada 4. Las recomendaciones son las mismas que para el nivel 3, pero se aplican cuando los recursos de sigmoidoscopía flexible y colonoscopía están más limitados.
Recomendaciones para tamizaje de individuos con riesgo promedio. La simgmoidoscopía flexible para hombres y mujeres de riesgo promedio una vez en la vida a los 50 años, en ausencia de factores que los colocarían en riesgo aumentado. Evaluación diagnóstica con colonoscopía para sigmoidoscopía positiva o neoplasia avanzada, dependiendo de los recursos de colonoscopía disponibles.
Recomendaciones para tamizaje de individuos con riesgo aumentado. Las recomendaciones para tamizaje de individuos con riesgo aumentado son las mismas que para el nivel 1.
Nivel de cascada 5. Las recomendaciones son las mismas que para el nivel de recursos 4, pero se aplican cuando la colonoscopía diagnóstica está severamente limitada.
Recomendaciones para tamizaje de individuos con riesgo promedio. Sigmoidoscopía flexible para los hombres y mujeres de riesgo promedio de 50 años una vez en la vida. Colonoscopía diagnóstica únicamente si se detecta neoplasia avanzada.
Recomendaciones para tamizaje de individuos con riesgo aumentado. Las recomendaciones para tamizaje de personas con riesgo aumentado dependen de los recursos colonoscópicos disponibles.
Nivel de cascada 6. Las recomendaciones son las mismas que para el nivel 1, pero se aplican cuando hay una severa limitación de los recursos de colonoscopía y sigmoidoscopía flexible.
Recomendaciones para tamizaje de individuos con riesgo promedio. Pruebas de sangre fecal todos los años para los hombres y mujeres de riesgo promedio comenzando a los 50 años de edad, en ausencia de factores que los colocarían en una categoría de riesgo aumentado. El tipo de prueba utilizado depende de los recursos de colonoscopía disponibles y los hábitos dietéticos de la población. La evaluación diagnóstica se pueden hacer ya sea con colonoscopía, si hubiera disponible, o enema baritado si no se dispone fácilmente de colonoscopía.
Recomendaciones para tamizaje de individuos con riesgo aumentado. La decisión de identificar por separado a estos individuos para un tamizaje especial (ver nivel 1) depende de los recursos de colonoscopía disponibles. Si no estuvieran disponibles, estos sujetos pueden ser tamizados junto con los individuos de riesgo promedio.
7. 3 Nuevas pruebas
Se dispone de CTC y pruebas de ADN sólo en unos pocos países de altos recursos, y generalmente no son aplicables a nivel mundial. Sin embargo, donde estuvieren disponibles, se los puede ofrecer a los hombres y mujeres de riesgo promedio, comenzando a los 50 años de edad, que no quieran ser estudiados utilizando otros métodos estándar, para aumentar el bajo número de individuos que se están estudiando actualmente en estos países.
7.4 Recomendaciones de acción — aplicación de un programa
Recomendaciones para acción — general:
- Desarrollar y difundir programas educativos estructurados para miembros del público, proveedores, sistemas de salud, y definidores de políticas/líderes políticos. Debe dirigirse programas educativos eficaces a cada uno de los participantes importantes de una manera aceptable.
- Desarrollar normas basadas en la evidencia para la calidad que abarque todo el proceso de tamizaje.
- Desarrollar y difundir sistemas de gestión clínica baratos y de sencillos.
- Promover el tamizaje a través de instancias nacionales y locales.
- Promover el tamizaje de cáncer colorrectal como parte de una atención clínica preventiva integral.
Recomendaciones — diseño de un programa
Planificación de un programa de tamizaje:
- Es preciso identificar una población objetivo — a saber, hombres y mujeres asintomáticos, edad, factores de riesgo (por ejemplo: familiares).
- La decisión de aplicar un programa de tamizaje del cáncer colorrectal debe basarse en la carga relativa del cáncer colorrectal en la población a investigar.
- La estrategia de tamizaje (prueba, intervalo, rango de edad) debe basarse en base a la evidencia médica (pautas), disponibilidad de recursos, nivel de riesgo, y aceptación cultural por parte de la población.
- El esencial contar con el apoyo de los profesionales influyentes, de los grupos de defensa de pacientes y de los medios de comunicación.
- Evaluar la factibilidad del programa propuesto. Ocuparse del desarrollo y la adjudicación de recursos (financieros, personales, instalaciones).
- Evaluar las necesidades específicas culturales y de idioma en la población.
Aplicación de un programa de tamizaje:
- Identificar la unidad objetivo a cargo de la aplicación, y asegurar la comunicación (entrenamiento y formación) con los prestadores de la salud (médicos generales y otros) y la población objetivo.
- Desarrollar y difundir guías sobre el tamizaje, diagnóstico, tratamiento, y vigilancia de una manera que sea sencilla para el paciente, y sensible desde un punto de vista cultural.
- Desarrollar métodos para el registro inicial de los pacientes, y su seguimiento.
Monitoreo del programa de tamizaje:
- Monitoreo cuidadoso y oportuno de las siguientes tasas: captación del tamizaje, repetición del tamizaje y seguimiento de las pruebas positivas.
- Cumplimiento con las recomendaciones de vigilancia.
- Debe instaurarse una medición de la calidad del programa, evaluándolo regularmente.
- Resultados, incluyendo las tasas de detección, distribución de los estadíos de cáncer, detección de adenomas, complicaciones, y finalmente, el efecto sobre la incidencia y mortalidad en la población.
8. Dónde obtener ayuda
8.1 The International Digestive Cancer Alliance (IDCA)
- http://omge.org/?idca
La misión de la International Digestive Cancer Alliance es promover la prevención y el manejo de los cánceres digestivos a nivel mundial mediante una alianza internacional de organizaciones que comparten la misma meta.
8.2 International Agency for Research on Cancer (IARC)
- http://www.iarc.fr/IARCPress/index.php
La IARC es parte de la Organización Mundial de la Salud. Se concentra en la investigación de la epidemiología, carcinogénesis ambiental y formación en investigación.
8.3 United States Centers for Disease Control and Prevention (CDC)
8.4 ACS American Cancer Society (ACS)
8.5 Union Internationale Contre le Cancer (International Union Against Cancer, UICC)
- http://www.uicc.org/
Como la mayor asociación mundial independiente de organizaciones no gubernamentales sin fines de lucro dedicadas a la lucha contra el cáncer, la UICC es un catalizador del diálogo responsable y la acción colectiva. La UICC reúne un amplio espectro de organizaciones, incluyendo las sociedades voluntarias contra el cáncer, los centros de investigación y tratamiento, las autoridades de salud pública, las redes de apoyo de pacientes, y los grupos de defensa de pacientes.
9. Datos útiles sobre sitios web, pautas y referencias seleccionadas
9.1 Pautas, declaraciones de consenso, sitios web
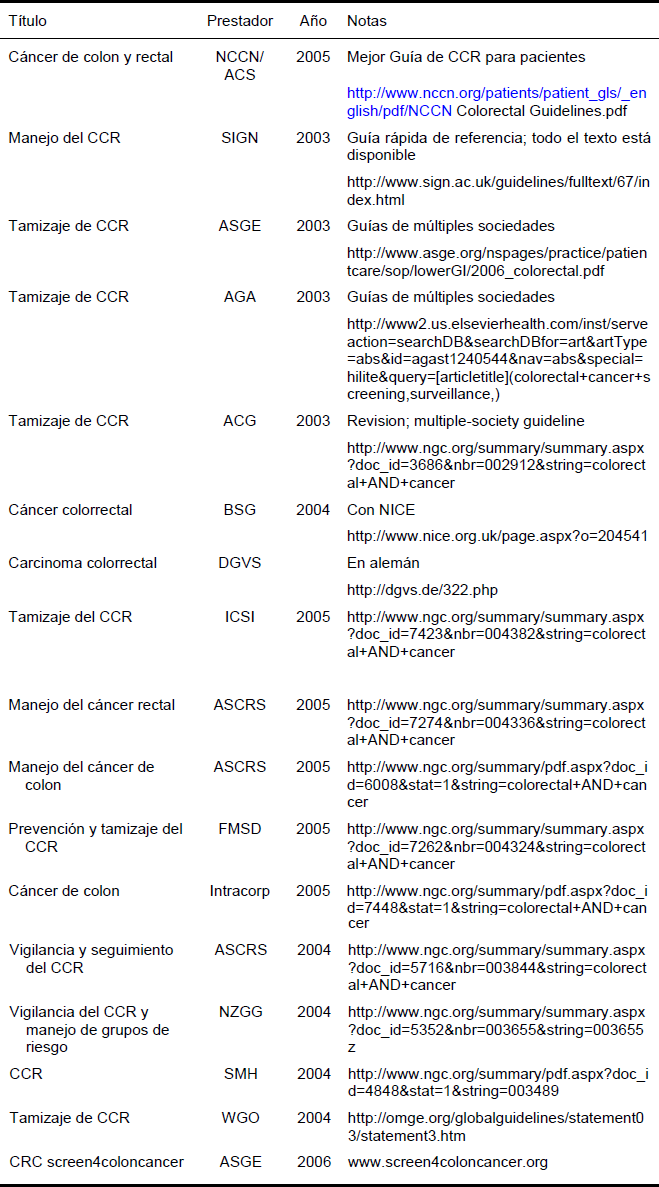
Abreviaturas: ACG, American College of Gastroenterology; ACS, American Cancer Society; AGA, American Gastroenterological Association; ASCRS, American Society of Colorectal Surgeons; ASGE, American Society of Gastrointestinal Endoscopy; BSG, British Society of Gastroenterology; DGVS, German Society for Digestive and Metabolic Diseases; FMSD, Finnish Medical Society Duodecim; ICSI, Institute for Clinical Systems Improvement; NCCN, National Comprehensive Cancer Network; NICE, National Institute of Clinical Excellence; NZGG, New Zealand Guidelines Group; SIGN, Scottish Intercollegiate Guidelines Network; SMH, Singapore Ministry of Health; WGO, World Gastroenterology Organisation.
9.2 Otras lecturas
- Lieberman DA, Weiss DG; Veterans Affairs Cooperative Study Group 380. One-time screening for colorectal cancer with combined fecal occult-blood testing and examination of the distal colon. N Engl J Med 2001;345:555–60 (PMID: 11529208).
- Barclay RL, Vicari JJ, Doughty AS, Johanson JF, Greenlaw RL. Colonoscopic withdrawal times and adenoma detection during screening colonoscopy. N Engl J Med 2006;355:2533–41 (PMID: 17167136).
- Sonnenberg A, Delcò F, Inadomi JM. Cost-effectiveness of colonoscopy in screening for colorectal cancer. Ann Intern Med 2000;133:573–84 (PMID: 11033584).
- Burt R, Neklason DW. Genetic testing for inherited colon cancer. Gastroenterology 2005;128:1696–1716 (PMID: 15887160).
- Faivre J, Dancourt V, Lejeune C, Tazi MA, Lamour J, Gerard D, et al. Reduction in colorectal cancer mortality by fecal occult blood screening in a French controlled study. Gastroenterology 2004;126):1674–80 (PMID: 15188160).
- Imperiale TF, Ransohoff DF, Itzkowitz SH, Turnbull BA, Ross ME. Fecal DNA versus fecal occult blood for colorectal-cancer screening in an average-risk population. N Engl J Med 2004;351:2704–14 (PMID: 15616205).
- Kronborg O, Jorgensen OD, Fenger C, Rasmussen M. Randomized study of biennial screening with a fecal occult blood test: results after nine screening rounds. Scand J Gastroenterol 2004;39:846–51 (PMID: 15513382).
- Parkin DM, Whelan SL, Ferlay J, et al., editors. Cancer incidence in five continents, vol. 8. Lyons: International Agency for Research on Cancer, 2002 (IARC Scientific Publications, no. 155) (PMID: 12812229).
- Winawer S, Fletcher R, Rex D, Bond J, Burt R, Ferrucci J, et al. Colorectal cancer screening and surveillance: clinical guidelines and rationale — update based on new evidence. Gastroenterology 2003;124:544–60 (PMID: 12557158).
- Winawer SJ, Zauber AG, Fletcher RH, Stillman JS, O’Brien MJ, Levin B, et al. Guidelines for colonoscopy surveillance after polypectomy: a consensus update by the US Multi-Society Task Force on Colorectal Cancer and the American Cancer Society. Gastroenterology 2006;130:1872–85 (PMID: 16697750).
- Young GP, St. John DJ, Winawer SJ, Rozen P; WHO (World Health Organization) and OMED (World Organization for Digestive Endoscopy). Choice of fecal occult blood tests for colorectal cancer screening: recommendations based on performance characteristics in population studies: a WHO (World Health Organization) and OMED (World Organization for Digestive Endoscopy) report. Am J Gastroenterol 2002;97:2499–507 (PMID: 12385430).
- Hewitson P, Glasziou P, Irwig L, Towler B, Watson E. Screening for colorectal cancer using the faecal occult blood test, Hemoccult. Cochrane Database Syst Rev 2007;(1):CD001216 (PMID: 17253456).
- Regula J, Rupinski M, Kraszewska E, Polkowski M, Pachlewski J, Orlowska J, et al. Colonoscopy in colorectal-cancer screening for detection of advanced neoplasia. N Engl J Med 2006;355:1863–72 (PMID: 17079760).
- Winawer SJ, Zauber AG, Ho MN, O’Brien MJ, Gottlieb LS, Sternberg SS, et al. Prevention of colorectal cancer by colonoscopic polypectomy. The National Polyp Study Workgroup. N Engl J Med 1993;329:1977–81 (PMID: 8247072).
- Winawer SJ, Stewart ET, Zauber AG, Bond JH, Ansel H, Waye JD, et al. A comparison of colonoscopy and double-contrast barium enema for surveillance after polypectomy. National Polyp Study Work Group. N Engl J Med 2000;342:1766–72 (PMID 10852998).
- Winawer SJ, Zauber AG, Gerdes H, O’Brien MJ, Gottlieb LS, Sternberg SS, et al. Risk of colorectal cancer in the families of patients with adenomatous polyps. National Polyp Study Workgroup. N Engl J Med 1996;334:82–7 (PMID: 8531963).
- Itzkowitz-Steven-H, Jandorf-Lina, Brand-Randall, Rabeneck-Linda, Schroy-Paul-C-3rd, Sontag-Stephen, Johnson-David, Skoletsky-Joel, Durkee-Kris, Markowitz-Sanford, Shuber- Anthony. Improved fecal DNA test for colorectal cancer screening. Clinical gastroenterology and hepatology Jan 2007 08 Dec 2006 , vol. 5, no. 1, p.111-7 PMID: 17161655
- Kim-David-H, Pickhardt-Perry-J, Taylor-Andrew-J, Leung-Winifred-K, Winter-Thomas-C, Hinshaw-J-Louis, Gopal-Deepak-V, Reichelderfer-Mark, Hsu-Richard-H, Pfau-Patrick-R. CT colonography versus colonoscopy for the detection of advanced neoplasia. N Engl J Med, 4 Oct 2007, vol. 357, no. 14, p. 1403-12, PMID: 17914041
- Allison JE, Sakoda LC, Levin TR, Tucker JP, Tekawa IS, Cuff T, Pauly MP, Shlager L, Palitz AM, Zhao WK, Schwartz JS, Ransohoff DF, Selby JV. Screening for colorectal neoplasms with new fecal occult blood tests: update on performance characteristics. J Natl Cancer Inst. 2007 Oct 3;99(19):1462-70. PMID: 17895475
Agradecimientos
Queremos expresar nuestro agradecimiento a la Agencia Internacional para la Investigación sobre el Cáncer (IARC; www.iarc.fr por los datos y las tablas, y a los Annals of Oncology (http://annonc.oxfordjournals.org/) por los datos de la Reunión de Oslo.
10. Preguntas y opiniones
El Comité de Guías Prácticas tiene interés en recibir comentarios y consultas de los lectores. ¿Le parece que algún aspecto ha sido descuidado? ¿Piensa que algunos procedimientos entrañan riesgos adicionales? Háganos conocer su experiencia. Presione el cursor en el enlace y exprese su opinión.
Escriba a: guidelines@worldgastroenterology.org








