L’Organisation mondiale de gastro-entérologie (OMG/WGO) a établi ce guideline sur la désinfection des endoscopes à l’intention des professionnels de la santé ainsi que du personnel qui s’occupe de l’utilisation, du nettoyage et de l’entretien des endoscopes. Elle cherche ainsi à soutenir les sociétés nationales, les instances officielles et les services d’endoscopie eux-mêmes en les aidant à l’élaboration de normes locales et de protocoles pour le retraitement des endoscopes.
Les guidelines de l’OMG sont le résultat d’un processus systématique de développement afin d’arriver à un consensus entre experts, processus basé sur la littérature médicale et scientifique, les directives cliniques existantes et les normes de bonne pratique régionales. Cette mise à jour traite les problèmes récents de l’apparition d’organismes multi résistants après endoscopie et propose des mesures afin de réduire le risque de survenue de tels foyers. Ces recommandations sont basées sur un consensus des membres d’un groupe de travail multidisciplinaire international d’experts en microbiologie, y compris les biofilms, le retraitement d’endoscopes, les soins infirmiers et la gastro-entérologie, et ayant une vaste expérience dans l’élaboration de guidelines nationaux et internationaux sur le retraitement.
1.1 Guidelines ou normes
La prestation de soins endoscopiques sûrs et efficaces repose sur le chevauchement de normes nationales et internationales, y compris sur celles qui règlent la conception et les effectifs des services, les appareils de retraitement automatiques des endoscopes flexibles, les désinfectants, la qualité de l’eau et les armoires de séchage.
La mise en œuvre de normes appropriées pour le retraitement devrait se baser sur les principes généraux de bonne pratique industrielle (good manufacturing practice (GMP)), représentées par un ensemble de règles, de codes et de guidelines pour un processus de production — dans le cas présent le retraitement d’un endoscope — afin d’effectuer une désinfection de haut niveau, tant sur le processus en soi que sur le contrôle de sa qualité. GMP est reconnu mondialement pour le contrôle et la gestion de la fabrication et les vérifications du contrôle de la qualité des produits pharmaceutiques et a évolué ces 60 dernières années afin de répondre aux problèmes multiples et très médiatisés rencontrés dans l’industrie pharmaceutique [1].
Les instructions pour le retraitement sont souvent décrites comme “guidelines,” mais elles sont plutôt des normes techniques qui énoncent la pratique minimale admissible pour le retraitement des endoscopes afin d’effectuer une désinfection de haut niveau. Les guidelines sur le plan medical se focalisent habituellement sur une question clinique particulière en utilisant des données sur une population — souvent les données venant des études randomisées — afin de guider le traitement d’un individu. Les études randomisées sont effectuées sur des populations spécifiques et c’est au clinicien lui-même de décider si ces guidelines s’appliquent à son patient [2].
L’application des normes est plus large et énumère les spécifications et les procédures permettant de s’assurer que les produits, les services et les systèmes sont sûrs et fiables et qu’ils fonctionnent conformément à ce qui était prévu. Les preuves à l’appui d’une norme se basent sur la science, la technologie et l’expérience en la matière. Il est rare que les études randomisées soient effectuées dans une population spécifique. Les normes pour le retraitement se basent sur la science et sont souvent validées par une mesure de l’efficacité dans un modèle comportant des terres artificielles ou un inoculum de bactéries connu. La dimension scientifique du nettoyage, de la désinfection, du séchage et l’aspect microbiologique constituent la base des normes pour le retraitement qui sont appropriés à tous les pays.
Les normes énumèrent la pratique minimale admissible.
Les termes “guidelines” et “normes” sont tous deux utilisés afin de décrire des instructions pour le retraitement des endoscopes [3,4].
1.2 Principes généraux du retraitement des endoscopes
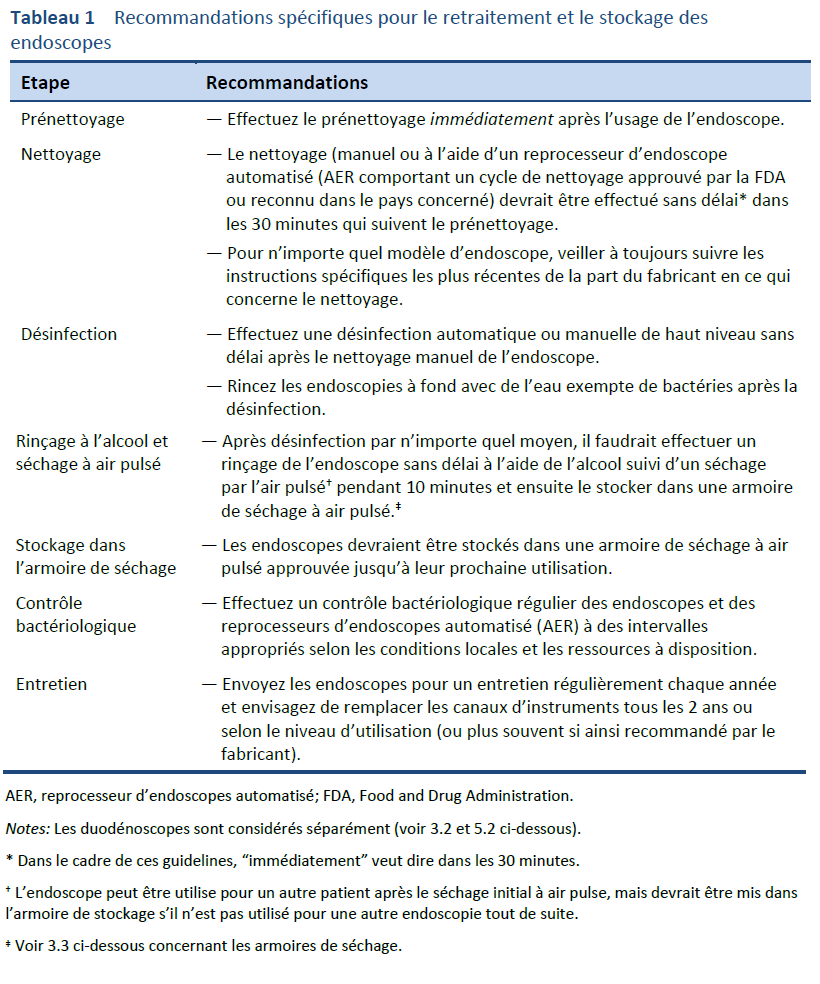
L’élément le plus important dans le retraitement des endoscopes consiste en un nettoyage manuel minutieux avant la désinfection. La désinfection échouera si le nettoyage a été inadéquat [5–7].
Le nettoyage manuel devrait être effectué par quelqu’un qui connaît bien la structure d’un endoscope et qui a reçu une formation dans la technique de son nettoyage. Le nettoyage devrait commencer immédiatement après l’utilisation de l’endoscope afin que les matières biologiques ne sèchent pas et se durcissent pas. Les détergents et les appareils de nettoyage appropriés devraient être utilises; en particulier des brosses d’un diamètre approprié devraient être utilisées afin de nettoyer chaque canal. Après nettoyage, un rinçage en profondeur devrait être effectué afin de s’assurer que tous les débris et les détergents sont éliminés avant la désinfection.
1.2.1 Nettoyage manuel
Pré nettoyage: immédiatement après chaque procédure, et pendant que l’endoscope est encore relié à la source lumineuse, essuyez le tube d’insertion avec un chiffon non-pelucheux à usage unique. Placez l’extrémité distale du tube dans une solution détergente peu moussante de qualité médicale et aspirez le détergent à travers tous les canaux, y compris le canal d’aspiration/biopsie. Rincer les canaux d’air et d’eau avec du détergent. Rincer tous les canaux, y compris l’éventuel canal de jet, avec de l’eau puis avec de l’air selon les instructions fournies par le fabricant. Utiliser une vanne spécifique si nécessaire afin de rincer les canaux à air et à eau avec du détergent.
Déconnectez l’endoscope de la source lumineuse amenez le dans la zone de nettoyage dans un récipient fermé qui permet d’éviter tout contamination de l’environnement par égouttage ou par fuite et qui est étiqueté d’une façon claire que l’endoscope s’y trouvant est contaminé.
Il est primordial que l’endoscope ne sèche pas avant le nettoyage ultérieur car ceci rendrait l’élimination des matières organiques difficile voire impossible. Les endoscopes devraient être traités sans tarder, dans les 30 minutes suivant l’examen.
Un test d’étanchéité devrait être effectué afin de contrôler l’intégrité de tous les canaux avant tout traitement supplémentaire. Enlevez toutes les valves et les boutons de l’endoscope et effectuez un test d’étanchéité selon les instructions fournies par le fabricant.
Brossez et nettoyez toutes les valves et tous les boutons, en accordant une attention particulière aux surfaces internes, et effectuez une désinfection/stérilisation de haut niveau selon les instructions fournies par le fabricant original de l’instrument.
Placez l’endoscope dans une solution détergente dans un évier dans la zone “sale” du local de décontamination et procédez à un lavage de la surface externe. Un détergent peu moussant de qualité médicale devrait être utilisé, à une dilution appropriée selon les instructions fournies par le fabricant. Brossez toutes les parties accessibles du canal d’aspiration-biopsie selon les instructions fournies par le fabricant. Brossez chaque canal jusqu’à ce que tous les débris aient été éliminés. Brossez l’extrémité et les poignées et nettoyez les sièges de soupape. Installez les adaptateurs de nettoyage et rincez les canaux avec du détergent propre pendant le temps nécessaire spécifique à l’appareil.
Rincez l’endoscope en laissant le détergent s’évacuer de l’évier, tout en rinçant sa surface externe à l’eau courante froide du robinet, puis en remplissant l’évier avec de l’eau du robinet et en purgeant les canaux avec de l’eau du robinet, en employant les adaptateurs de nettoyage selon les instructions fournies par le fabricant. Purgez les canaux avec de l’air afin d’éliminer l’eau de rinçage.
1.2.2 Désinfection
Une désinfection de haut niveau s’effectue à l’aide d’un reprocesseur d’endoscope automatisé (AER), qui devrait répondre aux normes nationales relevantes ou qui devrait être approuvé par le U.S. Food and Drug Administration (FDA). Il se peut que l’appareil comporte également un cycle de nettoyage automatique en plus du cycle de désinfection. Les connecteurs utilisés devraient être ceux qui sont propres à chaque modèle d’endoscope. Il est important de s’assurer que tous les canaux sont connectés au début et à la fin d’un cycle. Les composants détachables, comprenant notamment les vannes air/eau et celle de l’aspiration, peuvent être stérilisés à la vapeur ou bien être retraités avec l’endoscope au cas où cette fonction de nettoyage/désinfection des composants détachables est admise par le fabricant de l’AER.
Après une désinfection de haut niveau, l’endoscope subi un rinçage dans l’AER avec de l’eau stérile produite à l’aide d’un filtre spécial. Il est impératif de contrôler la qualité de l’eau régulièrement.
Une désinfection manuelle de haut niveau représente une autre option qui peut s’avérer efficace quand elle est effectuée par du personnel de retraitement dédié et bien formé, qui est muni d’un équipement de protection individuelle approprié. L’endoscope est immergé dans la solution désinfectante, en prenant bien soin de remplir tous les canaux. Les boutons et les vannes sont également immergés dans la solution désinfectante. Laissez tremper l’instrument pendant le temps nécessaire à la température requise et à la concentration nécessaire selon les instructions fournies par le fabricant de la solution désinfectante.
Purgez tous les canaux à l’aide de l’air et rincez l’extérieur de l’endoscope; rincez tous les canaux à l’aide de l’eau stérile avec le volume requis pour la solution désinfectante utilisée, afin d’éliminer tout trace de désinfectant.
1.2.3 Séchage
Les endoscopes devraient être séchés après chaque examen en éliminant l’eau restée dans les canaux à l’aide de l’air comprimé, puis en rinçant les canaux avec de l’alcool et en les séchant ensuite avec de l’air sous-pression. Le rinçage à l’alcool facilite le séchage et représente un complément utile à la désinfection en raison de ses effets bactéricides [8].
L’utilisation de l’alcool n’est pas admise dans certains pays (France, Royaume-Uni) en raison des craintes au sujet de la variante de la maladie de Creutzfeldt–Jakob (CJD).
L’endoscope devrait ensuite être stocké dans une armoire de séchage à air comprimé afin de renforcer le séchage.
Au cas où l’endoscope n’est pas souvent utilisé, on peut raisonnablement le stocker séparément en le suspendant verticalement dans une armoire conçue à cette fin, plutôt que dans une armoire de stockage/séchage à air comprimé, et ensuite procéder à un retraitement de l’endoscope avant le prochain usage. Il faut veiller à ce que les endoscopes soient tout à fait secs avant de les suspendre ainsi.
1.2.4 Accessoires
La bouteille d’eau devrait être remplacée et stérilisée à la vapeur après chaque séance d’endoscopie et la bouteille devrait être remplie d’eau stérile immédiatement avant sa prochaine utilisation.
1.2.5 Documentation
Toutes les étapes essentielles du processus de retraitement des endoscopes devraient être documentées afin de garantir sa qualité et afin de permettre la traçabilité de patients si nécessaire.
Lors de épidémies d’organismes multi résistants (MDRO) après endoscopie, les patients peuvent subir une colonisation bactérienne sans présenter des symptômes cliniques avec le développement d’infections systémiques sévère des semaines à des mois plus tard, avec un taux de mortalité pouvant aller jusqu’à 40% [36,52].
Très souvent, une espèce unique de bactéries porteuses de CPE est transmise à partir d’un seul endoscope à plusieurs reprises malgré un retraitement. La présence d’un biofilm sur l’endoscope, biofilm qui protège les bactéries lors du nettoyage et de la désinfection et qui agit comme un réservoir dans le cadre de la transmission de l’infection est l’origine la plus probable de cette épidémiologie.
5.1 Biofilm
En 1999 les « Centers for Disease Control and Prevention » (CDC) ont rapporté une épidémie de Pseudomonas aeruginosa produisant de la carbapénémase (CPE) après bronchoscopie et il a été considéré que la formation d’un biofilm dans les canaux de l’endoscope, étroits et difficiles à nettoyer, a bel et bien contribué à la survenue de l’épidémie [53]. Une investigation menée ultérieurement à des fins de recherche a examiné les surfaces des canaux endoscopiques à l’aide de la microscopie électronique à balayage et a permis de confirmer la formation d’un biofilm, souvent logé dans de petits défauts sur la surface des canaux [32]. D’autres études ont également permis d’identifier un biofilm dans les canaux de l’endoscope [54–56] et sur les endoscopes soupçonnés de défaut dans le cadre des épidémies [57–59].
Un biofilm est représenté par un groupement de bactéries qui se sont fixées sur une surface et reliées entre elles par une matrice extracellulaire de polysaccharides. Les bactéries qui se sont incorporées dans un biofilm ont souvent des caractéristiques autres que celles de bactéries flottantes libres (planctoniques) de la même espèce. Les bactéries se trouvant dans les biofilms sont résistantes aux désinfectants utilisés aux concentrations recommandées lors du retraitement [60]. Les bactéries porteuses de CPE planctoniques sont tuées en moins d’une minute avec les désinfectants standards, ce qui représente une grande marge de sécurité pour le retraitement de ces bactéries planctoniques [61]. Cependant la matrice du biofilm limite la diffusion du désinfectant et les multiples couches de cellules de la matrice du biofilm rendent la pénétration du désinfectant problématique [62]. Les concentrations standards de désinfectant ne sont pas en mesure de tuer le même type de bactérie de façon fiable dans les biofilms [63]. Les bactéries qui s’accumulent lors de la formation d’un biofilm sur les défauts de surface des canaux des endoscopes sont également protégées par des débris organiques et par des protéines réticulées, les rendant plus difficiles à tuer lors d’un retraitement standard [31,55]. Les paramètres actuels pour le retraitement sont basés sur les données venant de modèles utilisant des terres artificielles et les bactéries planctoniques plutôt que sur des modèles comportant des bactéries dans un biofilm or BBF.
Un biofilm agit comme une réservoir de bactéries attachées à la surface d’un canal endoscopique et sous certaines conditions favorables ces bactéries peuvent se multiplier, se détacher, reprendre leur état planctonique et se transmettre aux patients pendant l’endoscopie [31]. L’humidité et un apport de nutriments servent à faciliter la formation d’un biofilm avec libération de bactéries planctoniques.
Le rôle de l’humidité comme facteur facilitant la formation d’un biofilm pendant le stockage et l’importance d’un séchage complet après retraitement ont été sous-estimés dans le passé. Les données actuelles indiquent que 95% d’endoscopes montraient une humidité visible dans les canaux après un rinçage avec de l’alcool dans le reprocesseur automatisé (AER), un cycle de séchage de 3 minutes et le stockage pendant une nuit dans un cabinet standard [64]. Garder l’endoscope exempt d’humidité doit constituer une priorité — en particulier dans les canaux durant le stockage.
Un biofilm se forme facilement sur les défauts trouvés sur l’endoscope, très souvent les marques d’usure longitudinales sur les canaux à biopsie, et s’avère difficile voire impossible à enlever avec un retraitement standard [31,32,55,65]. Une étude multicentrique sur les endoscopes prêts à l’usage a trouvé des défauts dans tous les 45 endoscopes examinés [66]. Une inspection des canaux à l’aide d’un boroscope permet souvent d’identifier les défauts de surface occultes [66–68]. Les endoscopes devraient faire l’objet d’un entretien régulier afin d’identifier et de réparer les défauts macroscopiques ainsi qu’un remplacement des canaux de routine afin de réduire la prévalence de défauts occultes et de maintenir les surfaces des canaux lisses et nettoyables [6,37]. Une investigation menée par Verfallie et al. sur un duodénoscope soupçonné de défaut lors d’une épidémie a trouvé que les anneaux (O-rings) du duodénoscope représentaient un sujet préoccupant ; ceux-ci devraient être remplacés une fois par année ainsi que les canaux eux-mêmes [36]. Il est possible que sur d’autres endoscopes il soit nécessaire de remplacer les canaux moins souvent, par exemple tous le 1–2 an selon le volume du travail.
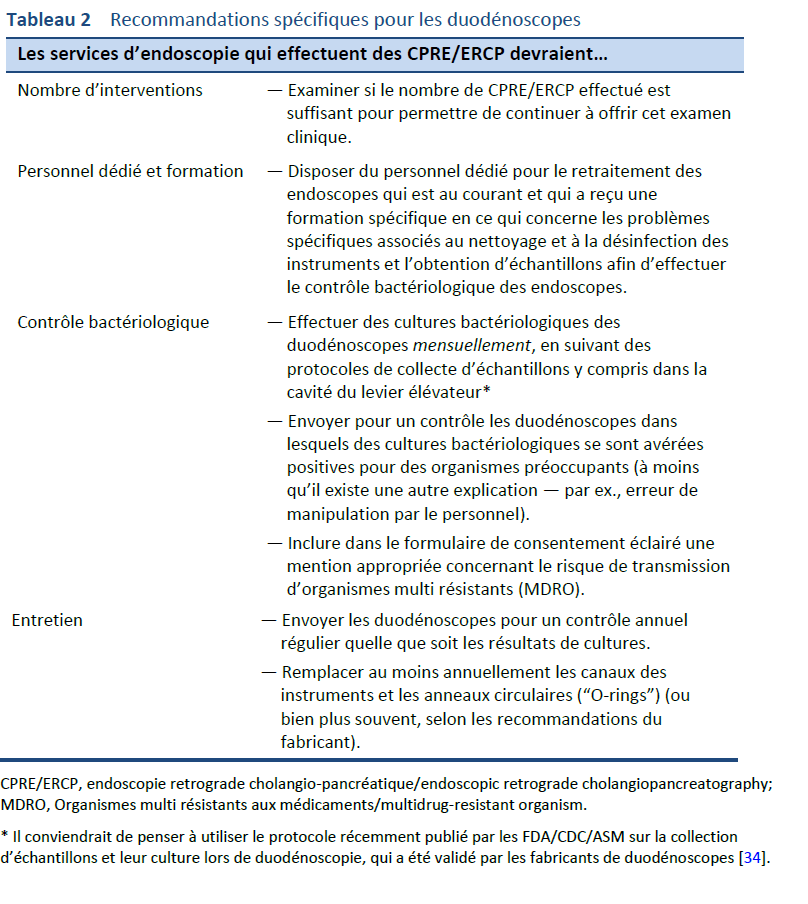
5.2 Duodénoscopes
Les duodénoscopes sont difficiles à nettoyer et à désinfecter. En plus de leur structure complexe, des facteurs tels les caractéristiques des patients qui devraient subir une ERCP et les interventions pratiquées contribuent au risque d’une colonisation et d’une infection ultérieure en raison des bactéries transmises pendant la procédure.
Le taux de contamination des duodénoscopes, à en juger par la présence de cultures de surveillance positives, est similaire aux taux de contamination trouvés dans les gastroscopes et dans les coloscopes [18–21]. On peut dire avec certitude que les caractéristiques des patients et les interventions pratiquées représentent les facteurs principaux dans l’incidence accrue d’épidémies après ERCP.
Les risques d’épidémies seraient mieux traités en effectuant les modifications spécifiques afin d’améliorer le nettoyage et la désinfection des duodénoscopes, ainsi que par des améliorations dans le retraitement de tous les types d’endoscope. Les mises à jour des protocoles de nettoyage par les fabricants représentent une amélioration importante dans le cadre du retraitement des duodénoscopes. Une revue de la base de données sur l’assurance qualité de 4307 cultures effectuées sur des duodénoscopes a révélé que l’application des nouveaux protocoles de nettoyage a permis de réduire de façon significative le taux de cultures positives [69].
5.3 Séchage
L’étape du séchage dans le retraitement a souvent été négligé ou effectué de manière incomplète et peut être sujet à l’erreur humaine [37]. Une enquête aux Etats-Unis sur le retraitement dans 249 services d’endoscopie effectuant des ERCP a trouvé que 52% des centres concernés n’ont pas respecté les guidelines des différentes sociétés professionnelles dans la matière et n’ont pas utilisé l’air pulsé pour le séchage des endoscopes [70]. Les guidelines eux-mêmes ne sont pas uniformes entre eux et ne précisent pas toujours les paramètres nécessaires afin de s’assurer d’un séchage adéquat [71]. Des études récentes ont trouvé du liquide résiduel jusque dans 95% des canaux des endoscopes après retraitement et séchage, ce qui suggère que les guidelines sur le séchage doivent être améliorés [55,64].
Les biofilms ont besoin d’humidité pour se développer. Dans une étude clé, Alfa et Sitter ont démontré que si les duodénoscopes restaient humides après le retraitement, les bactéries des espèces de Pseudomonas et d’Acinetobacter se sont rapidement développées [72]. Un séchage de 10 minutes à l’air pulsé a permis d’éviter une telle colonisation dans tous les endoscopes étudiés. L’application d’un rinçage à l’alcool suivi d’un séchage à air pulsé a permis d’éradiquer de telles épidémies d’infections à Pseudomonas après ERCP dans les années 1980s [73]. Les études plus récentes ont permis de confirmer qu’un rinçage à l’alcool suivi d’un séchage de 10 minutes à l’air pulsé était plus efficace qu’un rinçage à l’alcool suivi d’un temps de séchage à l’air pulsé plus court et de nature plus variable [66,74].
Les guidelines de l’Association des infirmières périopératoires (Association for periOperative Registered Nurses (AORN) recommandent que les endoscopes devraient être stockés dans une armoire à séchage et mentionnent que l’ensemble des preuves à disposition montrent qu’un stockage correct des endoscopes flexibles permet de faciliter le séchage, de diminuer toute contamination potentielle et d’offrir une protection contre les contaminants environnementaux (“The collective evidence shows that optimal storage of flexible endoscopes facilitates drying, decreases the potential for contamination, and provides protection from environmental contaminants.”)
Cette recommandation est confirmée par une revue des cultures de surveillance des endoscopes prêts à usage, y compris les duodénoscopes, les gastroscopes, les coloscopes et les écho endoscopes, qui a montré que l’introduction d’armoires de séchage a permis de réduire de façon significative le risque de contamination des endoscopes [75]. Lors d’une comparaison directe, une armoire de séchage à l’air pulse a permis de sécher les endoscopes de façon plus rapide et la croissance microbienne a été réduite de façon significative en comparaison avec une armoire de stockage standard [76].
5.4 Siméthicone
La simethicone est un polymère à base de silicone qui est utilisée lors d’endoscopie afin d’améliorer la visibilité. Des études randomisées ont permis de confirmer une diminution de la quantité de bulles ainsi qu’une visualisation améliorée lors de son utilisation. La siméthicone n’est cependant pas hydrosoluble et le fabricant Olympus a prévenu en 2009 que le produit était difficile à éliminer lors d’un retraitement standard [77]. Van Stiphout et al. ont rapporté en 2016 que si la siméthicone est ajoutée à l’eau injectée par le canal air/eau de l’endoscope, des dépôts de cristaux se formaient dans le connecteur et dans le canal lui-même [78]. Une étude plus récente a confirmé qu’à des différentes concentrations la simethicone qui sert au rinçage par le canal à air/eau formait un résidu qu’un retraitement standard n’a pas permis d’éliminer [79]. Il est possible que les résidus de la simethicone entravent le séchage des canaux et augmentent le risque qu’un biofilm se forme avec pour résultat que les microbes peuvent survivre à une désinfection et à une stérilisation de haut niveau. En juin 2018, le fabricant Olympus s’est prononcé contre l’utilisation de la simethicone et tout autre substance non hydrosoluble avec leurs appareils [80]. Il a été rapporté récemment que les fabricants Pentax et FujiFilm se sont prononcés également contre l’usage de la simethicone avec leurs endoscopes et les auteurs ont soulignés qu’il était capital de suivre les instructions des fabricants d’endoscopes [81].
5.5 Infections tropicales
Il n’existe que très peu de données sur le risque de transmission d’infections par des parasites lors d’une endoscopie gastro-intestinale. La plupart des agents parasitaires requièrent une progression dans un cycle de vie afin de devenir infectieux, ce qui prend du temps et ils ne sont ainsi pas tout de suite infectieux. La plupart des parasites infectieux potentiels ne survivront pas à un retraitement de l’endoscope.
De façon générale, il n’est pas admis qu’il y ait de risque pour les helminthes, les nématodes, les plathelminthes, l’Anisakis, ou les douves du foie tels Fasciola hepatica, mais une étude a cependant rapporté quatre cas d’œsophagite à Strongyloides en relation avec un gastroscope en particulier [82]. Des inquiétudes se sont manifestées cependant concernant le risque de transmission de Giardia lamblia, des espèces de Cryptosporidium et d’amibes.
5.6 Conclusion
La science du retraitement est en train d’évoluer. Les études nouvelles — comprenant la recherche de base, la recherche clinique et les études randomisées qui ont été entreprises en raison d’études dans la littérature faisant état d’épidémies de CPE — sont en train d’être publiées. Les fabricants d’endoscopes continuent à améliorer la conception des endoscopes et de valider de nouvelles instructions pour le retraitement de ceux-ci. Les techniques nouvelles quant au séchage et au nettoyage sont en train de faire leur apparition sur le marché. Les sociétés professionnelles sont en train de faire les mises à jour des guidelines concernant le retraitement pour répondre aux flux d’informations.
Ce guideline, ainsi que d’autres guidelines récents, recommande aux hôpitaux de nommer un comité pluridisciplinaire, représentant une diversité d’intérêts et d’expertise, afin d’évaluer les études nouvelles lors de leur publication et de développer, d’appliquer et — le plus important — de mettre à jour les guidelines pour le retraitement régulièrement selon leur pertinence quant aux ressources à disposition et à la composition de leur clientèle.
Un retraitement efficace est essential pour la sécurité des patients lors de l’endoscopie.
1. Patel KT, Chotai NP. Pharmaceutical GMP: past, present, and future—a review. Pharmazie. 2008;63(4):251–5.
2. Evidence-Based Medicine Working Group. Evidence-based medicine. A new approach to teaching the practice of medicine. JAMA. 1992;268(17):2420–5.
3. Society of Gastroenterology Nurses and Associates (SGNA). Standards and position statements [Internet] [Internet]. Chicago, IL: Society of Gastroenterology Nurses and Associates (SGNA); 2019 [cited 2018 Jan 18]. Available from: https://www.sgna.org/Practice/Standards-Practice-Guidelines
4. Association for periOperative Registered Nurses (AORN). Guidelines for perioperative practice [Internet]. Denver, CO: AORN, Inc.; 2019. Available from: https://www.aornbookstore.org/Product/Detail/MAN019
5. Gastroenterological Society of Australia (GESA). Infection control in endoscopy [Internet] [Internet]. Melbourne: Gastroenterological Society of Australia (GESA); 2010 [cited 2018 Jan 18]. Available from: http://www.gesa.org.au/resources/infection-control-in-endoscopy/
6. Kenters N, Huijskens E, Meier C, Voss A. Infectious diseases linked to cross-contamination of flexible endoscopes. Endosc Int Open. 2015;3(4):E259–65.
7. Alfa MJ. Current issues result in a paradigm shift in reprocessing medical and surgical instruments. Am J Infect Control. 2016 May;44(5):e41–5.
8. Kovacs BJ, Chen YK, Kettering JD, Aprecio RM, Roy I. High-level disinfection of gastrointestinal endoscopes: are current guidelines adequate? Am J Gastroenterol. 1999;94(6):1546–50.
9. Hayes, Inc. FDA Advisory Panel offers recommendations on procedures for reprocessing duodenoscopes [press release] [Internet]. Dallas, TX: Hayes, Inc.; 2015 [cited 2018 Feb 7]. Available from: https://www.hayesinc.com/hayes/resource-center/news-service/HNS-20150420-49/
10. U.S. Food and Drug Administration (FDA). Division of Industry and Consumer Education (DICE). Infections associated with reprocessed flexible bronchoscopes: FDA safety communication [Internet]. Silver Spring, MD: U.S. Food and Drug Administration (FDA); 2015 [cited 2018 Feb 9]. Available from: http://wayback.archive-it.org/7993/20170722213119/https://www.fda.gov/MedicalDevices/Safety/AlertsandNotices/ucm462949.htm
11. Naas T, Cuzon G, Babics A, Fortineau N, Boytchev I, Gayral F, et al. Endoscopy-associated transmission of carbapenem-resistant Klebsiella pneumoniae producing KPC-2 beta-lactamase. J Antimicrob Chemother. 2010;65(6):1305–6.
12. Bajolet O, Ciocan D, Vallet C, de Champs C, Vernet-Garnier V, Guillard T, et al. Gastroscopy-associated transmission of extended-spectrum beta-lactamase-producing Pseudomonas aeruginosa. J Hosp Infect. 2013 Apr;83(4):341–3.
13. Orsi GB, García-Fernández A, Giordano A, Venditti C, Bencardino A, Gianfreda R, et al. Risk factors and clinical significance of ertapenem-resistant Klebsiella pneumoniae in hospitalised patients. J Hosp Infect. 2011;78(1):54–8.
14. Koo VSW, O’Neill P, Elves A. Multidrug-resistant NDM-1 Klebsiella outbreak and infection control in endoscopic urology. BJU Int. 2012;110(11 Pt C):E922-926.
15. Tumbarello M, Spanu T, Sanguinetti M, Citton R, Montuori E, Leone F, et al. Bloodstream infections caused by extended-spectrum-beta-lactamase-producing Klebsiella pneumoniae: risk factors, molecular epidemiology, and clinical outcome. Antimicrob Agents Chemother. 2006;50(2):498–504.
16. Orsi GB, Bencardino A, Vena A, Carattoli A, Venditti C, Falcone M, et al. Patient risk factors for outer membrane permeability and KPC-producing carbapenem-resistant Klebsiella pneumoniae isolation: results of a double case-control study. Infection. 2013;41(1):61–7.
17. Voor In ’t Holt AF, Severin JA, Hagenaars MBH, de Goeij I, Gommers D, Vos MC. VIM-positive Pseudomonas aeruginosa in a large tertiary care hospital: matched case-control studies and a network analysis. Antimicrob Resist Infect Control. 2018;7:32.
18. Bisset L, Cossart YE, Selby W, West R, Catterson D, O’Hara K, et al. A prospective study of the efficacy of routine decontamination for gastrointestinal endoscopes and the risk factors for failure. Am J Infect Control. 2006;34(5):274–80.
19. Brandabur JJ, Leggett JE, Wang L, Bartles RL, Baxter L, Diaz GA, et al. Surveillance of guideline practices for duodenoscope and linear echoendoscope reprocessing in a large healthcare system. Gastrointest Endosc. 2016;84(3):392-399.e3.
20. Saliou P, Héry-Arnaud G, Le Bars H, Payan C, Narbonne V, Cholet F, et al. Evaluation of current cleaning and disinfection procedures of GI endoscopes. Gastrointest Endosc. 2016;84(6):1077.
21. Jones D. [Australia’s microbiological surveillance experience.]. In: U.S. Food and Drug Administration (FDA). Center for Devices and Radiological Health. Medical Devices Advisory Committee. Gastroenterology and Urology Devices Panel, editor. [Transcript of meeting held on May 14, 2015, Silver Spring, Maryland] [Internet]. Silver Spring, MD: U.S. Food and Drug Administration (FDA); 2015 [cited 2019 May 31]. p. 142–5. Available from: https://wayback.archive-it.org/7993/20170113091355/http://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/MedicalDevices/MedicalDevicesAdvisoryCommittee/Gastroenterology-UrologyDevicesPanel/UCM451164.pdf
22. Kelly CR, Kahn S, Kashyap P, Laine L, Rubin D, Atreja A, et al. Update on fecal microbiota transplantation 2015: indications, methodologies, mechanisms, and outlook. Gastroenterology. 2015;149(1):223–37.
23. Cammarota G, Ianiro G, Tilg H, Rajilić-Stojanović M, Kump P, Satokari R, et al. European consensus conference on faecal microbiota transplantation in clinical practice. Gut. 2017;66(4):569–80.
24. Rutala WA. ERCP scopes: a need to shift from disinfection to sterilization? In: U.S. Food and Drug Administration (FDA). Center for Devices and Radiological Health. Medical Devices Advisory Committee. Gastroenterology and Urology Devices Panel, editor. [Transcript of meeting held on May 15, 2015, Silver Spring, Maryland] [Internet]. Silver Spring, MD: U.S. Food and Drug Administration (FDA); 2015 [cited 2018 Mar 6]. p. 307–18. Available from: https://wayback.archive-it.org/7993/20170113091400/http://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/MedicalDevices/MedicalDevicesAdvisoryCommittee/Gastroenterology-UrologyDevicesPanel/UCM451165.pdf
25. U.S. Food and Drug Administration (FDA). Gastroenterology-Urology Devices Panel. 2015 materials of the Gastroenterology-Urology Devices Panel [Internet] [Internet]. Silver Spring, MD: U.S. Food and Drug Administration (FDA); 2015 [cited 2018 Feb 9]. Available from: https://wayback.archive-it.org/7993/20170112002249/http:/www.fda.gov/AdvisoryCommittees/CommitteesMeetingMaterials/MedicalDevices/MedicalDevicesAdvisoryCommittee/Gastroenterology-UrologyDevicesPanel/ucm445590.htm
26. Petersen BT, Cohen J, Hambrick RD, Buttar N, Greenwald DA, Buscaglia JM, et al. Multisociety guideline on reprocessing flexible GI endoscopes: 2016 update. Gastrointest Endosc. 2017;85(2):282-294.e1.
27. Snyder GM, Wright SB, Smithey A, Mizrahi M, Sheppard M, Hirsch EB, et al. Randomized comparison of 3 high-Level disinfection and sterilization procedures for duodenoscopes. Gastroenterology. 2017;153(4):1018–25.
28. U.S. Food and Drug Administration (FDA). Division of Industry and Consumer Education (DICE). Supplemental measures to enhance duodenoscope reprocessing: FDA safety communication [Internet]. Silver Spring, MD: U.S. Food and Drug Administration (FDA); 2015 [cited 2018 Feb 9]. Available from: http://wayback.archive-it.org/7993/20170722150658/https://www.fda.gov/MedicalDevices/Safety/AlertsandNotices/ucm454766.htm
29. Thaker AM, Kim S, Sedarat A, Watson RR, Muthusamy VR. Inspection of endoscope instrument channels after reprocessing using a prototype borescope. Gastrointest Endosc. 2018;88(4):612–9.
30. Bartles RL, Leggett JE, Hove S, Kashork CD, Wang L, Oethinger M, et al. A randomized trial of single versus double high-level disinfection of duodenoscopes and linear echoendoscopes using standard automated reprocessing. Gastrointest Endosc. 2018;88(2):306–313.e2.
31. Alfa MJ, Ribeiro MM, da Costa Luciano C, Franca R, Olson N, DeGagne P, et al. A novel polytetrafluoroethylene-channel model, which simulates low levels of culturable bacteria in buildup biofilm after repeated endoscope reprocessing. Gastrointest Endosc. 2017 Sep;86(3):442-451.e1.
32. Pajkos A, Vickery K, Cossart Y. Is biofilm accumulation on endoscope tubing a contributor to the failure of cleaning and decontamination? J Hosp Infect. 2004;58(3):224–9.
33. Roberts CG. The role of biofilms in reprocessing medical devices. Am J Infect Control. 2013;41(5 Suppl):S77-80.
34. U.S. Food and Drug Administration, Centers for Disease Control and Prevention (CDC), American Society for Microbiology (ASM). Duodenoscope surveillance. Sampling and culturing: reducing the risks of infection [Internet]. Silver Spring, MD: U.S. Food and Drug Administration (FDA); 2018 [cited 2018 Mar 7]. 58 p. Available from: https://www.fda.gov/downloads/medicaldevices/productsandmedicalprocedures/reprocessingofreusablemedicaldevices/ucm597949.pdf
35. Weingarten RA, Johnson RC, Conlan S, Ramsburg AM, Dekker JP, Lau AF, et al. Genomic analysis of hospital plumbing reveals diverse reservoir of bacterial plasmids conferring carbapenem resistance. mBio. 2018;9(1):e02011-17.
36. Verfaillie CJ, Bruno MJ, Voor in ’t Holt AF, Buijs JG, Poley J-W, Loeve AJ, et al. Withdrawal of a novel-design duodenoscope ends outbreak of a VIM-2-producing Pseudomonas aeruginosa. Endoscopy. 2015;47(6):493–502.
37. Jung M, Beilenhoff U. Hygiene: the looming Achilles heel in endoscopy. Visc Med. 2016;32(1):21–8.
38. Ling ML, Ching P, Widitaputra A, Stewart A, Sirijindadirat N, Thu LTA. APSIC guidelines for disinfection and sterilization of instruments in health care facilities. Antimicrob Resist Infect Control. 2018;7:25.
39. Murdani A, Kumar A, Chiu H-M, Goh K-L, Jang BI, Khor CJL, et al. WEO position statement on hygiene in digestive endoscopy: focus on endoscopy units in Asia and the Middle East. Dig Endosc. 2017;29(1):3–15.
40. Beilenhoff U, Neumann C, Rey J, Biering H, Blum R, Schmidt V. ESGE-ESGENA guideline for quality assurance in reprocessing: Microbiological surveillance testing in endoscopy. Endoscopy. 2007;39(02):175–81.
41. Chinese Society of Digestive Endoscopy. Consensus of experts on the safe operation of digestive endoscopy centers in China. J Dig Dis. 2016;17(12):790–9.
42. Roberts G, Roberts C, Jamieson A, Grimes C, Conn G, Bleichrodt R. Surgery and obstetric care are highly cost-effective interventions in a sub-Saharan African district hospital: a three-month single-institution study of surgical costs and outcomes. World J Surg. 2016;40(1):14–20.
43. Rennert-May E, Conly J, Leal J, Smith S, Manns B. Economic evaluations and their use in infection prevention and control: a narrative review. Antimicrob Resist Infect Control. 2018;7:31.
44. Bartsch SM, McKinnell JA, Mueller LE, Miller LG, Gohil SK, Huang SS, et al. Potential economic burden of carbapenem-resistant Enterobacteriaceae (CRE) in the United States. Clin Microbiol Infect. 2017;23(1):48.e9-48.e16.
45. Bardossy AC, Zervos J, Zervos M. Preventing hospital-acquired infections in low-income and middle-income countries. Infect Dis Clin North Am. 2016 Sep;30(3):805–18.
46. Association for the Advancement of Medical Instrumentation (AAMI). ANSI/AAMI ST91:2015 Comprehensive guide to flexible and semi-rigid endoscope processing in health care facilities [Internet]. Arlington, VA: Association for the Advancement of Medical Instrumentation; 2015. Available from: https://www.aami.org/productspublications/ProductDetail.aspx?ItemNumber=2477
47. Association for the Advancement of Medical Instrumentation (AAMI). Preventing device-related healthcare-associated infections: issues and outcomes from the September 2016 forum, Medical Technology and HAIs [Internet]. Arlington, VA: Association for the Advancement of Medical Instrumentation (AAMI); 2016 [cited 2018 Feb 7]. 19 p. Available from: https://s3.amazonaws.com/rdcms-aami/files/production/public/FileDownloads/Summits/161227_AAMI_HAI_Forum_Report.pdf
48. International Organization for Standardization (ISO). ISO 9000:2015(en). Quality management systems — fundamentals and vocabulary [Internet]. Geneva: International Organization for Standardization (ISO); 2015 [cited 2018 Jan 18]. Available from: https://www.iso.org/obp/ui/#iso:std:iso:9000:ed-4:v1:en
49. International Organization for Standardization (ISO). ISO 9001:2015. Quality management systems — requirements [Internet]. Geneva: International Organization for Standardization (ISO); 2015 [cited 2018 Jan 18]. Available from: https://www.iso.org/standard/62085.html
50. International Organization for Standardization (ISO). ISO 13485:2016. Medical devices — quality management systems — requirements for regulatory purposes [Internet]. Geneva: International Organization for Standardization (ISO); 2016 [cited 2018 Jan 18]. Available from: https://www.iso.org/standard/59752.html
51. Beilenhoff U, Biering H, Blum R, Brljak J, Cimbro M, Dumonceau J-M, et al. Prevention of multidrug-resistant infections from contaminated duodenoscopes: position statement of the European Society of Gastrointestinal Endoscopy (ESGE) and European Society of Gastroenterology Nurses and Associates (ESGENA). Endoscopy. 2017;49(11):1098–106.
52. Kallen AJ. CDC outbreak investigation. In: U.S. Food and Drug Administration (FDA). Center for Devices and Radiological Health. Medical Devices Advisory Committee. Gastroenterology and Urology Devices Panel, editor. [Transcript of meeting held on May 14, 2015, Silver Spring, Maryland] [Internet]. Silver Spring, MD: U.S. Food and Drug Administration (FDA); 2015 [cited 2018 Jun 3]. p. 199–210. Available from: https://wayback.archive-it.org/7993/20170113091355/http://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/MedicalDevices/MedicalDevicesAdvisoryCommittee/Gastroenterology-UrologyDevicesPanel/UCM451164.pdf
53. Centers for Disease Control and Prevention (CDC). Bronchoscopy-related infections and pseudoinfections—New York, 1996 and 1998. MMWR Morb Mortal Wkly Rep. 1999;48(26):557–60.
54. Wu R-P, Xi H-J, Qi K, Wang D, Nie X, Li Z-S. Correlation between the growth of bacterial biofilm in flexible endoscopes and endoscope reprocessing methods. Am J Infect Control. 2014;42(11):1203–6.
55. Hervé RC, Keevil CW. Persistent residual contamination in endoscope channels; a fluorescence epimicroscopy study. Endoscopy. 2016;48(7):609–16.
56. Herrmann IF, Heeg P, Matteja B, Strahl HM, Werner H-P, Boyce W, et al. Risques et dangers cachés de l’endoscopie, conduite à tenir. Acta Endosc. 2008;38(5):493–502.
57. Buss A, Been M, Borgers R, Stokroos I, Melchers W, Peters F, et al. Endoscope disinfection and its pitfalls — requirement for retrograde surveillance cultures. Endoscopy. 2008;40(04):327–32.
58. Kovaleva J, Meessen N, Peters F, Been M, Arends J, Borgers R, et al. Is bacteriologic surveillance in endoscope reprocessing stringent enough? Endoscopy. 2009;41(10):913–6.
59. Johani K, Hu H, Santos L, Schiller S, Deva AK, Whiteley G, et al. Determination of bacterial species present in biofilm contaminating the channels of clinical endoscopes. Infect Dis Health. 2018;23(4):189–96.
60. Otter JA, Vickery K, Walker JT, deLancey Pulcini E, Stoodley P, Goldenberg SD, et al. Surface-attached cells, biofilms and biocide susceptibility: implications for hospital cleaning and disinfection. J Hosp Infect. 2015;89(1):16–27.
61. Olson J. Medivators. In: U.S. Food and Drug Administration (FDA). Center for Devices and Radiological Health. Medical Devices Advisory Committee. Gastroenterology and Urology Devices Panel, editor. [Transcript of meeting held on May 14, 2015, Silver Spring, Maryland] [Internet]. Silver Spring, MD: U.S. Food and Drug Administration (FDA); 2015 [cited 2018 Jun 3]. p. 69–77. Available from: https://wayback.archive-it.org/7993/20170113091355/http://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/MedicalDevices/MedicalDevicesAdvisoryCommittee/Gastroenterology-UrologyDevicesPanel/UCM451164.pdf
62. Bridier A, Briandet R, Thomas V, Dubois-Brissonnet F. Resistance of bacterial biofilms to disinfectants: a review. Biofouling. 2011;27(9):1017–32.
63. Akinbobola AB, Sherry L, Mckay WG, Ramage G, Williams C. Tolerance of Pseudomonas aeruginosa in in-vitro biofilms to high-level peracetic acid disinfection. J Hosp Infect. 2017 Oct;97(2):162–8.
64. Ofstead CL, Wetzler HP, Johnson EA, Heymann OL, Maust TJ, Shaw MJ. Simethicone residue remains inside gastrointestinal endoscopes despite reprocessing. Am J Infect Control. 2016;44(11):1237–40.
65. da Costa Luciano C, Olson N, Tipple AFV, Alfa M. Evaluation of the ability of different detergents and disinfectants to remove and kill organisms in traditional biofilm. Am J Infect Control. 2016;44(11):e243–9.
66. Ofstead CL, Heymann OL, Quick MR, Eiland JE, Wetzler HP. Residual moisture and waterborne pathogens inside flexible endoscopes: Evidence from a multisite study of endoscope drying effectiveness. Am J Infect Control. 2018;46(6):689–96.
67. Ofstead CL, Doyle EM, Eiland JE, Amelang MR, Wetzler HP, England DM, et al. Practical toolkit for monitoring endoscope reprocessing effectiveness: identification of viable bacteria on gastroscopes, colonoscopes, and bronchoscopes. Am J Infect Control. 2016;44(7):815–9.
68. Ofstead CL, Wetzler HP, Eiland JE, Heymann OL, Held SB, Shaw MJ. Assessing residual contamination and damage inside flexible endoscopes over time. Am J Infect Control. 2016;44(12):1675–7.
69. Higa JT, Choe J, Tombs D, Gluck M, Ross AS. Optimizing duodenoscope reprocessing: rigorous assessment of a culture and quarantine protocol. Gastrointest Endosc. 2018;88(2):223–9.
70. Thaker AM, Muthusamy VR, Sedarat A, Watson RR, Kochman ML, Ross AS, et al. Duodenoscope reprocessing practice patterns in U.S. endoscopy centers: a survey study. Gastrointest Endosc. 2018;88(2):316-322.e2.
71. Kovaleva J. Endoscope drying and its pitfalls. J Hosp Infect. 2017;97(4):319–28.
72. Alfa MJ, Sitter DL. In-hospital evaluation of contamination of duodenoscopes: a quantitative assessment of the effect of drying. J Hosp Infect. 1991 Oct;19(2):89–98.
73. Petersen BT. Duodenoscope reprocessing: risk and options coming into view. Gastrointest Endosc. 2015;82(3):484–7.
74. Barakat MT, Huang RJ, Banerjee S. Comparison of automated and manual drying in the eliminating residual endoscope working channel fluid after reprocessing (with video). Gastrointest Endosc. 2018 Aug 24;
75. Saliou P, Le Bars H, Payan C, Narbonne V, Cholet F, Jézéquel J, et al. Measures to improve microbial quality surveillance of gastrointestinal endoscopes. Endoscopy. 2016;48(8):704–10.
76. Perumpail RB, Marya NB, McGinty BL, Muthusamy VR. Endoscope reprocessing: comparison of drying effectiveness and microbial levels with an automated drying and storage cabinet with forced filtered air and a standard storage cabinet [Epub ahead of print]. Am J Infect Control. 2019 Apr 6;
77. Catalone BJ, Olympus America Inc. Simethicone [letter to customers] [Internet]. 2009 Jun 9 [cited 2019 May 31]; Available from: https://medical.olympusamerica.com/sites/default/files/pdf/SimethiconeCustomerLetter.pdf
78. van Stiphout S, Laros I, van Wezel R, Gilissen L. Crystallization in the waterjet channel in colonoscopes due to simethicone. Endoscopy. 2016;48(S 01):E394–5.
79. Barakat MT, Huang RJ, Banerjee S. Simethicone is retained in endoscopes despite reprocessing: impact of its use on working channel fluid retention and adenosine triphosphate bioluminescence values (with video). Gastrointest Endosc. 2019;89(1):115–23.
80. ECRI Institute. Olympus—flexible endoscopes: manufacturer recommends against use of simethicone/non-water soluble additives — Alert [Internet]. Plymouth Meeting, PA: ECRI Institute; 2018 [cited 2019 Mar 1]. Available from: https://www.ecri.org/Components/Alerts/Pages/login.aspx?Page=AlertDisplay&AId=1635719
81. Visrodia K, Petersen BT. Borescope examination: Is there value in visual assessment of endoscope channels? Gastrointest Endosc. 2018;88(4):620–3.
82. Mandelstam P, Sugawa C, Silvis SE, Nebel OT, Rogers BH. Complications associated with esophagogastroduodenoscopy and with esophageal dilation. Gastrointest Endosc. 1976;23(1):16–9.