Варикозно расширенные вены пищевода представляют собой портосистемные коллатерали — т.е., сосудистые каналы, которые связывают портальный венозный и системный венозный кровоток. Они формируются как следствие портальной гипертензии (прогрессирующего осложнения цирроза), чаще всего в подслизистой оболочке нижних отделов пищевода. Разрывы и кровотечение из варикозно расширенных вен пищевода являются главными причинами осложнений портальной гипертензии и связаны с высокой частотой смертности. Кровотечение из варикозных вен является причиной 10–30% всех случаев кровотечения из верхних отделов желудочно-кишечного тракта.
1.1 Каскады ВГО – подход в зависимости от ресурсов
Стандартный подход применим в регионах и странах, где доступен полный диапазон диагностических исследований и вариантов медикаментозного лечения для ведения варикозного расширения вен пищевода. Тем не менее, в значительной части мира такие ресурсы не доступны. Диагностические и Лечебные Каскады ВГО предоставляют подход в зависимости от ресурсов.
Каскад: иерархический набор альтернативных диагностических, терапевтических вариантов и вариантов ведения риска и заболевания, распределенных в зависимости от доступных ресурсов.
1.2 Эпидемиология
Хотя варикоз вен может формироваться в любом месте желудочно-кишечного тракта, чаще всего он появляется на нескольких сантиметрах дистального отдела пищевода. Варикозно расширенные вены пищевода отмечаются приблизительно у 50% пациентов с циррозом. Варикоз вен желудка присутствует у 5–33% пациентов с портальной гипертензией.
Частота варикозного расширения вен пищевода варьирует в пределах от 30% до 70% пациентов с циррозом (Таблица 1), а у 9–36% пациентов имеется то, что называется варикозом «высокого риска». Варикоз вен пищевода развивается у пациентов с циррозом с ежегодной скоростью 5–8%, но узлы, достаточно крупные для возникновения кровотечения, отмечаются только в 1–2% случаев. Приблизительно у 4–30% пациентов небольшие узлы будут увеличиваться, что, следовательно, повышает риск развития кровотечения.
Таблица 1 Эпидемиология варикозного расширения вен пищевода и корреляция с заболеванием печени

Наличие расширенных гастроэзофагеальных вен коррелирует с тяжестью болезни печени. Тяжесть цирроза может быть рассчитана с использованием классификационной системы Чайлд-Пью (Child–Pugh) (Таблица 2).
Таблица 2 Классификация тяжести цирроза по Child-Pugh
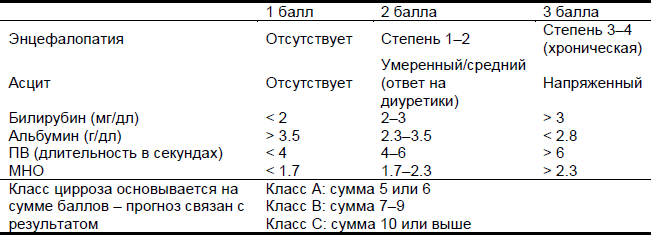
МНО, международное нормализованное отношение; ПВ, протромбиновое время.
1.3 Естественная история
У пациента с циррозом без варикозного расширения вен пищевода, портальная гипертензия еще не развилась, или портальное давление не достаточно велико для формирования варикоза. При увеличении портального давления у больного могут начать формироваться небольшие узлы. Со временем и возрастанием гипердинамической циркуляции, кровоток через варикозные вены увеличивается и, таким образом, повышается давление на стенку сосуда. Варикозное кровотечение в результате разрыва происходит тогда, когда возросшая сила превосходит максимальное напряжение стенки. Если нет изменений напряжения стенки, то существует высокий риск рецидива.
Таблица 3 – Прогноз у пациентов с варикозно расширенными венами пищевода

Рисунок 1 – Естественная история варикозного расширения вер и кровотечения у пациентов с циррозом2

ГПВД = градиент печеночного венозного давления; IGV = изолированные варикозные узлы, расположенные в дне желудка, в отсутствии пищеводных узлов; GOV2 = желудочно- пищеводные варикозно расширенные вены, распространяющиеся вдоль большой кривизны по направлению к дну желудка Факторы риска
Показатель Международного Нормализованного Отношения (МНО) > 1.5, диаметр портальной вены > 13 мм и тромбоцитопения были выявлены как прогностические факторы вероятности развития варикозно расширенных вен пищевода у пациентов с циррозом печени. Если не имеется ни одного, или имеются один, два или все три фактора, то < 10%, 20–50%, 40–60% и > 90% пациентов расцениваются как имеющие варикоз пищеводных вен, соответственно. Наличие одного или более факторов является показанием для проведения эндоскопии для исключения наличия варикозно расширенных вен и выполнения первичной профилактики кровотечения у пациентов с циррозом (Таблица 4).
Таблица 4 – Факторы риска развития варикозно расширенных вен пищевода и кровотечения
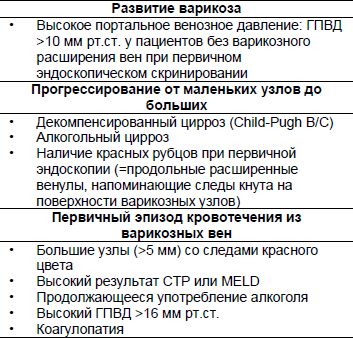
Эзофагогастродуоденоскопия – это золотой стандарт в диагностике варикозно расширенных вен пищевода. Если золотой стандарт недоступен, другим диагностическим методом может служить допплеровское ультразвуковое исследование кровотока (не эндоскопическое УЗИ). Хотя это и не лучший вариант выбора, он с определенностью может подтвердить наличие варикозно расширенных вен пищевода. Альтернативные методы включают рентгенографию/бариевый глоток пищевода и желудка, ангиографию портальной вены и манометрию.
Важно определить локализацию (пищевод или желудок) и размер узлов, признаки угрожающего, первого острого или рецидивирующего кровотечения, и (если это применимо) причину и тяжесть заболевания печени.
Таблица 5 – Практические рекомендации по диагностике варикозно расширенных вен пищевода
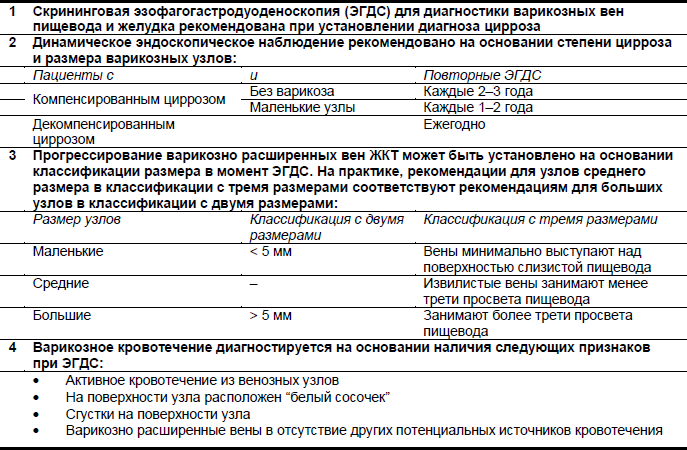
2.1 Дифференциальный диагноз варикозно расширенных вен пищевода/кровотечения
Дифференциальный диагноз для кровотечения из варикозно расширенных вен пищевода включает все этиологии кровотечений из (верхнего отдела) желудочно-кишечного тракта. У пациентов с циррозом также часто встречаются пептические язвы.
Таблица 6 – Дифференциальный диагноз для варикозно расширенных вен пищевода/кровотечения

Замечание: все эти состояния приводят к развитию варикозно расширенных вен пищевода как результата портальной гипертензии.
2.2 Пример из Африки — варикозно расширенные вены пищевода, вызванные шистосомиазом
Шистосомиаз – это наиболее частая причина варикозных вен пищевода в развивающихся странах — например, в Египте или Судане. В абсолютных цифрах эта причина может быть более частой, чем цирроз печени. В Судане имеются деревни, где более чем у 30% жителей выявляются варикозно расширенные вены пищевода. Функция печени у этих людей, тем не менее, хорошо сохранена. Они редко декомпенсируются и у них редко развивается гепатоцеллюлярная карцинома (ГЦК). Главной причиной смерти таких пациентов является кровотечение из варикозных вен пищевода. Если варикозные вены удаляются, эти пациенты могут выживать в течение более 25 лет.
2.3 Другие соображения
Таблица 7 – Соображения по диагнозу, профилактике и ведению варикозно расширенных вен пищевода и кровотечения из них

В ведении варикозно расширенных вен пищевода и кровотечения доступны следующие варианты (Таблицы 8 и 9). Хотя они и эффективны для остановки кровотечения, ни одна из этих мер, за исключением эндоскопической терапии, не оказывает влияния на показатель смертности.
Таблица 8 – Фармакологическая терапия

- Применение вазоактивных препаратов может быть безопасным и эффективным в тех случаях, когда эндоскопическая терапия не доступна в короткое время. Также оно связано с меньшим количеством отрицательных последствий по сравнению с экстренной склеротерапией.6
Таблица 9 – Эндоскопическая терапия

- Эндоскопическая склеротерапия и лигирование варикозных вен эффективны для остановки кровотечения у 90% пациентов. ЭВЛ более эффективно, чем эндоскопическая венозная склеротерапия (ЭВС), с большим контролем над кровотечением, уменьшенным повторным кровотечением и меньшим количеством побочных эффектов, но не отличающееся по показателю смертности.7, 8 Тем не менее, эндоскопическое лигирование труднее в исполнении, чем склеротерапия у пациентов с массивным активным кровотечением.
- Трансъюгулярное внутрипеченочное портосистемное шунтирование (TIPS) – это хорошая альтернатива при неэффективности эндоскопического лечения и фармакотерапии.
- Баллонная тампонада в настоящее время используется все реже, поскольку имеется риск повторного кровотечения после сдутия баллона и риск серьезных осложнений. Тем не менее, баллонная тампонада в большинстве случаев эффективна для, как минимум, временной остановки кровотечения, и может применяться в тех регионах мире, где невозможно быстрое проведение ЭГДС и TIPS. Она может способствовать стабилизации пациента на время, необходимое для подготовки к проведению позже ЭГДС и/или TIPS.
- Комбинированное эндоскопическое и фармакологическое лечение приводит к лучшему контролю над острым кровотечением, чем одно лишь эндоскопическое лечение.9
3.1 Клиническая практика
Подход к пациентам с циррозом и различными стадиями варикоза вен/кровотечения показан на следующих рисунках.
Рисунок 2 – Пациенты с циррозом, но без варикоза вен. ЭГДС, эзофагогастродуоденоскопия
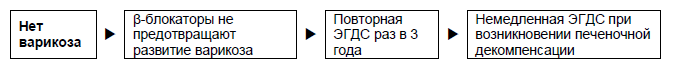
Рисунок 3 – Пациенты с циррозом и маленькими узлами, но без кровотечения.
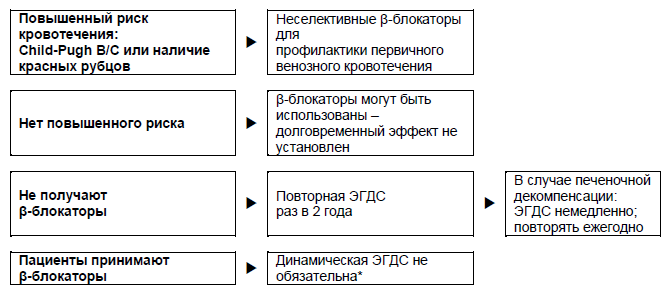
*Так как многие пациенты не отвечают на лечение β-блокаторами или профилактику кровотечения, рекомендуется проведение повторной ЭГДС через 2 года (также как и для неполучающих β-блокаторы).
Рисунок 4 – Пациенты с циррозом и средними или большими узлами, но без кровотечения. ЭВЛ, эндоскопическое венозное лигирование.

- Некардиоселективные β-блокаторы (пропранолол, надолол или карведилол) сначала назначаются в малых дозах, при необходимости доза увеличивается поэтапно до урежения частоты сердечных сокращений в покое на 25%, но не ниже 55 ударов в минуту.
- По сравнению с β-блокаторами, эндоскопическое венозное лигирование значительно уменьшает количество эпизодов кровотечения и тяжелых побочных явлений, но не оказывает влияния на показатель смертности.
Рисунок 5 – Пациенты с циррозом и острым кровотечением из варикозных вен.

ЭГДС, эзофагогастродуоденоскопия; ЭВЛ, эндоскопическое венозное лигирование; В/в, внутривенно; TIPS, трансъюгулярное внутрипеченочное портосистемное шунтирование.
Терлипрессин в настоящее время доступен в большинстве стран Европы, Индии, Австралии и ОАЭ, но не в США и Канаде.
- Острое кровотечение из варикозно расширенных вен пищевода часто связано с бактериальной инфекцией за счет кишечной дислокации и нарушений подвижности органа. Профилактическая антибиотикотерапия уменьшает бактериальную инфекцию, повторные кровотечения12, и увеличивает показатель выживаемости13.
- Интубация трахеи при остром или массивном кровотечении может помочь избежать аспирации крови в бронхи.
- У пациентов с кровотечением из варикозно расширенных вен дна желудка: предпочтительна эндоскопическая облитерация варикозных вен с использованием тканевых адгезивов (таких как цианоакрилат); второй выбор - ЭВЛ.
- TIPS необходимо рассматривать при неконтролируемом фундоварикозном кровотечении или его рецидиве несмотря на проводимую комбинированную эндоскопическую и фармакологическую терапию.
- При остром варикозном кровотечении при циррозе экстренная склеротерапия не более эффективна, чем фармакологическая терапия.
- Терлипрессин повышает эффективность контроля над кровотечением и смертностью,14 и должен служить препаратом первого выбора, когда он доступен. Там, где это средство не доступно, могут быть применены соматостатин, октреотид и вапреотид.
- Лечение пищеводного кровотечения аналогами соматостатина, вероятно, не уменьшает показатель смертности, но снижает необходимость переливания крови.
Рисунок 6 – Пациенты с циррозом, перенесшие острое варикозное кровотечение.
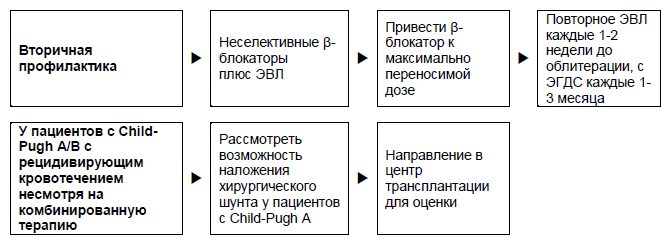
- Долговременный эндоскопический контроль и лигирование или склеротерапия рецидивирующих варикозных вен каждые 3–6 месяцев (во многих регионах развивающегося мира будет доступна только склеротерапия). Если эндоскопическое лигирование не доступно или противопоказано, назначаются некардиоселективные β-блокаторы (пропранолол, надолол или карведилол) сначала в малых дозах, при необходимости доза увеличивается поэтапно до урежения частоты сердечных сокращений в покое на 25%, но не ниже 55 ударов в минуту.
- У молодых пациентов с менее выраженным циррозом (Child–Pugh A), может рассматриваться добавление изосорбида 5-мононитрата (начиная с 2 × 20 мг в день с повышением до 2 × 40 мг в день), если не эффективны склеро- или фармакотерапия. Можно думать о проведении TIPS, особенно у кандидатов на трансплантацию. В особых случаях (пациенты с хорошо сохранившейся функцией печени, стабильным заболеванием печени), рассматривается вопрос о наложении портокавального шунта (Н- трансплантат) или дистального спленоренального шунта (шунт Уоррена).
- Портосистемные шунты связаны с более низким показателем повторных кровотечений из варикозно расширенных вен по сравнению со склеротерапией/лигированием, но они повышают частоту развития печеночной энцефалопатии15
- Всегда необходимо думать о трансплантации печени у пациентов с классами В или С по Child–Pugh.
Рекомендации для ведения первой линии пациентов с циррозом печени на каждой стадии естественного течения варикоза вен (Рис. 7)
Рисунок 7 – Рекомендации для ведения первой линии.
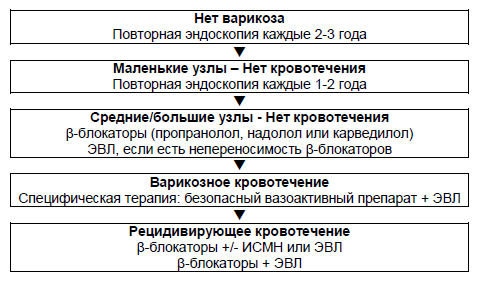
ЭВЛ, эндоскопическое венозное лигирование; ИСМН, изосорбид 5-мононитрат.
3.2 Каскад для лечения
Каскад – это иерархический набор диагностических и терапевтических техник для одного и того же заболевания, упорядоченный в зависимости от доступных ресурсов.
Как было указано выше, некоторые терапевтические варианты эффективны в большинстве клинических ситуаций, вовлекающих активное кровотечение из варикозно расширенных вен, а также для вторичной и первичной профилактики кровотечения. Оптимальная терапия в каждом индивидуальном случае сильно зависит от относительно легкой местной доступности этих методов и техник. Все это широко варьирует в различных регионах мира.
Если нет быстрого доступа к эндоскопии, необходимо применение фармакотерапии в любом случае подозрения на варикозное кровотечение — например, у пациентов с кровавой рвотой и признаками цирроза печени. Подобным образом фармакотерапия может использоваться для первичной профилактики у пациентов с циррозом и признаками портальной гипертензии (спленомегалия, тромбоцитопения) и/или нарушенной функцией печени, и для вторичной профилактики у пациентов с циррозом и кровотечением из верхних отделов ЖКТ в анамнезе.
Если фармакотерапия также не доступна, а имеется подозрение на варикозное кровотечение, необходимо обратиться к общим реанимационным мероприятиям и как можно быстрее переместить больного в медучреждение, где будут доступны необходимые диагностические/терапевтические возможности; в такой ситуации огромную помощь оказывает баллонная тампонада.
Рисунок 8 – Каскад для лечения острого кровотечения из варикозно расширенных вен пищевода.

В/в, внутривенная.
Замечание: Комбинация лигирования и склеротерапии обычно не используется, за исключением тех случаев, когда кровотечение слишком массивно для определения сосуда, который необходимо лигитровать. В таких случаях склеротерапия может быть выполнена для контроля над кровотечением и достаточной очистки области кровотечения для последующего лигирования.
Внимание: Существует множество состояний, которые могут привести к развитию варикозно расширенных вен пищевода. Также имеется много вариантов лечения, зависящих от доступных ресурсов. Как пример зависящего от ресурсов подхода к лечению в Африке, можно привести Fedail (2002).
3.3 Пример из Африки — варикозно расширенные вены пищевода и шистосомиаз
Table 10 – Лечение варикозно расширенных вен пищевода, вызванных шистосомиазом

Замечание: терапия вазоактивными препаратами нереалистична во многих развивающихся странах. В Судане, например, стоимость 1 мг терлипрессина (Глипрессина) эквивалентна 25% заработной платы семейного врача или, примерно, годовой зарплате государственного служащего.






















