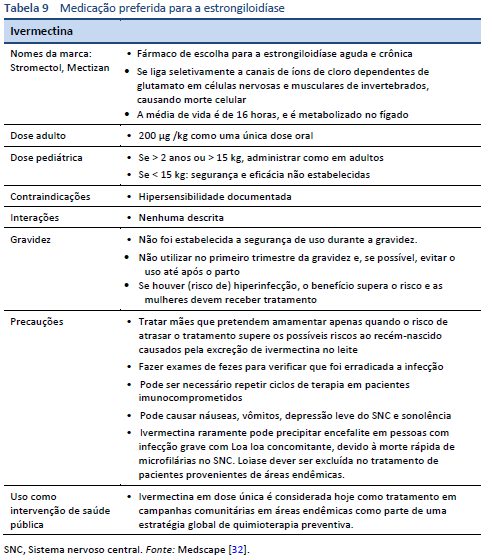
A estrongiloidíase é uma infecção pelo Strongyloides stercoralis (Fig. 1), um verme muito presente em áreas tropicais e subtropicais, mas também em países com climas temperados (Tabela 3).
- A estrongiloidíase humana é causada por duas espécies do nematoide parasitário Strongyloides, sendo S. stercoralis o patógeno mais frequente em humanos; S. fuelleborni pode ser encontrado esporadicamente na África e em Papua Nova Guiné.
- As larvas infectantes de S. stercoralis podem se reproduzir no intestino e autoinfectar diretamente a indivíduos positivos. A autoinfecção é o principal problema que diferencia a estrongiloidíase de outras infecções macroparasitárias do tipo helmintíase transmitidas pelo solo (HTS). As principais espécies que infectam os humanos são o nematoide (lombriga) (Ascaris lumbricoides), o tricocéfalo (Trichuris trichiura) e os ancilostomídeos (Necator americanus e Ancylostoma duodenale) [1].
- O verme adulto macho é encontrado somente no solo. Não é um parasita de tecidos e não se encontra no hospedeiro humano.
- O verme fêmea adulto é muito pequeno e quase transparente. Mede aproximadamente 2,2–2,5 mm em comprimento; tem um diâmetro de 50 µm e vive em túneis entre os enterócitos do intestino delgado humano.
- As larvas infectantes podem se reproduzir no solo contaminado e infectar as pessoas expostas.
A estrongiloidíase é diferente de todas as outras infecções helmínticas transmitidas pelo solo porque os ovos produto da partenogênese do verme fêmea fazem eclosão no intestino e produzem larvas rabditiformes.
- As larvas são geralmente eliminadas nas fezes, mas algumas podem amadurecer até a fase filarioide e reinfectar o hospedeiro penetrando na última parte do intestino ou na pele perianal (ciclo autoinfeccioso).
- Dependendo da resposta imune do hospedeiro, isto pode derivar em disseminação e hiperinfecção (Tabela 4).


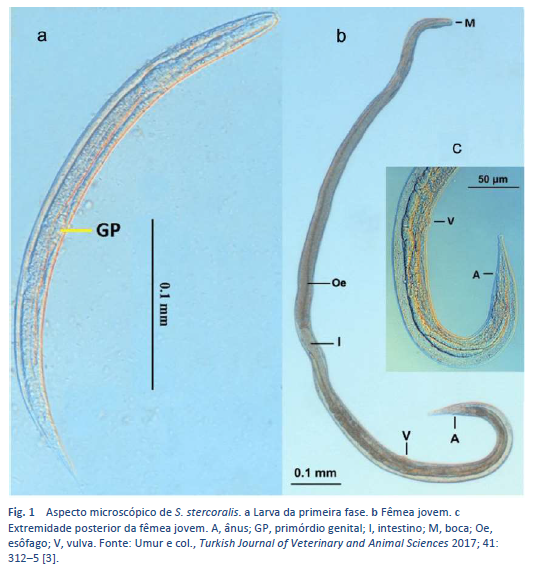
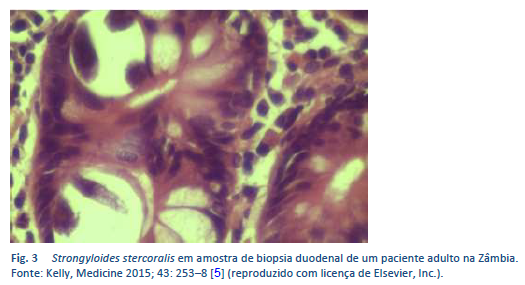
O ciclo de vida do parasita consta de duas fases importantes: a fase rabditiforme e a fase filarioide (Figs. 2, 3).

2.1 Helmintíase e estrongiloidíase transmitidas pelo solo
Apesar da estrongiloidíase ter uma via de infecção similar às outras helmintíases transmitidas pelo solo, precisa outras ferramentas de diagnóstico além da microscopia e requer tratamento diferente. Nas áreas nas quais foi aplicada a quimioterapia antihelmíntica preventiva com ivermectina para controlar a oncocercose ou a filariose linfática, houve uma redução perceptível da prevalência da estrongiloidíase [6–10]. O Comitê de Medicamentos Essenciais da OMS incluiu a ivermectina na sua lista para a estrongiloidíase, inclusive em combinação com albendazol. Aproximadamente 900 milhões de pessoas recebem agora esta combinação como parte das campanhas de doenças tropicais negligenciadas (NTD) [11].
2.2 Fisiopatologia
Strongyloides stercoralis tem um ciclo de vida único e complexo. A figura 4 descreve as vias singulares de sua replicação.
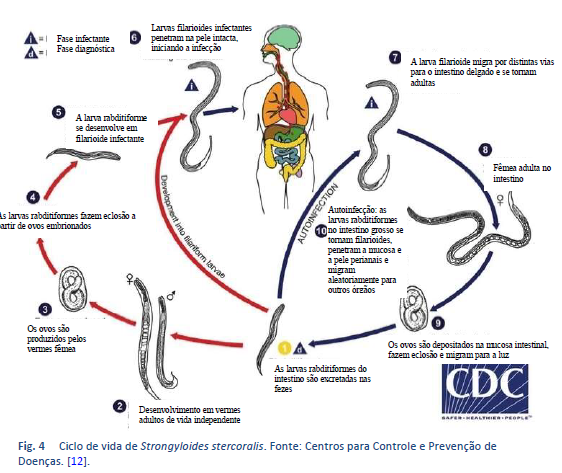
O ciclo de vida de Strongyloides é mais complexo que o da maioria dos nematoides por sua alternação entre ciclos de vida livre e formas parasitárias, e porque pode provocar autoinfecção e reprodução dentro do hospedeiro. Há dois tipos de ciclo:
- Ciclo de vida livre. As larvas rabditiformes excretadas com as fezes podem mudar duas vezes e se tornar larvas filarioides infectantes (desenvolvimento direto), ou mudar quatro vezes e se tornar machos e fêmeas adultos de vida livre que se acasalam e produzem ovos dos quais nascem larvas rabditiformes. Estas últimas, por sua vez, podem evoluir para uma nova geração de adultos de vida livre ou em larvas filarioides infectantes. As larvas filarioides penetram na pele do hospedeiro humano para iniciar o ciclo parasitário.
A fase de vida livre do ciclo de vida do nematoide está limitada a um máximo de uma geração [13]. Esta característica especial da estrongiloidíase tem implicações importantes tanto para o tratamento das pessoas infectadas como para o controle ambiental na prevenção da transmissão. Significa que é vital que a terapia de erradicação seja altamente eficaz para eliminar todas as formas viáveis do organismo do indivíduo infectado.
- Ciclo parasitário. As larvas filarioides presentes no solo contaminado penetram na pele humana e migram para os pulmões, onde penetram nas cavidades alveolares; são transportadas pela árvore brônquica até a faringe, são engolidas e chegam ao intestino delgado. No intestino delgado mudam duas vezes e se tornam vermes adultos fêmeas. As fêmeas vivem emaranhadas no epitélio do intestino delgado e produzem ovos por partenogênese que dão origem a larvas rabditiformes. As larvas rabditiformes podem ser eliminadas nas fezes (ver “ciclo de vida livre” acima) ou podem evoluir e causar autoinfecção. Na autoinfecção, as larvas rabditiformes se tornam larvas filarioides infectantes, que podem penetrar tanto a mucosa intestinal (autoinfecção interna) como a pele da área perianal (autoinfecção externa); em qualquer caso, as larvas filariformes podem seguir a via antes descrita, sendo levadas sucessivamente para os pulmões, árvore brônquica, faringe e intestino delgado, onde amadurecem em adultos; ou podem se disseminar pelo organismo todo. Até agora, a ocorrência de autoinfecção helmíntica em humanos apenas é reconhecida nas infecções por Strongyloides stercoralis e Capillaria philippinensis. S. stercoralis é muito mais frequente e difundido. Na estrongiloidíase, a autoinfecção explica a existência de infecções que persistem muitos anos em pessoas que não estiveram em área endêmica (o recorde atual é de 65 anos) e a morbidade e potencial letalidade da hiperinfecção em indivíduos imunocomprometidos, ambos excepcionais para infecções por nematoides.
2.3 Carga da doença e endemicidade
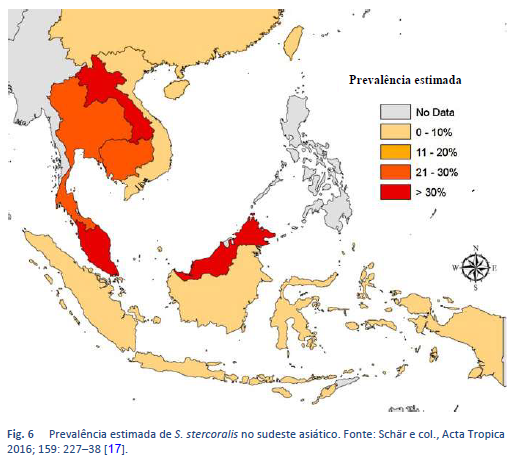
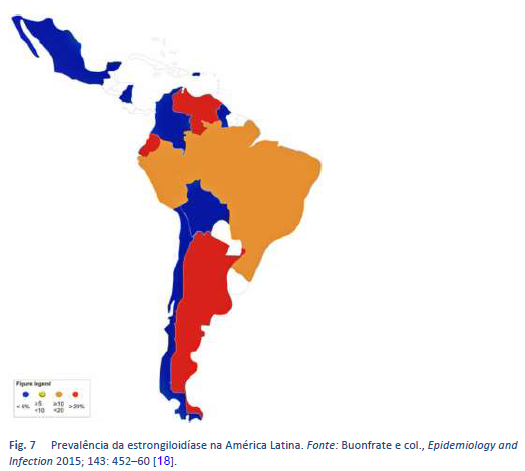
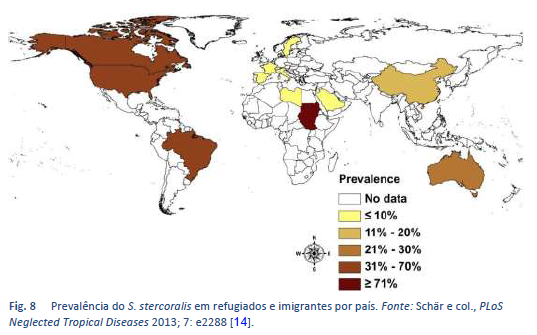
A estrongiloidíase é endêmica nas regiões tropicais e subtropicais (Figuras 5-8), e a prevalência provavelmente muito mais alta do que os 100 milhões de pessoas previamente citadas: foram publicadas estimativas mais altas, de até 370 milhões de pessoas [2]. A parasitose também está muito disseminada na Europa Oriental, e foram notificados focos espalhados da infecção em pessoas idosas na região mediterrânea.
Sabemos pouco sobre a prevalência da infecção, e menos sobre a carga clínica de sua morbidade. Se for realmente disseminada, o risco de hiperinfecção iatrogênica (paciente com tratamento imunossupressor) constitui um desafio. A estrongiloidíase poderia infetar até 40% da população em algumas zonas tropicais e subtropicais [14].
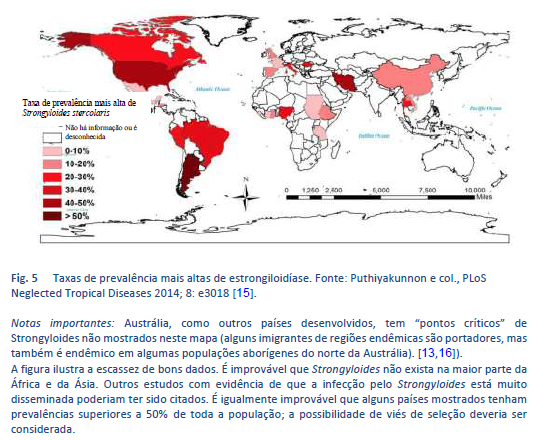
As infecções migratórias podem acontecer em qualquer país e representar um risco global potencial. A doença pode aparecer em qualquer consultório em qualquer lugar.
2.4 Fatores de risco e grupos especiais em risco de infecção
O maior fator de risco, em geral, é a desvantagem socioeconômica em um ambiente onde Strongyloides é endêmico.
- Pobreza, precariedade habitacional e saneamento deficiente; andar descalço, viver em ambiente com defecação a céu aberto
- Prisioneiros de guerra
- Condição de refugiado: refugiados de países nos quais a estrongiloidíase é endêmica
- Viajantes que vão para áreas endêmicas ou que retornam delas
- Estudos apontaram o sexo masculino, a idade avançada, a transmissão animal-humana e os climas úmidos e chuvosos nos trópicos e subtrópicos como fatores de risco [17]
2.5 Fatores de risco e grupos especiais em risco de infecção disseminada
- Medicamentos imunossupressores: especialmente corticosteroides, mas também tacrolimo e agentes quimioterápicos
- Pacientes com imunidade celular alterada
- Infecção pelo vírus linfotrópico humano tipo 1
- Neoplasias, particularmente neoplasias hematológicas (linfoma, leucemia)
- Transplante de órgãos (indivíduos transplantados com aloenxerto renal)
- Fatores de risco menores/possíveis: doença vascular do colágeno, má absorção e estados de desnutrição, doença renal terminal, diabetes mellitus, fatores locais do hospedeiro, alças cegas e divertículos (estrongiloidíase persistente em alça intestinal cega)
2.6 Estrongiloidíase e pacientes imunodeprimidos
A estrongiloidíase varia de forma assintomática a severa e pode causar síndrome de hiperinfecção e doença disseminada, associada a uma alta taxa de mortalidade em pacientes imunodeprimidos.
Nos trópicos há muitos pacientes com artrite reumatoide, asma brônquica e glomerulonefrite recebendo tratamento com esteroides em longo prazo. Os pacientes podem comprar os corticoides livremente nas farmácias.
A estrongiloidíase não é uma infecção oportunista importante associada ao HIV, mas é uma infecção oportunista associada ao vírus linfotrópico de células T humanas tipo I (HTLV-I) [19]. Embora os pacientes com vírus de imunodeficiência humana e síndrome de imunodeficiência adquirida (VIH/SIDA) possam ter síndrome de estrongiloidíase disseminada ou hiperinfecção, os estudos observacionais não demonstraram um risco aumentado nesta população [20].
2.7 Mortalidade e morbidade
A estrongiloidíase aguda é muitas vezes assintomática e pode permanecer oculta durante décadas. Se não for tratada, os pacientes imunocomprometidos têm frequentemente infecções crônicas assintomáticas durante toda a vida.
As infecções crônicas podem ser causa importante de morbidade não declarada. Também, há uma falta de ferramentas eficientes de diagnóstico, que são frequentemente complexas e de baixa sensibilidade, de forma que verdadeira prevalência da infecção e da morbidade não é conhecida. Considerando que a estrongiloidíase é vista como uma doença incomum, houve pouco investimento em estudos de diagnóstico ou epidemiológicos, especialmente em crianças.
A presença da estrongiloidíase clinicamente aparente pode provocar sintomas cutâneos, gastrointestinais e pulmonares.
A evidência destaca a necessidade de estudar os pacientes com eosinofilia, inclusive sem antecedentes de residir ou ter visitado área endêmica.[22].
Com o passar dos anos, foram desenvolvidos vários procedimentos diagnósticos cujo uso depende da disponibilidade local e do conhecimento especializado: testes do cordão, aspirados duodenais, biopsia duodenal, lavado broncoalveolar (LBA), testes imunodiagnósticos e testes repetidos de fezes frescas com diferentes métodos.
A prevalência mundial da infecção pelo Strongyloides stercoralis foi subestimada muito tempo. Isso talvez seja devido à confiança na microscopia direta das fezes e na técnica de Kato-Katz, utilizadas comumente em estudos de prevalência mas que são inadequadas para a detecção de S. stercoralis [23]. Os métodos baseados em amostras fecais comumente utilizados têm sensibilidade especialmente baixa. A microscopia pode melhorar com o exame de várias amostras de fezes e técnicas de concentração [24], mas a sensibilidade permanece baixa.
Tanto nos países de rendas baixas/médias quanto nos países desenvolvidos, o número de profissionais bem formados na identificação microscópica de parasitas parece estar diminuindo.
- A aplicação de ensaios moleculares em parasitologia, ainda muito atrasada no que respeita à virologia ou bacteriologia, deverá aumentar.
- O diagnóstico molecular da infecção pelo S. stercoralis ainda tem que demonstrar uma sensibilidade ótima.
- É pouco provável que o diagnóstico molecular substitua completamente as outras técnicas de diagnóstico.
- Os ensaios sorológicos atualmente mostram a maior sensibilidade e são importantes para a detecção de S. stercoralis e avaliação da cura [23].
Lodh e col. [25] apresentaram resultados de estudos mostrando que é possível detectar o ADN de S. stercoralis na urina. Quando disponíveis, e se forem suficientemente sensíveis, os testes de amostras de urina podem ser adequados, porque requer muito menos mão de obra e recursos e não envolve o risco para a saúde de examinar fezes frescas [25].
4.1 Exames de fezes
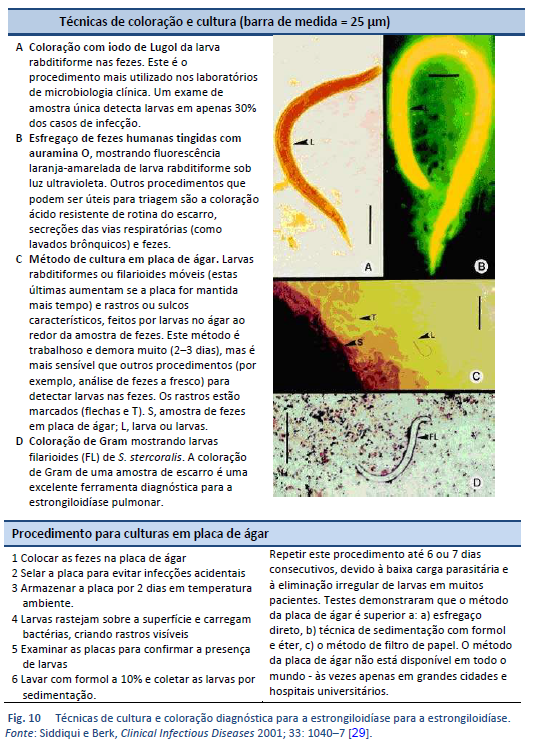
O achado microscópico de larvas nas fezes, líquido duodenal ou ocasionalmente em outros tecidos ou líquidos permite fazer diagnóstico definitivo de estrongiloidíase (Tabelas 7, 8; Figs. 10, 11). Ainda assim, devido à baixa densidade de larvas, um único exame não é sensível [26].
Vários métodos são utilizados para identificar as larvas nas fezes por microscopia:
Microscopia após concentração
- Técnica do funil de Baermann (ainda considerada como padrão ouro)
- Técnica de concentração formol-éter (TCFE)
Microscopia com culturas
- Método de Harada- Mori, cultura em filtro de papel
- Método de Koga, cultura em placa de ágar
Microscopia direta
- Uso de microscópio de disseção para identificar larvas em placas de ágar
- Esfregaço direto de fezes em coloração salina de lugol
O uso desses métodos depende da disponibilidade local de recursos e especialmente da experiência do microscopista.
Os exames de fezes para detecção de Strongyloides que usam a técnica do funil de Baermann e o método Koga de cultura em ágar são hoje os melhores métodos diagnósticos disponíveis nessa área. Eles detectam o parasita com maior sensibilidade que outros métodos.
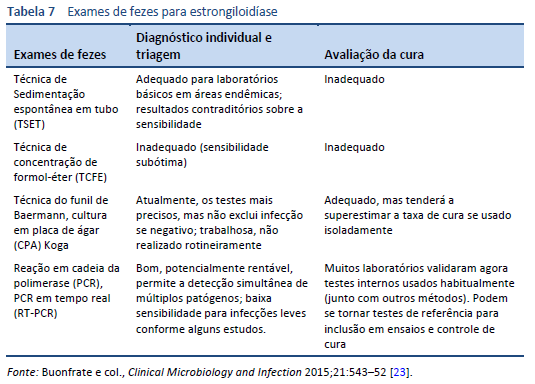
- Apesar da PCR ser prometedora, ainda não foi padronizada e existem preocupações sobre sua sensibilidade, pois varia entre os diferentes estudos.
- Anamnart e col. [27] estudaram a estimulação da excreção de larvas de S. stercoralis nas fezes administrando uma dose única de 400 mg de albendazol por via oral e sugerem que albendazol poderia ser utilizado junto com a técnica de concentração de formol-éter modificada (TCFEM) em pacientes com suspeita de estrongiloidíase assintomática, diarreia crônica inexplicável, naqueles que retornam de áreas onde a estrongiloidíase é endêmica e aqueles pacientes com resultados negativos em testes parasitológicos [27].


4.2 Sorodiagnóstico da estrongiloidíase
Se comparados à técnica de Baermann e cultura em placa de ágar, os testes sorológicos têm maior sensibilidade, embora alguns autores estejam preocupados com a especificidade [20].
- Muitos testes sorológicos apresentam reação cruzada com outros parasitas: filarias, esquistossomos e Ascaris lumbricoides, o que reduz a especificidade dos testes.
- Pode ser difícil distinguir entre casos ativos e infecções antigas, pois os anticorpos podem persistir durante algum tempo.
- Testes sorológicos mais específicos, que utilizam antígenos recombinantes, foram e continuam sendo desenvolvidos, e estão disponíveis em laboratórios específicos.
- Testes sorológicos comuns mostram uma diminuição significativa dos títulos entre os 6 e 12 meses após a erradicação do parasita, portanto, podem ser usados para avaliar a cura [20].
O método sorológico mais conveniente e mais utilizado é o ensaio imunoabsorvente ligado à enzima (ELISA) para a detecção de imunoglobulina G (IgG) no soro contra extrato bruto de larvas filarioides. O ensaio ELISA requer trabalho intensivo e certo nível de infraestrutura do laboratório para a obtenção e interpretação dos resultados, o que dificultou sua aplicabilidade, especialmente em áreas onde Strongyloides é endêmico [26]. Além disso, a sorologia tem valor limitado para o seguimento depois da cura em áreas endêmicas, pois pode ocorrer reinfecção.
4.3 Diagnóstico diferencial
Existem muitas afecções que produzem sintomas semelhantes, como certas patologias que provocam diarreia aguda ou crônica e má absorção, eosinofilia e septicemia Gram negativa grave. No diagnóstico diferencial devem ser considerados os seguintes:
- Infecções intestinais: amebíase, colite bacteriana, Shigella, Campylobacter, Yersinia, Clostridium difficile; ver a Diretriz Mundial sobre Diarreia Aguda da WGO, Tabela 4 [30].
- Infecção por ancilostomídeo não humano, que produz a larva migrans cutânea, diferenciada da larva currens do S. stercoralis por não provocar formação de crostas, rápida migração, envolvimento perianal e larga faixa de urticária
- Doença inflamatória intestinal.
- Síndrome do intestino irritável
- Transtornos gastroabdominais funcionais
- Medicamentos, anti-inflamatórios não esteroidais (AINEs) e muitos outros, podem provocar eosinofilia
A chave do diagnóstico é pensar na estrongiloidíase como um possível diagnóstico e identificar o parasita diretamente e/ou por testes sorológicos/moleculares.
- Não se pode esperar por uma cura espontânea devido ao ciclo de vida único da autoinfecção do parasita.
- Tratar todos os pacientes com estrongiloidíase, mesmo quando assintomáticos, em virtude do risco de hiperinfecção, uma complicação potencialmente mortal.
- É necessário um diagnóstico confiável dos pacientes em risco para um correto reconhecimento e tratamento antes de iniciar terapia imunossupressora, ou em pacientes com HTLV-I ou infecção pelo vírus da imunodeficiência humana (HIV).
- Se um paciente com estrongiloidíase não diagnosticada previamente precisar uma imunossupressão de emergência e os testes de diagnóstico não estiverem disponíveis rapidamente (muito poucos hospitais podem fazer uma sorologia no mesmo dia), deve ser considerado o tratamento presuntivo com ivermectina.
- A cura pode ser alcançada com uma dose única de ivermectina.
- O fracasso do tratamento com ivermectina geralmente é devido à deficiência da imunidade do hospedeiro (frequente em pacientes com infecção pelo HTLV-I) [26,31].
5.1 Estrongiloidíase não complicada
O tratamento da estrongiloidíase (Tabela 9) é difícil porque, a diferença de outras infecções helmínticas, a carga do Strongyloides deve ser erradicada completamente.
- É difícil confirmar a erradicação completa devido à baixa carga de vermes e à eliminação irregular de larvas.
- A cura não pode ser confirmada apenas com base em um exame negativo de fezes de seguimento; também é preciso constatar a diminuição tanto dos títulos sorológicos como da eosinofilia.
- Ao estudar casos conhecidos de infecção pelo Strongyloides foi constatado que uma única análise de fezes pode ser negativa para estrongiloidíase em até 70% dos casos. Para que os testes sejam confiáveis são requeridos múltiplos testes de fezes, provavelmente pelo menos três e com técnicas adequadas.
- Nos trópicos, o seguimento dos pacientes constitui um problema, e, se estiver disponível somente o exame de fezes, ele se torna o método de escolha.
- Albendazol (400 mg duas vezes por dia durante 3 dias) é usado às vezes como alternativa ou concessão [33,34]. No entanto, a eficácia do albendazol no tratamento da estrongiloidíase foi demonstrada ser muito baixa se comparado com a ivermectina e, portanto, não deve ser utilizado a menos que não exista outra alternativa [35].
5.2 Hiperinfecção ou infecção disseminada
Embora alguns autores afirmem que estes termos descrevem dois aspectos diferentes da infecção (hiperinfecção: altos níveis de larvas nas partes habituais do corpo; disseminação: larvas presentes em qualquer parte do corpo, não incluídas geralmente no ciclo parasitário), podem provavelmente ser usados indiferentemente. De fato, ambos se referem a uma carga parasitária muito alta e uma rápida expansão da infecção, geralmente em pacientes imunossuprimidos e, frequentemente, associados à corticoterapia. A hiperinfecção está relacionada a um alto risco de septicemia por Gram-negativos, portanto, são administrados antibióticos de amplo espectro, especialmente para prevenir a meningite bacteriana.
Em pessoas criticamente doentes com hiperinfecção ou estrongiloidíase disseminada, e que não podem tomar medicamentos orais, a ivermectina foi administrada com sucesso pela via subcutânea [36]. No caso de pacientes graves, a ivermectina é administrada diariamente durante pelo menos 14 dias, e a duração total do tratamento depende do momento de negativação do exame microscópico dos líquidos corporais que deram positivos para larvas (pode ser fezes ou urina ou outros em casos de hiperinfecção) [37].
5.3 Prevenção e controle de doenças
A infecção é prevenida evitando o contato direto da pele com solo contendo larvas infectantes. Pessoas em risco, especialmente crianças, devem usar calçado quando caminharem em solo infectado. Identificar pacientes em risco e realizar testes diagnósticos apropriados antes de iniciar terapia imunossupressora.
Os contatos domiciliários não correm risco de infecção. A adequada eliminação das excretas humanas reduz substancialmente a prevalência da estrongiloidíase.
Não existe nenhum regime profilático aceito nem vacina disponível.
As precauções padrão devem ser respeitadas nos pacientes internados com estrongiloidíase. As medidas higiénicas como uso de luvas e batas ou túnicas e uma cuidadosa lavagem das mãos são importantes para aqueles suscetíveis de entrarem em contato com as fezes do paciente [20].
- Detecção precoce e tratamento efetivo da infecção pelo S. stercoralis.
- Triagem dos pacientes que correm risco de apresentar estrongiloidíase crônica antes de iniciar o tratamento imunossupressor, especialmente com corticosteroides.
- A OMS ainda não recomenda a quimioterapia preventiva (QP) para infecção pelo S. stercoralis, nem está incluída na estratégia recomendada para controle do helminto transmitido pelo solo. Contudo, foram demonstrados benefícios colaterais consistentes na prevalência do S. stercoralis depois de aplicar os programas de eliminação da filariose linfática e da oncocercose que utilizavam QP repetida com ivermectina/albendazol ou só com ivermectina [38].
- Adequada avaliação do tratamento por meio de exame de fezes (com testes altamente sensíveis, como técnica de Baermann, cultura em filtro de papel e cultura em placa de ágar) e seguimento sorológico de igG específico durante 1-2 anos [39].
- Programas de tratamento presuntivo no exterior em populações de refugiados de países onde os parasitas intestinais são endêmicos (ancilostomídeo, Trichuris trichiura, Ascaris lumbricoides e Strongyloides stercoralis) [40].
- Instalação e uso de sistemas seguros de eliminação de resíduos ainda são importantes [41].
- Uso de calçado poderia interromper a transmissão da estrongiloidíase, mas a aceitabilidade cultural do calçado é baixa, especialmente em climas cálidos, portanto, devem ser avaliados outros métodos de controle ambiental [42]. As pessoas que não têm sapatos muitas vezes não têm cadeiras, então as nádegas constituem um novo objetivo.
- Detecção precoce da resistência antihelmíntica. Vários métodos in vivo e in vitro estão disponíveis para avaliar a eficácia dos antihelmínticos, e podem ser aplicados métodos de laboratório específicos para confirmar uma suspeita de resistência em campo - por exemplo, como descrito nas recomendações de estudo e diretrizes da Associação Mundial para o Avanço da Parasitologia Veterinária (WAAVP) [43–45].
O estudo de Forrer e col. [46] mostrou que o tratamento na comunidade com ivermectina em dose única contra S. stercoralis mais o saneamento reduziu efetivamente o risco de infecção nas comunidades rurais no Camboja; mais de 85% dos aldeões se mantêm negativos 1 ano após o tratamento. O controle de infecções é fatível e altamente benéfico, em particular na combinação com saneamento melhorado [46].
Khieu e col. [47] encontraram que a infecção com s. stercoralis era muito menos frequente nos indivíduos com latrina na casa do que aqueles sem ela. O risco atribuível da população calculada iria se reduzir em 39% se todos os participantes usassem latrina para defecar [17,47].
Croker e She observaram que a alta prevalência de eosinofilia em pessoas com infecção latente pelo Strongyloides no condado de Los Ángeles destaca a importância de estudar as pessoas com eosinofilia nas quais causas mais comuns foram excluídas [48].
StrongNet [38], rede internacional para melhorar o diagnóstico e o acesso ao tratamento para controle da estrongiloidíase, preconiza o uso de um método diagnóstico mais eficaz e fácil de usar no lugar, bem como a disponibilidade em grande escada de ivermectina para controle da estrongiloidíase em áreas endêmicas. Graças aos esforços desta rede, a ivermectina foi incluída recentemente na Lista de medicamentos essenciais da OMS para tratamento da estrongiloidíase; o objetivo final é desenvolver uma estratégia de controle de saúde pública e incluir S. stercoralis na estratégia de quimioterapia preventiva da OMS para helmintíase transmitida pelo solo.
5.4 Prognóstico
A estrongiloidíase aguda e crônica têm um bom prognóstico. No entanto, a infecção não tratada pode persistir por toda a vida do paciente devido ao ciclo de autoinfecção. A ausência prolongada do paciente de áreas endêmicas não é garantia de se livrar da infecção. A infecção severa disseminada é comumente um evento fatal, e muitas vezes não responde ao tratamento.
Na estrongiloidíase crônica, a imunossupressão constitui um risco de autoinfecção acelerada. Pode provocar uma síndrome similar à sepse, hiperinfecção pelo S. stercoralis e a disseminação de larvas para órgãos distantes como o sistema nervoso central, causando meningite associada ao S. stercoralis [49].
6.1 Abreviações

6.2 Diretriz padrão ouro
Centros de Controle e Prevenção de Doenças. Parasitas - Strongyloides. Recursos para profissionais da saúde [internet]. Atlanta, GA: Centros de controle e Prevenção de Doenças; 2016 [visitado 13 de março de 2018]. Disponível em:
https://www.cdc.gov/parasites/strongyloides/health_professionals/index.html. [20].
6.3 Referências
1. World Health Organization. Soil-transmitted helminth infections [Internet]. Geneva: World Health Organization; 2017 [accessed 2018 Mar 13]. Available from: http://www.who.int/mediacentre/factsheets/fs366/en/.
2. Bisoffi Z, Buonfrate D, Montresor A, Requena-Méndez A, Muñoz J, Krolewiecki AJ, et al. Strongyloides stercoralis: a plea for action. PLoS Negl Trop Dis 2013 May 9;7(5):e2214.
3. Umur Ş, Meral Y, Bölükbaş CS, Gürler AT, Açici M. First clinical Strongyloides stercoralis case in a dog in Turkey. Turk J Vet Anim Sci 2017;41:312–5.
4. Pidchayathanakorn P. Nemathelminthes [46 slides] [Internet] 2015 [accessed 2018 Mar 13]. Available from: https://www.slideshare.net/PaemikaPidchayathana/nemathelminthes-review.
5. Kelly P. Infectious diarrhoea. Med Abingdon 2015 May;43(5):253–8.
6. Knopp S, Mohammed KA, Rollinson D, Stothard JR, Khamis IS, Utzinger J, et al. Changing patterns of soil-transmitted helminthiases in Zanzibar in the context of national helminth control programs. Am J Trop Med Hyg 2009 Dec;81(6):1071–8.
7. Anselmi M, Buonfrate D, Guevara Espinoza A, Prandi R, Marquez M, Gobbo M, et al. Mass administration of ivermectin for the elimination of onchocerciasis significantly reduced and maintained low the prevalence of Strongyloides stercoralis in Esmeraldas, Ecuador. PLoS Negl Trop Dis 2015 Nov;9(11):e0004150.
8. Barda B, Albonico M, Buonfrate D, Ame SM, Ali S, Speich B, et al. Side benefits of mass drug administration for lymphatic filariasis on Strongyloides stercoralis. Prevalence on Pemba Island, Tanzania. Am J Trop Med Hyg 2017 Sep;97(3):681–3.
9. Bisoffi Z. Human strongyloidiasis: time to act? Paper presented at the 27th European Congress of Clinical Microbiology And Infectious Diseases (ECCMID), Vienna, April 2017. Basel, Switzerland: European Society of Clinical Microbiology and Infectious Diseases; 2017. (ESCMID eLibrary). Available from: www.escmid.org/escmid_publications/escmid_elibrary/material/?mid=44339.
10. World Health Organization. What are intestinal worms (soil transmitted helminthiasis)? [Internet]. Geneva: World Health Organization; [accessed 2018 Mar 13]. Available from: http://www.who.int/intestinal_worms/disease/en/.
11. Bundy DAP, Appleby LJ, Bradley M, Croke K, Hollingsworth TD, Pullan R, et al. Mass deworming programs in middle childhood and adolescence. In: Bundy DAP, de Silva N, Horton S, Jamison DT, Patton GC, editors. Child and Adolescent Health and Development [Internet]. 3rd ed. Washington, DC: International Bank for Reconstruction and Development / World Bank Group; 2017. p. 165–82. (Disease Control Priorities; vol. 8). Available from: http://dcp-3.org/chapter/2437/deworming.
12. Centers for Disease Control and Prevention. Parasites — Strongyloides [Internet]. Atlanta, GA: Centers for Disease Control and Prevention; 2015 [accessed 2018 Mar 13]. Available from: https://www.cdc.gov/parasites/strongyloides/biology.html.
13. Ross KE, Bradbury RS, Garrard TA, O’Donahoo FJ, Shield JM, Page W, et al. The National Strongyloides Working Group in Australia 10 workshops on: commendations and recommendations. Aust N Z J Public Health 2017 Jun;41(3):221–3.
14. Schär F, Trostdorf U, Giardina F, Khieu V, Muth S, Marti H, et al. Strongyloides stercoralis: global distribution and risk factors. PLoS Negl Trop Dis 2013;7(7):e2288.
15. Puthiyakunnon S, Boddu S, Li Y, Zhou X, Wang C, Li J, et al. Strongyloidiasis — an insight into its global prevalence and management. PLoS Negl Trop Dis 2014 Aug;8(8):e3018.
16. Kearns TM, Currie BJ, Cheng AC, McCarthy J, Carapetis JR, Holt DC, et al. Strongyloides seroprevalence before and after an ivermectin mass drug administration in a remote Australian Aboriginal community. PLoS Negl Trop Dis 2017 May;11(5):e0005607.
17. Schär F, Giardina F, Khieu V, Muth S, Vounatsou P, Marti H, et al. Occurrence of and risk factors for Strongyloides stercoralis infection in South-East Asia. Acta Trop 2016 Jul;159:227–38.
18. Buonfrate D, Mena MA, Angheben A, Requena-Mendez A, Muñoz J, Gobbi F, et al. Prevalence of strongyloidiasis in Latin America: a systematic review of the literature. Epidemiol Infect 2015 Feb;143(3):452–60.
19. Crompton DWT, Engels D, Savioli L, Montresor A, Neira M, editors. Preparing to control schistosomiasis and soil-transmitted helminthiasis in the twenty-first century [special double issue of journal]. Acta Trop 2003;86(2–3):121–347.
20. Centers for Disease Control and Prevention. Parasites — Strongyloides. Resources for health professionals [Internet]. Atlanta, GA: Centers for Disease Control and Prevention; 2016 [accessed 2018 Mar 13]. Available from: https://www.cdc.gov/parasites/strongyloides/health_professionals/index.html.
21. Smith JD, Goette DK, Odom RB. Larva currens. Cutaneous strongyloidiasis. Arch Dermatol 1976 Aug;112(8):1161–3.
22. Repetto SA, Ruybal P, Solana ME, López C, Berini CA, Alba Soto CD, et al. Comparison between PCR and larvae visualization methods for diagnosis of Strongyloides stercoralis out of endemic area: A proposed algorithm. Acta Trop 2016 May;157:169–77.
23. Buonfrate D, Formenti F, Perandin F, Bisoffi Z. Novel approaches to the diagnosis of Strongyloides stercoralis infection. Clin Microbiol Infect 2015 Jun;21(6):543–52.
24. Knopp S, Mgeni AF, Khamis IS, Steinmann P, Stothard JR, Rollinson D, et al. Diagnosis of soil-transmitted helminths in the era of preventive chemotherapy: effect of multiple stool sampling and use of different diagnostic techniques. PLoS Negl Trop Dis 2008;2(11):e331.
25. Lodh N, Caro R, Sofer S, Scott A, Krolewiecki A, Shiff C. Diagnosis of Strongyloides stercoralis: detection of parasite-derived DNA in urine. Acta Trop 2016 Nov;163:9–13.
26. van Doorn HR, Koelewijn R, Hofwegen H, Gilis H, Wetsteyn JCFM, Wismans PJ, et al. Use of enzyme-linked immunosorbent assay and dipstick assay for detection of Strongyloides stercoralis infection in humans. J Clin Microbiol 2007 Feb;45(2):438–42.
27. Anamnart W, Pattanawongsa A, Intapan PM, Maleewong W. Albendazole stimulates the excretion of Strongyloides stercoralis larvae in stool specimens and enhances sensitivity for diagnosis of strongyloidiasis. J Clin Microbiol 2010 Nov;48(11):4216–20.
28. Tello R, Terashima A, Marcos LA, Machicado J, Canales M, Gotuzzo E. Highly effective and inexpensive parasitological technique for diagnosis of intestinal parasites in developing countries: spontaneous sedimentation technique in tube. Int J Infect Dis 2012 Jun;16(6):e414-416.
29. Siddiqui AA, Berk SL. Diagnosis of Strongyloides stercoralis infection. Clin Infect Dis 2001 Oct 1;33(7):1040–7.
30. World Gastroenterology Organisation. Acute diarrhea in adults and children: a global perspective [Internet]. Milwaukee, WI: World Gastroenterology Organisation; 2012 [accessed 2018 Mar 13]. Available from: http://www.worldgastroenterology.org/guidelines/global-guidelines/acute-diarrhea/acute-diarrhea-english.
31. Varatharajalu R, Kakuturu R. Strongyloides stercoralis: current perspectives. Rep Parasitol 2016;(5):23–33.
32. Medscape. Ivermectin (Rx). Brand and other names: Stromectol. Dosage forms & strengths. [Internet]. Medscape; [accessed 2018 Mar 13]. Available from: https://reference.medscape.com/drug/stromectol-ivermectin-342657.
33. Horton J. Albendazole: a review of anthelmintic efficacy and safety in humans. Parasitology 2000;121 Suppl:S113-132.
34. Venkatesan P. Albendazole. J Antimicrob Chemother 1998 Feb;41(2):145–7.
35. Henriquez-Camacho C, Gotuzzo E, Echevarria J, White AC, Terashima A, Samalvides F, et al. Ivermectin versus albendazole or thiabendazole for Strongyloides stercoralis infection. Cochrane Database Syst Rev 2016 Jan 18;(1):CD007745.
36. Chiodini PL, Reid AJ, Wiselka MJ, Firmin R, Foweraker J. Parenteral ivermectin in Strongyloides hyperinfection. Lancet 2000 Jan 1;355(9197):43–4.
37. Boulware DR. Strongyloides infection. BMJ Best Pract [Internet]. Available from: http://bestpractice.bmj.com/best-practice/monograph/907/treatment/step-by-step.html.
38. Albonico M, Becker SL, Odermatt P, Angheben A, Anselmi M, Amor A, et al. StrongNet: An international network to improve diagnostics and access to treatment for strongyloidiasis control. PLoS Negl Trop Dis 2016 Sep;10(9):e0004898.
39. Luvira V, Watthanakulpanich D, Pittisuttithum P. Management of Strongyloides stercoralis: a puzzling parasite. Int Health 2014 Dec;6(4):273–81.
40. Maskery B, Coleman MS, Weinberg M, Zhou W, Rotz L, Klosovsky A, et al. Economic analysis of the impact of overseas and domestic treatment and screening options for intestinal helminth infection among US-bound refugees from Asia. PLoS Negl Trop Dis 2016 Aug;10(8):e0004910.
41. Nelson GS. [Review of D.I. Grove, A history of human helminthology (1990).]. J Helminthol 1991;65(2):120.
42. Ross KE, O’Donahoo FJ, Garrard TA, Taylor MJ. Simple solutions to Strongyloides stercoralis infection. BMJ Clin Res Ed 2013 Oct 22;347:f6294.
43. European Medicines Agency Committee for Medicinal Products for Veterinary Use (CVMP). Reflection paper on anthelmintic resistance [Internet]. London: European Medicines Agency; 2017 [accessed 2018 Mar 13]. Available from: http://www.ema.europa.eu/ema/index.jsp?curl=pages/regulation/general/general_content_001563.jsp&mid=WC0b01ac058002ddc2.
44. Wood IB, Amaral NK, Bairden K, Duncan JL, Kassai T, Malone JB, et al. World Association for the Advancement of Veterinary Parasitology (W.A.A.V.P.) second edition of guidelines for evaluating the efficacy of anthelmintics in ruminants (bovine, ovine, caprine). Vet Parasitol 1995 Jun;58(3):181–213.
45. Coles GC, Bauer C, Borgsteede FH, Geerts S, Klei TR, Taylor MA, et al. World Association for the Advancement of Veterinary Parasitology (W.A.A.V.P.) methods for the detection of anthelmintic resistance in nematodes of veterinary importance. Vet Parasitol 1992 Sep;44(1–2):35–44.
46. Forrer A, Khieu V, Schindler C, Schär F, Marti H, Char MC, et al. Ivermectin treatment and sanitation effectively reduce Strongyloides stercoralis infection risk in rural communities in Cambodia. PLoS Negl Trop Dis 2016 Aug;10(8):e0004909.
47. Khieu V, Schär F, Forrer A, Hattendorf J, Marti H, Duong S, et al. High prevalence and spatial distribution of Strongyloides stercoralis in rural Cambodia. PLoS Negl Trop Dis 2014 Jun;8(6):e2854.
48. Croker C, She R. Increase in reports of Strongyloides infection — Los Angeles County, 2013–2014. MMWR Morb Mortal Wkly Rep 2015 Aug 28;64(33):922–3.
49. Keiser PB, Nutman TB. Strongyloides stercoralis in the immunocompromised population. Clin Microbiol Rev 2004 Jan;17(1):208–17.
50. World Health Organization. World Health Assembly adopts resolution on neglected tropical diseases [Internet]. Geneva: World Health Organization; 2013 [accessed 2018 Mar 13]. Available from: http://www.who.int/neglected_diseases/WHA_66_seventh_day_resolution_adopted/en/.

























