1. Introduction
Le 21 mai, 2010, la 63ème Assemblée mondiale de l'Organisation mondiale de la santé a adopté une résolution désignant le 28 juillet comme journée mondiale de l'hépatite et a déclaré "le soutien des pays membres pour que l'OMS développe une approche détaillée pour la prévention et le contrôle de ces maladies." Les maladies concernées comprennent les hépatites virales A-E. Cette résolution, ainsi qu'une deuxième concernant la maladie hépatique alcoolique, représentent la première déclaration formelle de la part de l'OMS que les maladies hépatiques constituent un problème majeur de santé publique à l’échelon mondial. Cependant, même si les hépatites virales et la maladie hépatique alcoolique sont cruciales au niveau mondial, elles ne représentent pas toutes—ou même pas les plus importantes—les affections hépatiques à l'origine du fardeau pour la santé mondiale. Ces deux dernières décennies, il est apparu de plus en plus évident que la stéatose hépatique non alcoolique (NAFLD) et la stéato-hépatite non alcoolique (NASH) représentent actuellement la cause numéro une de maladie hépatique dans les pays occidentaux. La prévalence de la NAFLD a doublé ces 20 dernières années, tandis que la prévalence d'autres maladies hépatiques chroniques est restée stable ou a même diminué. Les données les plus récentes confirment que la NAFLD et la NASH jouent un rôle tout aussi important au Moyen-Orient, en Extrême-Orient, dans les Caraïbes et en Amérique latine.
La NAFLD est une affection caractérisée par une accumulation excessive de graisses dans le foie sous forme de triglycérides (stéatose) (>5% des hépatocytes sont atteints à l’histologie). Un sous-groupe de patients avec NAFLD présente également des lésions des cellules hépatiques ainsi qu'une inflammation en plus d'un excès de graisses (stéato-hépatite). Cette dernière situation, appelée stéato-hépatite non alcoolique (NASH), est quasi-impossible à distinguer histologiquement de la stéatohépatite alcoolique (SHA). Même si la stéatose simple rencontrée dans la NAFLD n'est pas associée à court terme avec une augmentation de la morbidité ou de la mortalité dramatique, la progression de la maladie vers une NASH augmente de façon dramatique le risque de cirrhose, d'insuffisance hépatique et de carcinome hépatocellulaire (CHC). La cirrhose due à une NASH représente une indication de plus en plus fréquence à une transplantation hépatique. Tandis que la morbidité et la mortalité dues aux problèmes hépatiques sont nettement augmentées chez les patients avec une NASH, il existe une corrélation encore plus forte avec la morbidité et la mortalité résultant d'une maladie cardiovasculaire.
Tableau 1 Mortalité dans la NAFLD/NASH
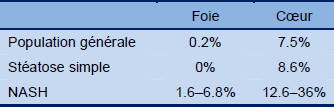
La NASH est largement considérée comme étant la manifestation hépatique du syndrome métabolique—comprenant les maladies liées à un diabète de type 2, la résistance à l’insuline, l’obésité tronculaire, une hyperlipidémie (cholestérol lié aux lipoproteïnes de faible/haute densité ; LDL-cholestérol, HDL-cholestérol), une hypertriglycéridémie et une hypertension artérielle. Il existe actuellement à l’échelon mondial une « épidémie » de diabète et d’obésité. En 2008, au moins 1.46 milliard d’adultes et 170 millions d’enfants avaient un excès pondéral ou étaient obèses. Dans certaines régions d’Afrique, davantage d’enfants souffrent d’obésité plus que de malnutrition. Ces chiffres continuent à augmenter, ce qui montre qu’à l’avenir la NASH constituera un problème de plus en plus fréquent tant dans les pays riches que dans les pays en voie de développement, augmentant ainsi le fardeau des maladies hépatiques sur le plan des coûts de la santé. On estime que la NAFLD/NASH augmentera les coûts directs et indirects de 26% dans les 5 ans.
Tableau 2 Diagnostic clinique du syndrome métabolique (directives de la Société Américaine de Cardiologie (American Heart Association) et de l’Institut National pour le Coeur, les Poumons et le Sang des Etats-Unis (National Heart, Lung, and Blood Institute)
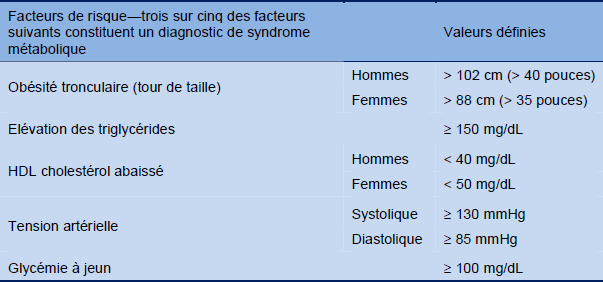
HDL, lipoprotéines de haute densité.
La cause exacte de la NASH n’a pas été formellement élucidée et il est presque certain que l’étiologie n’est pas la même chez tous les patients. Même si elle est très étroitement liée à la résistance à l’insuline, à l’obésité et au syndrome métabolique, tous les patients qui en souffrent ne présentent pas une NAFLD/NASH et inversement tous les patients avec une NAFLD/NASH ne présentent pas une résistance à l’insuline, une obésité et un syndrome métabolique. Comme déjà mentionné plus haut, la NASH demeure cependant une maladie potentiellement mortelle, entraînant une cirrhose, une insuffisance hépatique et un carcinome hépato-cellulaire.
Il n’existe aucun traitement formellement reconnu ni de directives basées sur l’évidence clinique. Il n’existe pas non plus d’étude prospective contrôlée à doubleaveugle adéquate pouvant fournir les données nécessaires à l’établissement de directives basées sur l’évidence clinique. Les présentes directives ont pour but de fournir les meilleurs avis émanant d’un groupe d’experts provenant du monde entier sur tous les aspects du problème et sur les meilleures approches diagnostiques et thérapeutiques, en tenant compte des ressources à disposition localement.
Algorithmes—une approche tenant compte des ressources à disposition
Il est possible de définir une approche de référence pour les régions et les pays qui ont à disposition toute la gamme des tests diagnostiques et des moyens thérapeutiques pour la prise en charge de la NASH. Ces ressources ne sont cependant pas à disposition partout dans le monde. L’Organisation Mondiale de Gastroentérologie mets à disposition des algorithmes diagnostiques et thérapeutiques qui tiennent compte des ressources à disposition.
Algorithme: une gamme hiérarchique d’options diagnostiques, thérapeutiques et de prise en charge en fonction les ressources à disposition.
2. Epidémiologie
La NASH est une maladie hépatique chronique de plus en plus répandue avec une distribution mondiale et qui est étroitement liée au diabète et à l’obésité, qui ont toute deux atteint les proportions d’une épidémie. Il est estimé qu’il y a au moins 1.46 milliard d’adultes souffrant d’obésité dans le monde. Il est estimé qu’environ 6 millions de personnes aux Etats-Unis ont montré une progression vers une NASH et que 600'000 souffrent d’une cirrhose liée à une NASH. Il existe des différences culturelles et géographiques importantes dans la prévalence de l’obésité.
Tandis que dans la plupart des pays occidentaux, en particulier chez les femmes, l’image corporelle idéale est celle d’une grande minceur avec un minimum de graisse corporelle, ceci n’est pas forcément vrai partout ailleurs dans le monde. Dans beaucoup de cultures, l’obésité est considérée comme souhaitable et est également considérée comme signe marqué de prospérité (cf. par exemple les données émanant d’Egypte citées ci-dessous).
Aux Etats-Unis, l’obésité est particulièrement épidémique dans les groupes socioéconomiques peu favorisés qui se nourrissent en grande partie d’aliments riches en graisses et en calories (restauration rapide—« fast food »). Le contraire se rencontre dans beaucoup de pays pauvres où la prévalence de l’obésité est plus marquée dans les populations aisées et mieux éduquées.
Données régionales concernant l’obésité/l’excès pondéral
Tableau 3 Données régionales concernant l’obésité/l’excès pondéral (exemples représentatifs)
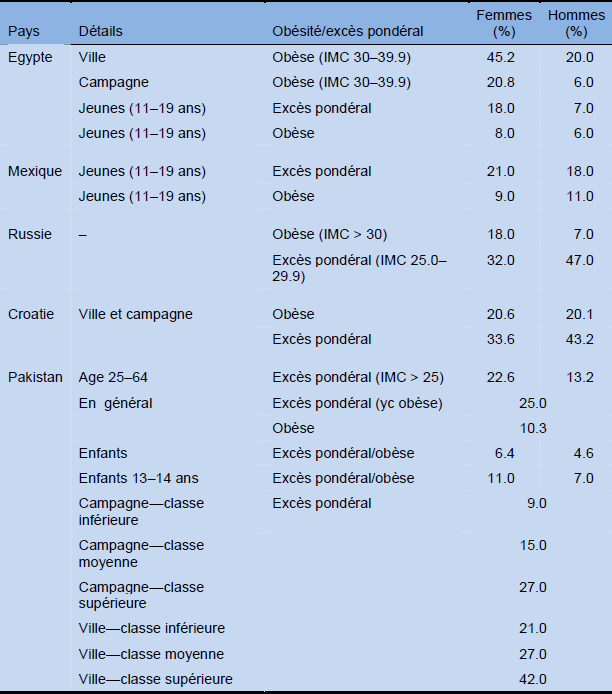
IMC, index de masse corporelle.
Fig. 1 Estimation de la prévalence de l’obésité (IMC > 25) chez les hommes et les femmes de plus de 15 ansin males and females aged 15+ (2010).
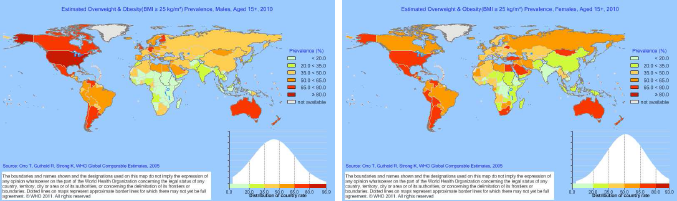
Source: WHO InfoBase.
Tableau 4 Excès pondéral/obésité—résumé de la prévalence par région (2004)
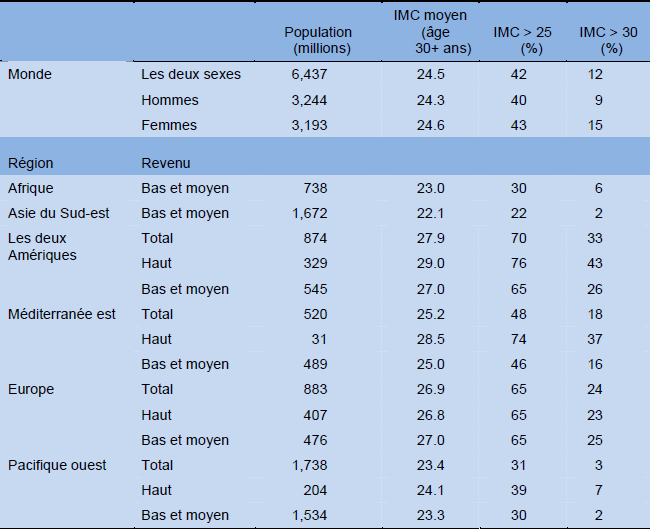
Source: OMS 2009 [25]. Cliquer ici pour trouver la source.
Prévalence de la NAFLD/NASH
Tableau 5 Estimation de la prévalence de la NAFLD et de la NASH. Il existe une différence importante dans la prévalence de la NAFLD et de la NASH en raison des définitions différentes, des différences entre les populations étudiées et les moyens diagnostiques utilisés
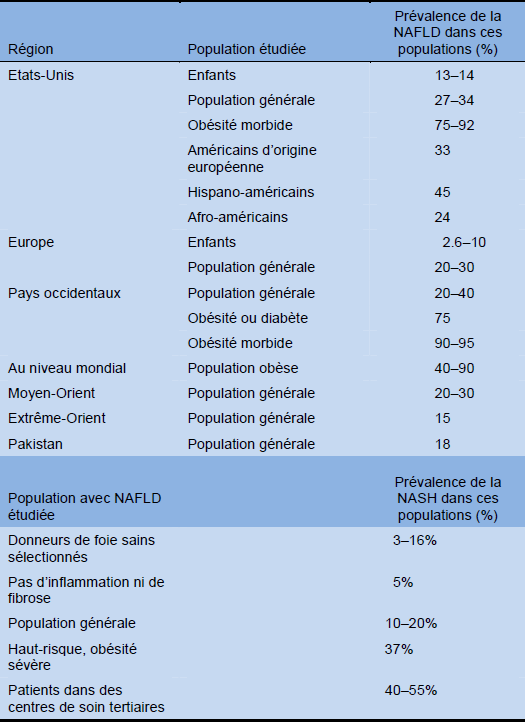
3. Pathogenèse et facteurs de risque
La NASH est considérée comme la manifestation la plus sévère histologiquement de la stéatose hépatique non alcoolique (NAFLD), définie comme une accumulation de graisses dans le foie représentant plus de 5% du poids du foie. Des critères uniformes pour le diagnostic et les différentes stades de la NASH sont actuellement sujet de discussion (voir ci-dessous).
La résistance à l’insuline est en relation avec l’obésité et constitue l’élément clé dans la pathogénèse de la NAFLD. Le stress oxydatif et les cytokines représentent également des facteurs favorisants importants, qui s’associent dans la pathogénèse de la stéatose et de l’atteinte hépatique progressive chez les sujets génétiquement susceptibles.
Les composants histologiques clés de la NASH sont la stéatose, le ballonnement des hépatocytes et l’inflammation lobulaire ; la fibrose ne fait pas partie de la définition histologique de la NASH. Cependant le degré de fibrose lors d’une biopsie hépatique (stade) est considéré comme étant un facteur prédictif dans le pronostic, tandis que le degré d’inflammation et de nécrose (grade) ne le sont pas.
La maladie peut très bien rester asymptomatique pendant des années ou bien progresser vers une cirrhose et un carcinome hépatocellulaire.
Un des hypothèses dans la pathogénèse de la NASH est l’hypothèse multifactorielle selon laquelle le syndrome métabolique joue un rôle majeur en raison de la résistance à l’insuline avec des composants proinflammatoires relayés par différentes protéines et processus communs. L’identité de ces multiples facteurs n’est pas la même chez tous les patients et demeure actuellement en grande partie non identifiée.
Fig. 2 L’hypothèse multifactorielle de la stéato-hépatite non alcoolique (NASH).
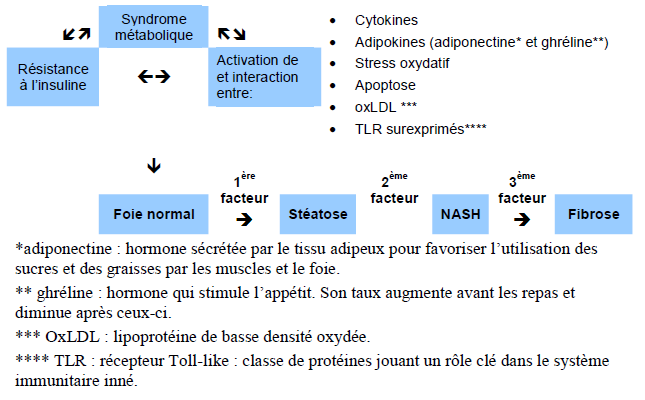
Facteurs de risque et conditions associées
Une population à faible risque se caractérise par: la jeunesse, une bonne santé, une faible consommation d’alcool et l’absence d’obésité.
Tableau 6 Facteurs de risque et conditions associées
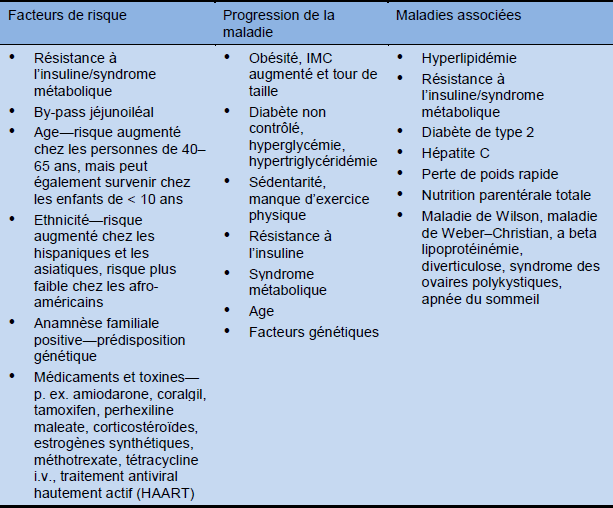
Tableau 7 Calcul de la résistance à l’insuline

HOMA, homeostasis model assessment; QUICKI, quantitative insuline sensitivity check index.
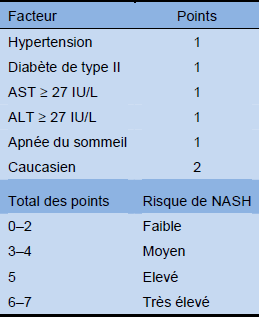
Tableau 8 Système de score pour la NASH dans l’obésité morbide
Pronostic et complications
- Progression de la maladie de la NAFLD à la NASH à la cirrhose/insuffisance hépatique et au CHC.
- La NAFLD n’aggrave pas l’hépatotoxicité et n’augmente pas les effets secondaires des médicaments, y compris les inhibiteurs de l’HMG-CoA réductase.
- La NAFLD avec une obésité associée et les facteurs métaboliques associés peut aggraver d’autres maladies hépatiques—p. ex. une maladie hépatique alcoolique.
- L’association de la NAFLD avec l’hépatite C ou le HIV aggrave le pronostic et diminue les réponses au traitement.
- Une hépatite C, de génotype 3, est fréquemment associée à une stéatose hépatique, ce qui peut rendre problématique le diagnostic d’hépatite C vs. NASH vs. les deux ensemble.
- Une biopsie hépatique peut indiquer la sévérité de la maladie, mais seule la fibrose et non l’inflammation ou la nécrose, permet d’établir un pronostic.
- Une progression histologique vers l’étape terminale de la maladie hépatique peut se produire: NASH + fibrose en pont ou cirrhose.
- La NASH en phase finale est souvent une cause mal reconnue de cirrhose cryptogénique ; une fibrose progressive pourrait être masquée par une stéatose stable ou en voie d’amélioration et par des facteurs sérologiques, surtout chez les patients plus âgés avec une NASH.
- La présence d’une cirrhose cryptogénique en relation avec une NASH augmente le risque de carcinome hépatocellulaire (CHC).
- Causes de mortalité chez les patients avec une NASH au stade de la cirrhose:
- Insuffisance hépatique
- Septicémie
- Hémorragie digestive sur rupture de varices
- CHC
- Maladie cardiovasculaire
Tableau 9 Taux de survie de la NASH et comparaison avec la stéatose simple et la stéatose alcoolique (ASH)

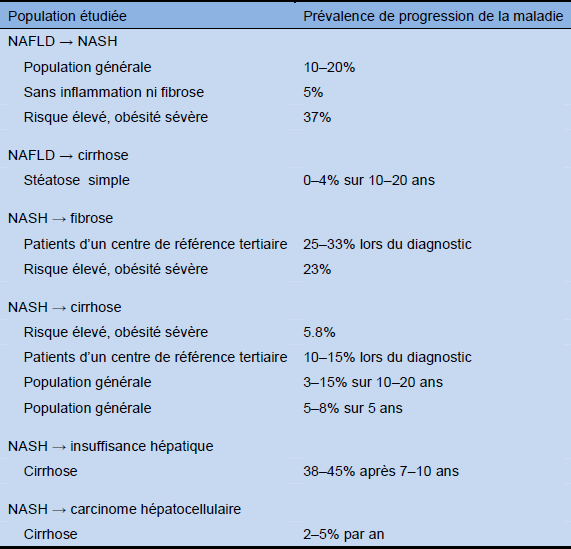
Tableau 10 Progression de la NAFLD vers la NASH, la cirrhose, l’insuffisence hépatique et le CHC. Les résultats des études de prévalence et d’incidence varient considérablement à cause des différences de définition, des différentes populations étudiées et des méthodes de diagnostic utilisées.
- Facteurs prédictifs indépendants de la progression de la fibrose:
- Age > 45–50
- IMC > 28–30 kg/m2
- Degré de résistance à l’insuline
- Diabète
- Hypertension artérielle
- Impact négatif sur la survie en présence d’une NASH:
- Diabète et alanine aminotransférase sérique (ALT) et asparate aminotransférase (AST) sériques élevées
- Age avancé et présence d’une inflammation nécrotique à la biopsie hépatique initiale
- Age avancé avec glycémie à jeun pathologique et présence d’une cirrhose
4. Diagnostic
Anamnèse et évaluation clinique
- Symptomatologie:
- En général, pas de symptomatologie particulière en cas de NASH.
- Parfois vagues symptômes de fatigue, malaise et gène abdominale.
- En présence d’un des éléments suivants, surtout s’il existe une notion d’élévation des ASAT/ALAT, un bilan pour NAFLD/NASH devrait être effectué:
- Présence d’une obésité, surtout en cas d’obésité morbide (IMC > 35)
- Diagnostic d’une diabète de type 2
- Diagnostic d’un syndrome métabolique
- Anamnèse d’un syndrome d’apnée du sommeil
- Présence d’une résistance à l’insuline (voir ci-dessous et Tableau 7)
- Elévation chronique des AST/ALT, autrement inexpliquée
- Anamnèse détaillée concernant la consommation d’alcool—seuil < 20 g/jour chez les femmes, < 30 g/jour chez les hommes. Ceci est crucial car il n’existe à ce jour aucun examen diagnostic permettant de distinguer avec certitude entre ASH et NASH.
- Il est nécessaire d’utiliser des questionnaires spécifiques appropriés ou des systèmes de notation pour l’évaluation de la consommation d’alcool.
- Test CAGE: CAGE est un acronyme pour les quatre questions suivantes:
- Vous êtes vous déjà senti Coupable au sujet de votre consommation d’alcool?
- Avez-vous déjà ressenti le besoin d’Abaisser votre consommation d’alcool?
- Avez-vous déjà eu le besoin de boire de l’alcool en vous réveillant pour calmer vos nerfs ou faire passer un Gueule de bois?
- Avez-vous déjà été Ennuyé par des remarques d’autrui critiquant votre consommation d’alcool? Le test CAGE est un moyen de dépistage largement utilisé pour mettre en évidence un alcoolisme et permet de confirmer une consommation d’alcool cliniquement significative si la réponse à au moins une des questions s’avère positive et si le score de l’Alcohol Use Disorders Identification Test (AUDIT) est supérieur à 8.
- Bien qu’une abstention totale de toute consommation d’alcool soit généralement conseillée en présence d’une maladie hépatique, ceci peut poser problème chez les patients avec un syndrome métabolique chez qui une maladie coronarienne a été mise en évidence et chez qui une consommation modeste de vin a pu se montrer bénéfique. Quelques rares études suggèrent qu’une consommation modeste de vin (0.12 L par jour) peut être associée à une prévalence abaissée de NAFLD. Son efficacité en tant que traitement d’une NAFLD existante n’a pas été étudiée.
- Une corrélation existe entre une obésité tronculaire et la sévérité de l’inflammation mise en évidence à la biopsie hépatique; une lipohypertrophie dorsocervicale (bosse de bison) est associée avec une lésion des hépatocytes.
- Signes physiques en cas de progression/de maladie hépatique avancée: angiomes stellaires, ascite, hépatomégalie, splénomégalie, érythème palmaire, ictère, encéphalopathie hépatique.
Tests de laboratoire de routine et examens par imagerie
- ALT et AST élevées:
- ALT et AST peuvent se être normales chez 10% des patients avec une NASH, en particulier chez les patients avec une stéatose simple.
- Il est toujours nécessaire d’exclure une NASH en présence d’une ferritine anormale avec une saturation de la transferrine normale.
- Rapport AST/ALT < 1—ce rapport est habituellement > 2 en cas d’hépatite alcoolique.
- Tests d’imagerie typiques confirmant une accumulation de graisses dans le foie:
- L’imagerie par résonance magnétique (IRM) a une valeur quantitative, mais ne permet pas de distinguer entre une NASH et une stéato-hépatite alcoolique (SHA).
- L’ultrasonographie est la méthode de dépistage habituelle pour la stéatose hépatique.
Aucune méthode d’imagerie ne peut identifier la présence de graisses avec certitude si < 33% ou faire la distinction entre NASH et SHA.
Examens visant à exclure:
- Hépatite virale—antigène de surface pour hépatite B (HBs Ag), anticorps pour le virus de l’hépatite C ou HCV-RNA, anticorps pour l’hépatite A de type IgM, anticorps pour l’hépatite E (dans le cadre géographique approprié); il est cependant à noter que le patient peut souffrir à la fois d’une hépatite virale et d’une NAFLD/NASH.
- Maladie hépatique en relation avec une consommation d’alcool y compris une stéato-hépatite alcoolique (SHA).
- Maladie hépatique auto-immune.
- Maladie hépatique congénitale chronique: hémochromatose héréditaire, maladie de Wilson, déficit en alpha-1-antitrypsine, syndrome des ovaires polykystiques.
- Maladie hépatique d’origine médicamenteuse.
Examens de laboratoire, systèmes de scores et modalités d’imagerie
Plusieurs tentatives ont été faites afin de développer des systèmes de score ou de techniques d’imagerie afin de pouvoir poser un diagnostic de NASH de façon non invasive et d’éviter la nécessité d’effectuer une biopsie hépatique. Actuellement aucun système ou technique n’a été testé assez de manière rigoureuse dans le cadre d’études prospectives à double-aveugle ; leur aptitude à prédire le pronostic ou la réponse à un traitement n’a pas non plus été évaluée. La plupart des tests sériques spécifiques ou des scores émanent uniquement de certains laboratoires ou de laboratoires de recherche et ce à un prix très élevé ; ils n’ont ainsi que de peu de valeur dans les pays avec de faibles ressources. Il en va de même pour les modalités d’imagerie spécialisées, y compris le FibroScan qui utilise un nouveau paramètre original « d’atténuation contrôlée (PAC) », et pour la tomographie par émission de positrons (TEP/PET scan) qui sont peu disponibles, très chers et qui souffrent d’un manque de données contrôlées.
L’article de Dowman et al. [7] passe en revue de façon approfondie les diverses modalités et les données à disposition à l’heure actuelle. Ratziu et al. [11] ont également largement commenté ces thèmes. Les méthodes discutées sont prometteuses pour l’avenir mais ne peuvent être recommandées actuellement pour l’usage général.
Biopsie hépatique
Une biopsie hépatique est indispensable afin d’établir le diagnostic et le stade de la NASH, même si la biopsie est invasive et qu’il existe potentiellement la possibilité d’erreurs d’échantillonage et que l’interprétation histopathologique peut s’avérer contradictoire. Le système de notation histologique le plus couramment utilisé actuellement est résumé dans le Tableau 11 ; il est utilisé essentiellement dans le cadre d’études contrôlées pour évaluer les effets de traitements expérimentaux plutôt que pour permettre d’établir un diagnostic de NASH. Il a été validé de façon indépendante et s’applique aussi bien chez les adultes et chez les enfants souffrant de NAFLD/NASH. Il n’existe pas de moyen fiable pour distinguer entre NAFLD/ALD et NASH/SHA sans effectuer de biopsie hépatique. En raison de la difficulté d’interpréter une biopsie hépatique de façon adéquate, il est souhaitable que celle-ci soit lue par un hépatopathologue spécialisé avec une expérience en matière de diagnostic histopathologique.
Tableau 11 Système de notation histologique de la NASH selon le Clinical Research Network
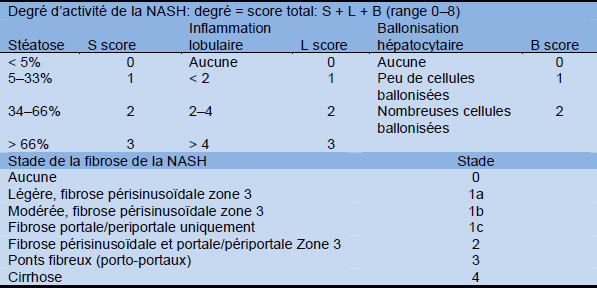
Source: Kleiner et al., Hepatology 2005;41:1313–21 [35].
Une biopsie hépatique avec histologie est indiquée afin de permettre de confirmer un diagnostic de NASH, ainsi que pour le grading et le staging de la maladie, et afin de pouvoir exclure un autre diagnostic en présence d’une ou plusieurs des observations suivantes:
- Une ferritine sérique anormale en absence d’une élévation de la saturation de la transferrine
- Une cytopénie
- Une splénomégalie
- Des signes cliniques d’une maladie hépatique chronique
- Un diabète avec des AST/ALT anormales et constamment élevées
- Une obésité avec un âge > 45 ou AST/ALT anormales
- Une hépatomégalie inexpliquée
Tableau 12 Examens diagnostiques pour la stéatose hépatique
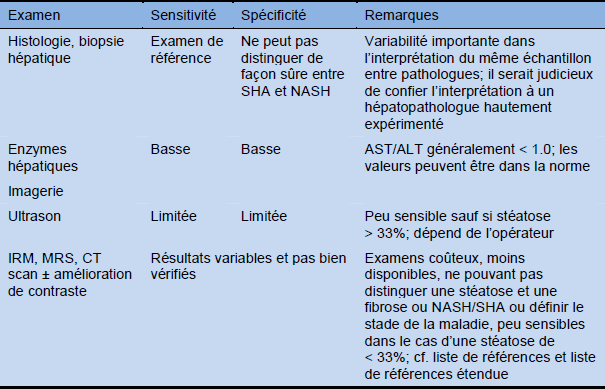
ALT, alanine aminotransferase; ASH, stéatohépatite alcoolique; AST, aspartate aminotransférase; CT, tomodensitométrie; IRM, imagerie par résonance magnétique; SRM, spectroscopie par résonance magnétique; NASH, stéatohépatite non alcoolique.
Stratégie diagnostique pour la NASH
Fig. 3 Algorithme de prise en charge pour la stéatose hépatique noon alcoolique selon Rafiq et Younossi [10].
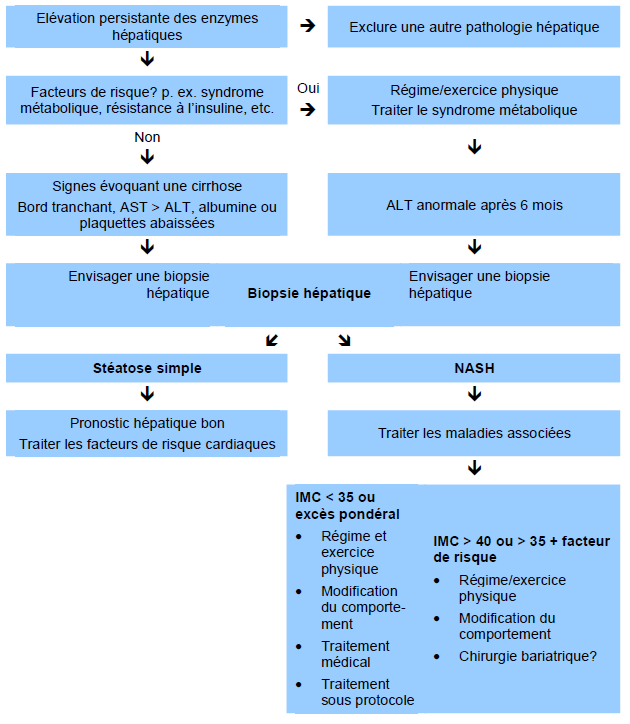
Tests hépatiques et ultrasonographie hépatique:
- Chez des patients qui consultent pour une résistance à l’insuline/un syndrome métabolique/un diabète
Imagerie pour évaluation de la présence d’une stéatose:
- Chez des patients avec des enzymes hépatiques élevées
Biopsie hépatique:
- Peut être indiquée s’il existe une forte suspicion de fibrose avancée, en présence d’enzymes hépatiques élevées et si l’ultrasonographie s’avère positive pour une stéatose.
- Pour déterminer la sévérité de la maladie/la fibrose en présence d’examens non invasifs peu conclusifs.
- Indiquée chez les patients avec une maladie hépatique chronique (à part NAFLD) et des tests positifs pour des facteurs de risque métabolique, une résistance à l’insuline et une stéatose à l’ultrasonographie.
- Pour exclure une NASH en présence d’une ferritine élevée avec une saturation de la transferrine normale.
- Pendant une intervention chirurgicale chez d’autres groupes à haut risque—p. ex. chirurgie bariatrique, cholécystectomie.
Aucun test non invasif ne permet d’exclure d’autres possibles maladies sous jacentes ou d’établir le stade de la maladie dans un but pronostic.
Au bout du compte, NAFLD/NASH constitue un diagnostic d’exclusion et une biopsie hépatique sera souvent nécessaire afin de confirmer le diagnostic, d’établir le stade de la maladie, d’exclure une autre pathologie hépatique ainsi que pour déterminer la nécessité d’un traitement agressif et de l’urgence à l’effectuer.
Fig. 4 Algorithme pour la biopsie hépatique chez les patients suspectés d’avoir une NAFLD, après exclusion d’une autre pathologie hépatique.
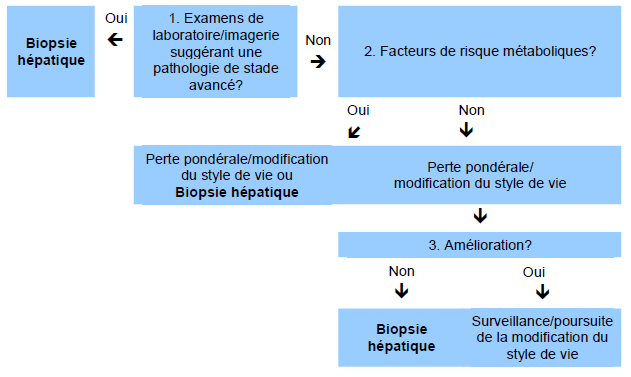
Fig. 5 Options diagnostiques pour NAFLD

ALT, alanine aminotransferase; AMA, anticorps antimitochondries; ANA, anticorps antinucléaires; anti-LKM Ab, anticorps anti-microsomes du foie et du rein; ASMA, anticorps anti-muscle lisse; AST, aspartate aminotransférase; IMC, indice de masse corporelle; CT, tomographie computérisée; FBG, glycémie à jeun; GGT, gamma-glutamyl transférase; HBsAg, antigène de surface de l’hépatite B; HCV, virus hépatite C.
Cascade—options diagnostiques chez les patients avec une suspicion de NAFLD/NASH
Tableau 13 Cascade diagnostique en tenant compte de ressources élevées, moyennes et faibles
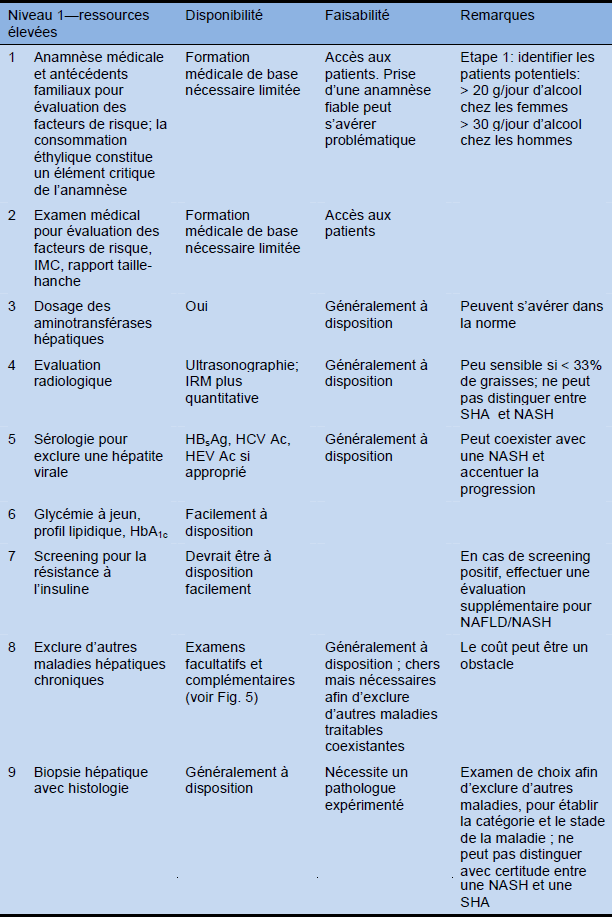
Ac, anticorps; HbA1c, hémoglobine glyquée; HBsAg, antigène de surface de l’hépatite B; HCV, virus hépatite C; HEV, virus hépatite E; MRI, imagerie par résonance magnétique.

Ac, anticorps; HbA1c, hémoglobine glyquée; HBsAg, antigène de surface de l’hépatite B; HCV, virus hépatite C; HEV, virus hépatite E.

5. Prise en charge
Rationnel thérapeutique
Les cibles du traitement sont la résistance à l’insuline et le stress oxydatif. Plusieurs options thérapeutiques sont actuellement en cours d’évaluation, mais la valeur de la majorité des traitements demeure incertaine ou l’effet bénéfique cesse lors de l’arrêt du traitement. Les objectifs du traitement de la NASH sont une réduction des lésions histologiques, une amélioration de la résistance à l’insuline et des enzymes hépatiques.
Actuellement, il n’existe aucun traitement médicamenteux approuvé et basé sur les preuves pour la NAFLD/NASH. Une modification du style de vie est cruciale si on espère inverser le cours d’une NAFLD/NASH.
En l’absence de traitement pouvant représenter un standard de référence, la prise en charge d’une NASH se concentre sur les maladies associées. La NASH devrait bénéficier d’une prise en charge agressive afin de prévenir la progression vers une cirrhose, les patients concernés n’étant fréquemment pas aptes à bénéficier d’une transplantation hépatique en raison d’une obésité morbide, de maladies cardiovasculaires ou d’autres complications liées à la maladie sous jacente.
L’objectif général de la modification du style de vie devrait être une réduction de l’excès pondéral: il a été démontré que même une perte pondérale progressive de 5–10% aboutit à une amélioration de l’histologie et des enzymes hépatiques, mais pas de la fibrose. On a plus de chances de succès en combinant la perte de poids avec un entraînement physique actif et une renoncement à la sédentarité. Dans certaines cultures, il serait peut-être nécessaire d’utiliser une approche tenant compte des sensibilités locales pour expliquer les problèmes liés à l’obésité car celle-ci peut être considérée comme un signe de beauté/attractivité et/ou prospérité.
La transplantation hépatique est appropriée en présence d’une insuffisance hépatique. Environ 30–40% des patients avec une cirrhose liée à une NASH ont besoin d’une transplantation hépatique. La plupart des programmes de transplantation récusent les patients avec un IMC élevé (> 35 à > 45, selon les critères utilisés localement). Une NASH peut récidiver dans le foie transplanté ou une nouvelle NASH peut se développer.
Options thérapeutiques pour la NASH
Comme mentionné ci-dessus, les modifications du style de vie sont cruciales si on veut inverser le cours d’une NAFLD/NASH, et il n’existe actuellement aucun traitement médicamenteux fondé sur les preuves et approuvé pour une NAFLD/NASH.
Traitement des problèmes métaboliques
Un contrôle efficace du diabète de type II, de l’hyperlipidémie et des risques cardiovasculaires est recommandé. Des études sur l’atorvastatine et la pravastatine ont montré une amélioration de l’histologie chez les patients avec une NASH. Les patients souffrant d’une NAFLD avec dyslipidémie devraient être traité par des statines. Les patients avec une maladie hépatique sous-jacente ne semblent pas avoir un risque supplémentaire de toxicité liée aux statines. Une hépatotoxicité due aux statines est rare.
Amélioration de la sensibilité à l’insuline—perte pondérale
- Régime: l’objectif devrait être une perte pondérale de 5–10% avec une diminution de l’apport calorique normal de 25% (apport calorique normal estimé à environ 2500 calories par jour) selon l’âge et le sexe du patient. Un régime comportant une restriction calorique modérée avec une modification de la composition des macronutriments produit des résultats plus favorables qu’un régime très pauvre en calories. Il faudrait veiller à expliquer le rôle d’un régime hypocalorique et donner des conseils concernant le type d’aliments à consommer—éviter le fructose et les graisses trans présentes dans les boissons non alcoolisées et les fast-foods et augmenter les acides gras polyinsaturés oméga-3/oméga-6 dans le régime alimentaire. Les patients peuvent avoir des difficultés à adhérer à un tel régime et beaucoup reprennent du poids après une perte pondérale initiale.
- Exercice physique: il faut encourager le patient à instaurer un programme d’exercice physique modéré 3-4 fois par semaine afin d’atteindre un rythme cardiaque de 60–75% du maximum conseillé pour l’âge du patient.
- Il faudrait évaluer l’efficacité des mesures diététiques et de l’exercice physique après 6 mois ; en l’absence d’effet favorable, il faudrait envisager d’autres options thérapeutiques tel un traitement médicamenteux.
- Chirurgie bariatrique peut s’avérer bénéfique chez les patients avec une obésité morbide; comme déjà mentionné, celle-ci devrait être prise en considération suffisamment tôt car la plupart des programmes excluent les patients qui souffrent déjà d’une cirrhose. Il existe quelques études montrant une amélioration dramatique de la maladie hépatique ainsi que des autres complications du syndrome métabolique/résistance à l’insuline après une chirurgie bariatrique réussie.
- Les médicaments visant la résistance à l’insuline (thiazolidinediones, metformine) sont actuellement approuvés pour traiter le diabète mais pas la NAFLD/NASH, et devraient être considérés comme traitement expérimental (voir la liste de références ci-dessous pour de plus amples informations et une discussion détaillée).
Agents antioxydants et antifibrotiques
Les agents antioxydants et antifibrotiques, tels la vitamine E et la pentoxifylline, ne sont pas approuvés pour le traitement de la NASH/NAFLD. Il n’existe que peu de données à ce sujet et peu voire presque pas de données émanant d’études contrôlées à double-aveugle. Ces médicaments sont tous considérés comme expérimentaux (voir la liste de références ci-dessous pour de plus amples informations et une discussion détaillée).
Stratégie de surveillance
La progression de la maladie et d’éventuelles complications peuvent être mises en évidence pendant le suivi comme indiqué dans le Tableau 14.
Tableau 14 Examens de suivi et leur échéance
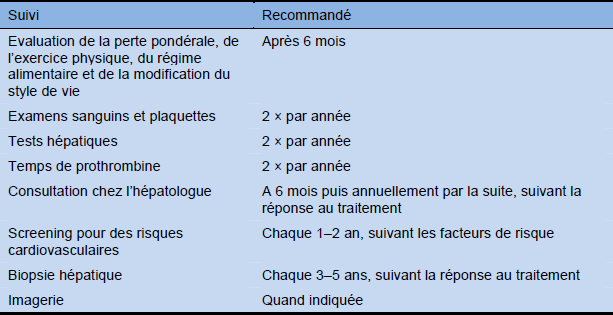
Cascades—options thérapeutiques
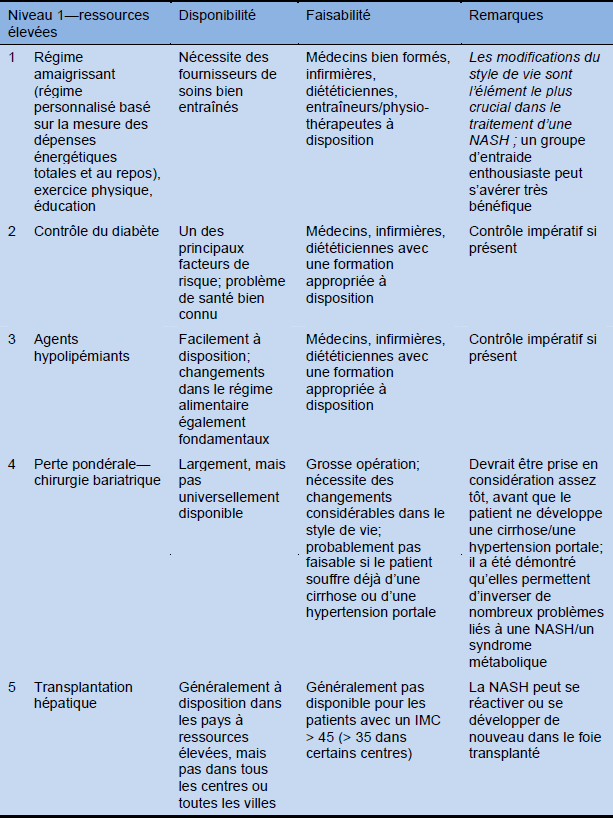
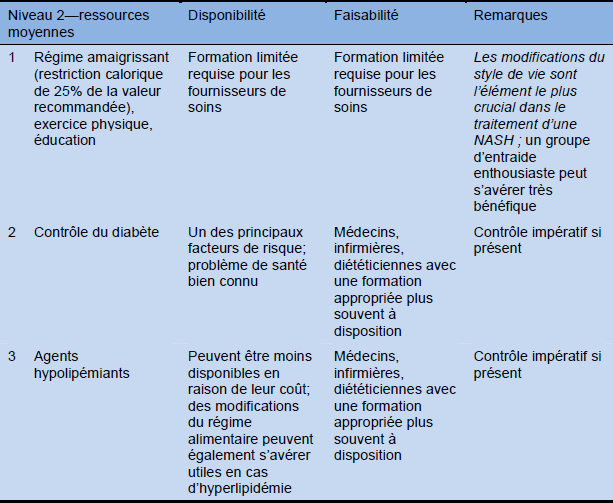
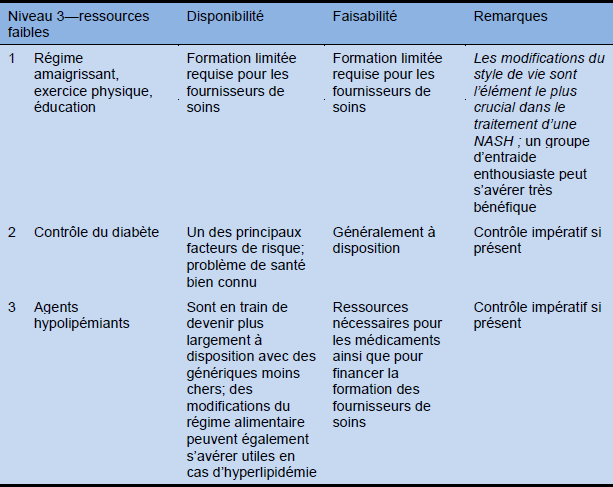
Tableau 15 Cascade pour le traitement en tenant compte de ressources élevées, moyennes et faibles
6. Résumé
- La NAFLD et la NASH représentent un problème mondial majeur de santé publique qui touche aussi bien les pays riches que les pays pauvres.
- Il n’existe actuellement pas suffisamment d’évidence pour justifier un screening pour la NASH/la maladie hépatique avancée dans la population générale.
- Il est impératif d’établir un diagnostic chez tous les patients qui présentent des facteurs de risque pour une NASH. Les patients avec facteurs de risque n’auront pas tous une NAFLD ou une NASH; inversement tous les patients avec une NASH ne présentent pas les facteurs de risque habituels.
- Il n’est pas nécessaire d’instaurer un traitement agressif chez tous les patients avec une stéatose.
- Un régime approprié et un programme d’exercice physique devraient être mis en place chez tous ces patients.
- Une biopsie hépatique devrait être pratiquée uniquement chez les patients avec des facteurs de risque pour une NASH et/ou d’autres maladies hépatiques.
- Les patients avec une NASH ou des facteurs de risque pour une NASH devraient d’abord être traités par un régime amaigrissant et un programme d’exercice physique avec l’adjonction éventuelle de vitamine E ou de pentoxifylline. Un traitement expérimental ne devrait être envisagé que par des praticiens expérimentés et uniquement chez les patients qui n’ont pas réussi à atteindre une perte pondérale de 5–10% après 6 mois - une année de modification réussie de leur style de vie.
- Une chirurgie bariatrique devrait être envisagée chez les patients chez qui les mesures décrites ci-dessus ont échoué et elle devrait en tout cas se faire avant que les patients ne développent une cirrhose.
- Une transplantation hépatique peut être couronnée de succès chez les patients répondant aux critères d’une insuffisance hépatique, mais une NASH peut se reproduire après transplantation ; les patients avec une obésité morbide peuvent se voir refuser une transplantation.
- La NAFLD et la NASH sont en train de devenir un problème de plus en plus sérieux chez les enfants, y compris chez les enfants de moins de 10 ans.
- En fin de compte, la NAFLD et la NASH constituent des diagnostics d’exclusion et il faut considérer soigneusement tout autre diagnostic. Tout comme le clinicien ne peut établir un diagnostic de NASH uniquement sur la base des données cliniques, le pathologue peut documenter des lésions de stéatohépatite à l’histologie, mais ne peut pas distinguer de façon certaine si ces lésions sont d’origine non alcoolique ou au contraire d’origine alcoolique.
Références
Position statements and reviews
Comme déjà cité dans l’Introduction, il n’existe pas assez d’études randomisées, contrôlées, à double-aveugle pour pouvoir fournir des données basées sur les preuves et ainsi permettre d’établir un guideline formel. Suit une liste d’articles sélectionnés: position statements, reviews, and expert opinion articles.
- Angulo P. Nonalcoholic fatty liver disease. N Engl J Med 2002;346:1221–31. PMID: 11961152.
- Angulo P. Diagnosing steatohepatitis and predicting liver-related mortality in patients with NAFLD: two distinct concepts. Hepatology 2011;53:1792–4. doi: 10.1002/hep.24403. PMID: 21557278.
- Brunt EM. Nonalcoholic steatohepatitis. Semin Liver Dis 2004;24:3–20. PMID: 15085483.
- Chalasani N, Younossi Z, Lavine JE, Diehl AM, Brunt EM, Cusi K, et al. The diagnosis and management of non-alcoholic fatty liver disease: Practice Guideline by the American Association for the Study of Liver Diseases, American College of Gastroenterology, and the American Gastroenterological Association. Hepatology 2012;55:2005–23. doi: 10.1002/hep.25762. PMID: 22488764
- Cheung O, Sanyal AJ. Recent advances in nonalcoholic fatty liver disease. Curr Opin Gastroenterol 2010;26:202–8. PMID: 20168226.
- Clark JM, Brancati FL, Diehl AM. Nonalcoholic fatty liver disease. Gastroenterology 2002;122:1649–57. PMID: 12016429.
- Dowman JK, Tomlinson JW, Newsome PN. Systematic review: the diagnosis and staging of non-alcoholic steatohepatitis. Aliment Pharmacol Ther 2011;33:525–40. doi:10.1111/j.1365- 2036-2010.04556.x. Epub 2010 Dec 29. PMID: 21198708.
- Fabbrini E, Sullivan S, Klein S. Obesity and nonalcoholic fatty liver disease: biochemical, metabolic, and clinical implications. Hepatology 2010;51:679–89. PMID: 20041406.
- Lancet 2011 Aug 27–Sept 2;378(9793): virtually this entire issue addresses the global obesity pandemic, with articles on world epidemiology, cultural and political costs, pathogenesis, therapy, and proposed approaches to the problem. A virtual primer on global obesity. Articles are detailed in the next section, under Epidemiology.
- Rafiq N, Younossi ZM. Nonalcoholic fatty liver disease: a practical approach to evaluation and management. Clin Liver Dis 2009;13:249–66. PMID: 19442917.
- Ratziu V, Bellentani S, Cortez-Pinto H, Day C, Marchesini G. A position statement on NAFLD/NASH based on the EASL 2009 special conference. J Hepatol 2010;53:372–84. Epub 2010 May 7. PMID: 20494470
- Sanyal AJ, Brunt EM, Kleiner DE, Kowdley KV, Chalasani N, Lavine JE, et al. Endpoints and clinical trial design for nonalcoholic steatohepatitis. Hepatology 2011;54:344–53. doi: 10.1002/hep.24376. PMID: 21520200.
- Torres DM, Harrison SA. Diagnosis and therapy of nonalcoholic steatohepatitis. Gastroenterology 2008;134:1682–98. PMID: 18471547.
- Vernon G, Baranova A, Younossi ZM. Systematic review: the epidemiology and natural history of non-alcoholic fatty liver disease and non-alcoholic steatohepatitis in adults. Aliment Pharmacol Ther 2011;24:274–85. doi: 10.1111/j.1365-2036.2011.04724.x. Epub 2011 May 30. PMID: 2162852.
- Vuppalachi R, Chalasani N. Nonalcoholic fatty liver disease and nonalcoholic steatohepatitis: selected practical issues in their evaluation and management. Hepatology 2009;49:306–17. PMID: 19065650.
Bibliographie étendue
Pour ceux qui souhaite des informations complémentaires et de connaître les bases pour les recommandations mentionnées dans ce guideline, il existe une liste d’articles supplémentaire soigneusement sélectionnés sous les titres d’épidémiologie, épidémiologie pédiatrique, diagnostic histologique, diagnostic non invasif, hépatite C et NAFLD/NASH, pathophysiologie et traitement.
Epidémiologie
- Lancet 2011 Aug 27–Sept 2;378(9793).
- Editorial. Urgently needed: a framework convention for obesity control Lancet 2011;378:742.PMID: 21872732.
- Baur LA. Changing perceptions of obesity—recollections of a paediatrician. Lancet 2011;378:762–3. PMID: 21877330.
- Dietz WH. Reversing the tide of obesity. Lancet 2011;378:744–6. PMID: 21872735.
- Freudenberg N. The social science of obesity. Lancet 2011;378:760.
- Gortmaker SL, Swinburn BA, Levy D, Carter R, Mabry PL, Finegood DT, et al. Changing the future of obesity: science, policy, and action. Lancet 2011;378:838–47. PMID: 21872752.
- Hall KD, Sacks G, Chandramohan D, Chow CC, Wang YC, Gortmaker SL, et al. Quantification of the effect of energy imbalance on bodyweight. Lancet 2011;378:826–37. PMID: 21872751.
- King D. The future challenge of obesity. Lancet 2011;378:743–4. PMID: 21872734.
- Mozaffarian D. Diets from around the world—quality not quantity. Lancet 2011;378:759.
- Pincock S. Boyd Swinburn: combating obesity at the community level. Lancet 2011;378:761. PMID: 21872738.
- Rutter H. Where next for obesity? Lancet 2011;378:746–7. PMID: 21872736.
- Swinburn BA, Sacks G, Hall KD, McPherson K, Finegood DT, Moodie ML, et al. The global obesity pandemic: shaped by global drivers and local environments. Lancet 2011;378:804–14.
- Wang YC, McPherson K, Marsh T, Gortmaker SL, Brown M. Health and economic burden of the projected obesity trends in the USA and the UK. Lancet 2011;378:815–25. PMID: 21872750.
- Adams LA. Mortality in nonalcoholic fatty liver disease: clues from the Cremona study. Hepatology 2011;54:6–8. doi: 10.1002/hep.24445. PMID: 21618568.
- Centers for Disease Control and Prevention. 1990–2010 changes of percentage of obese adults in the USA (BMI > 30). Available at: www.cdc.gov/obesity/data/trends.html.
- Danaei G, Finucane MM, Lu Y, Singh GM, Cowan MJ, Paciorek CJ, et al. National, regional, and global trends in fasting plasma glucose and diabetes prevalence since 1980: systematic analysis of health examination surveys and epidemiological studies with 370 country-years and 2.7 million participants. Lancet 2011;378:31–40. Epub 2011 Jun 24. PMID: 21705069.
- Gastaldelli A, Kozakova M, Højlund K, Flyvbjerg A, Favuzzi A, Mitrakou A, et al. Fatty liver is associated with insulin resistance, risk of coronary heart disease, and early atherosclerosis in a large European population. Hepatology 2009;49:1537–44. PMID: 19291789.
- Gu D, Reynolds K, Wu X, Chen J, Duan X, Reynolds RF, et al. Prevalence of the metabolic syndrome and overweight among adults in China. Lancet 2005;365:1398–405.
- Ludwig DS, Currie J. The association between pregnancy weight gain and birthweight: a withinfamily comparison. Lancet 2010;376:984–90. Epub 2010 Aug 4. PMID: 20691469.
- Passas G, Akhtar T, Gergen P, Hadden WC, Kahn AQ. Health status of the Pakistani population: a health profile and comparison with the United States. Am J Public Health 2001;91:93–8.
- Williams CD, Stengel J, Asike MI, Torres DM, Shaw J, Contreras M, et al. Prevalence of nonalcoholic fatty liver disease and nonalcoholic steatohepatitis among a largely middle-aged population utilizing ultrasound and liver biopsy: a prospective study. Gastroenterology 2011;140:124–31. Epub 2010 Sep 19. PMID: 20858492.
- World Health Organization. Global health risks: mortality and burden of disease attributable to selected major risks. Geneva: World Health Organization, 2009; Overweight and obesity—summary of prevalence by region. Geneva: World Health Organization, 2004. Available at: www.who.int/evidence/bod and www.who.int/healthinfo/global_burden_disease/risk_factors/en/index.html.
- Younossi ZM, Stepanova M, Afendy M, Fang Y, Younossi Y, Mir H, et al. Changes in the prevalence of the most common causes of chronic liver diseases in the United States from 1988 to 2008. Clin Gastroenterol Hepatol 2011;9:524–530.e1; quiz e60. Epub 2011 Mar 25. PMID:21440669.
Epidémiologie pédiatrique
- Alkhouri N, Carter-Kent C, Lopez R, Rosenberg WM, Pinzani M, Bedogni G, et al. A combination of the pediatric NAFLD fibrosis index and enhanced liver fibrosis test identifies children with fibrosis. Clin Gastroenterol Hepatol 2011;9:150–5. Epub 2010 Oct 1. PMID: 20888433.
- Galal OM. The nutrition transition in Egypt: obesity, undernutrition and the food consumption context. Public Health Nutr 2002;5:141–8. Review. PMID: 12027277.
- Kerkar N. Non-alcoholic steatohepatitis in children. Pediatr Transplant 2004;8:613–8. PMID: 15598336.
- Mathur P, Das MK, Arora NK. Non-alcoholic fatty liver disease and childhood obesity. Indian J Pediatr 2007;74:401–7. PMID: 17476088.
- Salazar-Martinez E, Allen B, Fernandez-Ortega C, Torres-Mejia G, Galal O, Lazcano-Ponce E. Overweight and obesity status among adolescents from Mexico and Egypt. Arch Med Res 2006;37:535–42. PMID: 16624655.
Diagnostic histologique
- Angulo P. Long-term mortality in nonalcoholic fatty liver disease: is liver histology of any prognostic significance? Hepatology 2010;51:373–5. Erratum in: Hepatology 2010 May;51(5):1868. PMID: 20101746.
- Brunt EM, Tiniakos DG. Histopathology of nonalcoholic fatty liver disease. World J Gastroenterol 2010;16:5286–96. Review. PMID: 21072891.
- Brunt EM, Janney CG, Di Bisceglie AM, Neuschwander-Tetri BA, Bacon BR. Nonalcoholic steatohepatitis: a proposal for grading and staging the histological lesions. Am J Gastroenterol 1999;94:2467–74. PMID: 10484010.
- Kleiner DE, Brunt EM, Van Natta M, Behling C, Contos MJ, Cummings OW, et al. Design and validation of a histological scoring system for nonalcoholic fatty liver disease. Hepatology 2005;41:1313–21. PMID: 15915461.
- Tiniakos DG. Nonalcoholic fatty liver disease/nonalcoholic steatohepatitis: histological diagnostic criteria and scoring systems. Eur J Gastroenterol Hepatol 2010;22:643–50. PMID: 19478676.
- Younossi ZM, Stepanova M, Rafiq N, Makhlouf H, Younoszai Z, Agrawal R, et al. Pathologic criteria for nonalcoholic steatohepatitis: interprotocol agreement and ability to predict liverrelated mortality. Hepatology 2011;53:737–45. doi: 10.1002/hep.24131. Epub 2011 Feb 11. PMID: 21360720.
Diagnostic non invasif
- Angulo P, Hui JM, Marchesini G, Bugianesi E, George J, Farrell GC, et al. The NAFLD fibrosis score: a noninvasive system that identifies liver fibrosis in patients with NAFLD. Hepatology 2007;45:846–54. PMID: 17393509.
- Babor TF, Higgins-Biddle JC, Saunders JB, Monteiro MG. The alcohol use disorders identification test: guidelines for use in primary care. 2nd ed. Geneva: World Health Organization, 2001.
- Baranova A, Younossi ZM. The future is around the corner: noninvasive diagnosis of progressive nonalcoholic steatohepatitis. Hepatology 2008;47:373–5. PMID: 18220279.
- Bedogni G, Bellentani S, Miglioli L, Masutti F, Passalacqua M, Castiglione A, et al. The Fatty Liver Index: a simple and accurate predictor of hepatic steatosis in the general population. BMC Gastroenterol 2006;6:33. PMID: 17081293.
- Calori G, Lattuada G, Ragogna F, Garancini MP, Crosignani P, Villa M, et al. Fatty liver index and mortality: the Cremona study in the 15th year of follow-up. Hepatology 2011;54:145–52. doi: 10.1002/hep.24356. PMID: 21488080.
- Campos GM, Bambha K, Vittinghoff E, Rabl C, Posselt AM, Ciovica R, et al. A clinical scoring system for predicting nonalcoholic steatohepatitis in morbidly obese patients. Hepatology 2008;47:1916–23. PMID: 18433022.
- Chalasani N. Nonalcoholic fatty liver disease liver fat score and fat equation to predict and quantitate hepatic steatosis: promising but not prime time! Gastroenterology 2009;137:772–5. Epub 2009 Jul 26. PMID: 19638269.
- Cho CS, Curran S, Schwartz LH, Kooby DA, Klimstra DS, Shia J, et al. Preoperative radiographic assessment of hepatic steatosis with histologic correlation. J Am Coll Surg 2008;206:480–8. Epub 2007 Nov 26. PMID: 18308219.
- Hernaez R, Lazo M, Bonekamp S, Kamel I, Brancati FL, Guallar E, et al. Diagnostic accuracy and reliability of ultrasonography for the detection of fatty liver: A meta-analysis. Hepatology 2011;54:1082–9. doi: 10.1002/hep.24452. PMID: 21618575.
- Hettihawa LM, Palangasinghe S, Jayasinghe SS, Gunasekara SW, Weerarathna TP. Comparison of insulin resistance by indirect methods—HOMA, QUICKI and McAuley—with fasting insulin in patients with type 2 diabetes in Galle, Sri Lanka: a pilot study. Online J Health Allied Sci 2006;1:2. Available at: http://www.ojhas.org/issue17/2006-1-2.htm.
- Hrebícek J, Janout V, Malincíková J, Horáková D, Cízek L. Detection of insulin resistance by simple quantitative insulin sensitivity check index QUICKI for epidemiological assessment and prevention. J Clin Endocrinol Metab 2002;87:144–7. PMID: 11788638.
- Imbert-Bismut F, Naveau S, Morra R, Munteanu M, Ratziu V, Abella A, et al. The diagnostic value of combining carbohydrate-deficient transferrin, fibrosis, and steatosis biomarkers for the prediction of excessive alcohol consumption. Eur J Gastroenterol Hepatol 2009;21:18–27. PMID: 19011575.
- Katz A, Nambi SS, Mather K, Baron AD, Follmann DA, Sullivan G, et al. Quantitative insulin sensitivity check index: a simple, accurate method for assessing insulin sensitivity in humans. J Clin Endocrinol Metab 2000;85:2402–10. PMID: 10902758.
- Keskin M, Kurtoglu S, Kendirci M, Atabek ME, Yazici C. Homeostasis model assessment is more reliable than the fasting glucose/insulin ratio and quantitative insulin sensitivity check index for assessing insulin resistance among obese children and adolescents. Pediatrics 2005;115:e500–3. Epub 2005 Mar 1. PMID: 15741351.
- Kotronen A, Peltonen M, Hakkarainen A, Sevastianova K, Bergholm R, Johansson LM, et al. Prediction of non-alcoholic fatty liver disease and liver fat using metabolic and genetic factors. Gastroenterology 2009;137:865–72. Epub 2009 Jun 12. PMID: 19524579.
- Matthews DR, Hosker JP, Rudenski AS, Naylor BA, Treacher DF, Turner RC. Homeostasis model assessment: insulin resistance and beta-cell function from fasting plasma glucose and insulin concentrations in man. Diabetologia 1985;28:412–9. PMID: 3899825.
- Poynard T, Ratziu V, Naveau S, Thabut D, Charlotte F, Messous D, et al. The diagnostic value of biomarkers (SteatoTest) for the prediction of liver steatosis. Comp Hepatol 2005;4:10. PMID: 16375767.
- Saadeh S, Younossi ZM, Remer EM, Gramlich T, Ong JP, Hurley M, et al. The utility of radiological imaging in nonalcoholic fatty liver disease. Gastroenterology 2002;123:745–50. PMID: 12198701.
- Stern SE, Williams K, Ferrannini E, DeFronzo RA, Bogardus C, Stern MP. Identification of individuals with insulin resistance using routine clinical measurements. Diabetes 2005;54:333–9. PMID: 15677489.
- Thabut D, Naveau S, Charlotte F, Massard J, Ratziu V, Imbert-Bismut F, et al. The diagnostic value of biomarkers (AshTest) for the prediction of alcoholic steato-hepatitis in patients with chronic alcoholic liver disease. J Hepatol 2006;44:1175–85. Epub 2006 Mar 13. PMID: 16580087.
- Yajima Y, Ohta K, Narui T, Abe R, Suzuki H, Ohtsuki M. Ultrasonographic diagnosis of fatty liver: significance of the liver–kidney contrast. Tohoku J Exp Med 1983;139:43–50. PMID: 6220488.
Hépatite C et NAFLD/NASH
- Bugianesi E, Marchesini G, Gentilcore E, Cua IH, Vanni E, Rizzetto M, et al. Fibrosis in genotype 3 chronic hepatitis C and nonalcoholic fatty liver disease: role of insulin resistance and hepatic steatosis. Hepatology 2006;44:1648–55. PMID: 17133473.
- Charlton MR, Pockros PJ, Harrison SA. Impact of obesity on treatment of chronic hepatitis C. Hepatology 2006;43:1177–86. PMID: 16729327.
- Everhart JE, Lok AS, Kim HY, Morgan TR, Lindsay KL, Chung RT, et al. Weight-related effects on disease progression in the hepatitis C antiviral long-term treatment against cirrhosis trial. Gastroenterology 2009;137:549–57. Epub 2009 May 13. PMID: 19445938.
- Koike K. Hepatitis C as a metabolic disease: Implication for the pathogenesis of NASH. Hepatol Res 2005;33:145–50. Epub 2005 Oct 3. PMID: 16202646.
- Negro F, Clément S. Impact of obesity, steatosis and insulin resistance on progression and response to therapy of hepatitis C. J Viral Hepat 2009;16:681–8. Epub 2009 Sep 1. PMID: 19732324.
- Popkin BM. Is the obesity epidemic a national security issue around the globe? Curr Opin Endocrinol Diabetes Obes 2001;18:328–31. PMID: 21543976.
- Powell EE, Jonsson JR, Clouston AD. Metabolic factors and non-alcoholic fatty liver disease as co-factors in other liver diseases. Dig Dis 2010;28:186–91. Epub 2010 May 7. PMID: 20460909.
- Sanyal AJ, Banas C, Sargeant C, Luketic VA, Sterling RK, Stravitz RT, et al. Similarities and differences in outcomes of cirrhosis due to nonalcoholic steatohepatitis and hepatitis C. Hepatology 2006;43:682–9. PMID: 16502396.
- Targher G, Day CP, Bonora E. Risk of cardiovascular disease in patients with nonalcoholic fatty liver disease. N Engl J Med 2010;363:1341–50. PMID: 20879883.
Pathophysiologie
- Ascha MS, Hanouneh IA, Lopez R, Tamimi TA, Feldstein AF, Zein NN. The incidence and risk factors of hepatocellular carcinoma in patients with nonalcoholic steatohepatitis. Hepatology 2010;51:1972–8. PMID: 20209604.
- de Alwis NM, Day CP. Non-alcoholic fatty liver disease: the mist gradually clears. J Hepatol 2008;48(Suppl 1):S104–12. Epub 2008 Feb 4. PMID: 18304679.
- Lim JS, Mietus-Snyder M, Valente A, Schwarz JM, Lustig RH. The role of fructose in the pathogenesis of NAFLD and the metabolic syndrome. Nat Rev Gastroenterol Hepatol 2010;7:251–64. Epub 2010 Apr 6. PMID: 20368739.
- Neuschwander-Tetri BA. Evolving pathophysiologic concepts in nonalcoholic steatohepatitis. Am J Gastroenterol 2001;96:2813–4. PMID: 11693313.
- Polyzos SA, Kountouras J, Zavos C. The multi-hit process and the antagonistic role of tumor necrosis factor-alpha and adiponectin in non alcoholic fatty liver disease. Hippokratia 2009;13:127. PMID:19561788.
- Zein CO, Unalp A, Colvin R, Liu YC, McCullough AJ; Nonalcoholic Steatohepatitis Clinical Research Network. Smoking and severity of hepatic fibrosis in nonalcoholic fatty liver disease. J Hepatol 2011;54:753–9. Epub 2010 Sep 22. PMID: 21126792.
Traitement
- Abdelmalek MF, Suzuki A, Guy C, Unalp-Arida A, Colvin R, Johnson RJ, et al. Increased fructose consumption is associated with fibrosis severity in patients with nonalcoholic fatty liver disease. Hepatology 2010;51:1961–71. PMID: 20301112.
- Brunt EM, Kleiner DE, Wilson LA, Belt P, Neuschwander-Tetri BA; NASH Clinical Research Network (CRN). Nonalcoholic fatty liver disease (NAFLD) activity score and the histopathologic diagnosis in NAFLD: distinct clinicopathologic meanings. Hepatology 2011;53:810–20. doi: 10.1002/hep.24127. Epub 2011 Feb 11. PMID: 21319198
- Bugianesi E, Gentilcore E, Manini R, Natale S, Vanni E, Villanova N, et al. A randomized controlled trial of metformin versus vitamin E or prescriptive diet in nonalcoholic fatty liver disease. Am J Gastroenterol 2005;100:1082–90. PMID: 15842582.
- Charlton MR, Burns JM, Pedersen RA, Watt KD, Heimbach JK, Dierkhising RA. Frequency and outcomes of liver transplantation for nonalcoholic steatohepatitis in the United States. Gastroenterology 2011;141:1249–53. Epub 2011 Jul 2. PMID: 21726509.
- Chavez-Tapia NC, Tellez-Avila FL, Barrientos-Gutierrez T, Mendez-Sanchez N, Lizardi- Cervera J, Uribe M. Bariatric surgery for non-alcoholic steatohepatitis in obese patients. Cochrane Database Syst Rev 2010;(1):CD007340. PMID: 20091629.
- Dunn W, Xu R, Schwimmer JB. Modest wine drinking and decreased prevalence of suspected nonalcoholic fatty liver disease. Hepatology 2008;47:1947–54. PMID: 18454505.
- Geier A. Shedding new light on vitamin D and fatty liver disease. J Hepatol 2011;55:273–5. Epub 2011 Jan 12. PMID: 21236303.
- Georgescu EF. Angiotensin receptor blockers in the treatment of NASH/NAFLD: could they be a first-class option? Adv Ther 2008;25:1141–74. PMID: 18972077.
- Henriksen JH, Ring-Larsen H. Rosiglitazone: possible complications and treatment of nonalcoholic steatohepatitis (NASH). J Hepatol 2008;48:174–6. Epub 2007 Nov 5. PMID: 18022724.
- Mummadi RR, Kasturi KS, Chennareddygari S, Sood GK. Effect of bariatric surgery on nonalcoholic fatty liver disease: systematic review and meta-analysis. Clin Gastroenterol Hepatol 2008;6:1396–402. Epub 2008 Aug 19. PMID: 18986848.
- Nakano T, Cheng YF, Lai CY, Hsu LW, Chang YC, Deng JY, et al. Impact of artificial sunlight therapy on the progress of non-alcoholic fatty liver disease in rats. J Hepatol 2011;55:415–25. Epub 2010 Dec 22. PMID: 21184788
- Neuschwander-Tetri BA. NASH: Thiazolidinediones for NASH—one pill doesn’t fix everything. Nat Rev Gastroenterol Hepatol 2010;7:243–4. PMID: 20442730.
- Promrat K, Kleiner DE, Niemeier HM, Jackvony E, Kearns M, Wands JR, et al. Randomized controlled trial testing the effects of weight loss on nonalcoholic steatohepatitis. Hepatology 2010;51:121–9. PMID: 19827166.
- Ratziu V, Giral P, Jacqueminet S, Charlotte F, Hartemann-Heutier A, Serfaty L, et al. Rosiglitazone for nonalcoholic steatohepatitis: one-year results of the randomized placebocontrolled Fatty Liver Improvement with Rosiglitazone Therapy (FLIRT) Trial. Gastroenterology 2008;135:100–10. Epub 2008 Apr 8. PMID: 18503774
- Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass NM, et al. Pioglitazone, vitamine E, or placebo for nonalcoholic steatohepatitis. N Engl J Med 2010;362:1675–85. Epub 2010 Apr 28. PMID: 20427778.
- Suzuki A, Lindor K, St. Saver J, Lymp J, Mendes F, Muto A, et al. Effect of changes on body weight and lifestyle in nonalcoholic fatty liver disease. J Hepatol 2005;43:1060–6. Epub 2005 Jul 11. PMID: 16140415.
- Zein CO, Yerian LM, Gogate P, Lopez R, Kirwan JP, Feldstein AE, et al. Pentoxifylline improves nonalcoholic steatohepatitis: a randomized placebo-controlled trial. Hepatology 2011;54:1610–9. doi: 10.1002/hep.24544. Epub 2011 Aug 24. PMID: 21748765.
- Zelber-Sagi S, Nitzan-Kaluski D, Goldsmith R, Webb M, Zvibel I, Goldiner I, et al. Role of leisure-time physical activity in nonalcoholic fatty liver disease: a population-based study. Hepatology 2008;48:1791–8. PMID: 18972405.




























