5.1 Por qué é difícil diagnosticar a doença celíaca?
- O amplo espectro de características clínicas, que podem variar durante a vida do paciente.
- Os sintomas podem se sobrepor aos da síndrome do intestino irritável.
- Os pacientes podem ter manifestações extraintestinais, ou inclusive nenhum sintoma.
- Existe uma falta de consciência sobre a doença celíaca entre os médicos (e pacientes).
- Há falta de capacidade de diagnóstico em algumas áreas geográficas, como a África intertropical.
Existem também vários “mitos”, como:
- A doença celíaca é rara.
- A doença celíaca ocorre:
- Apenas em caucasianos
- Principalmente na Europa e nos Estados Unidos.
- Apenas na infância.
- Apenas em pacientes com diarreia crônica.
- A doença celíaca pode ser curada após (um período de) tratamento.
- A doença celíaca é um transtorno leve e “o problema desaparece após o diagnóstico e uma dieta sem glúten”.
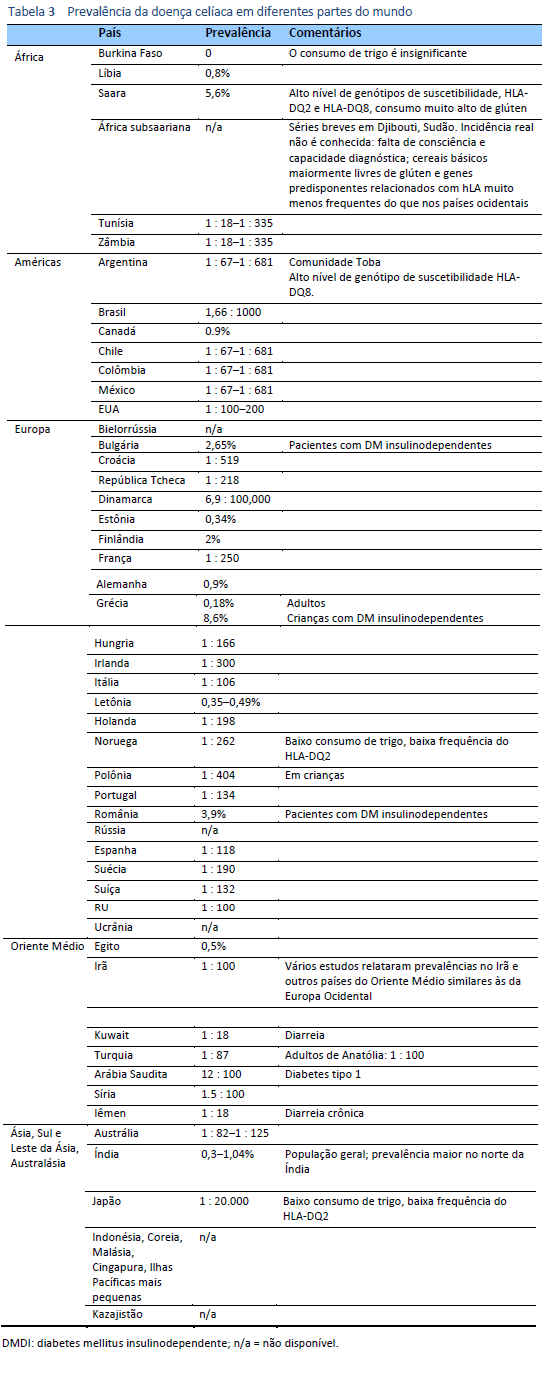
Em adultos e crianças, o diagnóstico de doença celíaca depende da presença de autoanticorpos positivos específicos para a doença celíaca e biopsias intestinais diagnósticas concomitantes [15].
Em pacientes sintomáticos com sinais de má absorção (doença celíaca clássica), foi sugerido que a presença de títulos elevados (10×) de autoanticorpos (anti-transglutaminase) confirmados por testes de autoanticorpos positivos (AAE ou DGP) em uma segunda amostra de sangue seria suficiente para diagnosticar doença celíaca, sem biopsias intestinais. Isso deve ser considerado após analisar os prós e contras com um médico especialista [62].
- Para diagnóstico, segundas biopsias (pós-tratamento) não são necessárias na maioria dos pacientes, se elas tiverem resultados positivos na sorologia diagnóstica inicial e responderem satisfatoriamente a uma dieta sem glúten. Não existe consenso entre especialistas ou diretrizes a respeito desta declaração [63,64].
- As segundas biopsias devem ser reservadas para pacientes nos quais as primeiras biopsias e testes sorológicos foram inconclusivos (por exemplo, enteropatia soronegativa) ou para pacientes que não respondem apesar da adesão estrita à dieta sem glúten [65].
- O teste de provocação com glúten, no qual é reintroduzido glúten puro ou alimentos contendo glúten, deve ser reservada para pacientes que iniciaram uma dieta sem glúten mas têm diagnóstico duvidoso [66,67].
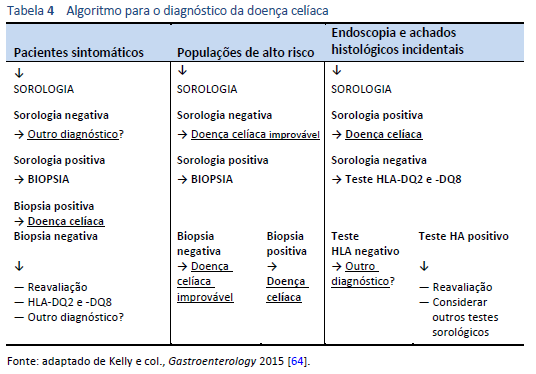
5.2 Quais pacientes devem ser examinados?
Uma revisão recente [68] sugere que, embora a doença celíaca cumpra vários critérios da OMS para a triagem em massa, ainda falta uma prova suficiente de seu benefício, e uma estratégia de detecção proativa de casos em grupos de alto risco é, hoje, a abordagem apropriada.
5.2.1 Pacientes com manifestações clínicas sugestivas de doença celíaca
- Diarreia crônica ou intermitente (por exemplo, SII)
- Anemia ferropriva
- Atraso no desenvolvimento
- Perda de peso
- Atraso no crescimento
- Puberdade tardia
- Amenorreia primária ou secundária
- Fadiga persistente
- Dermatite herpetiforme, tipo erupção
- Fratura por traumatismo menor/osteopenia/osteoporose
- Infertilidade
- Ataxia
- Aumento inexplicável das transaminases
5.2.2 Condições associadas a um maior risco de doença celíaca
• Diabetes mellitus tipo 1
• Doença tireoidiana autoimune
• Doença hepática autoimune
• Síndrome de Down
• Síndrome de Turner
• Síndrome de Williams
• Deficiência seletiva de imunoglobulina A (IgA)
• Níveis elevados de aminotransferase sérica sem explicação
Nota: estas condições podem não estar relacionadas patogenicamente à doença celíaca, mas a alta prevalência de casos torna necessário fazer testes sorológicos aos pacientes.
5.2.3 Parentes de primeiro grau de pacientes com doença celiaca
- Todos os parentes de primeiro grau devem ser triados para a doença celíaca.
- Aproximadamente 7-10% dos parentes de primeiro grau podem desenvolver doença celíaca, e o risco varia consideravelmente segundo sua relação com o paciente índice.
- O risco de ter doença celíaca é maior nos irmãos (9%), seguido por filhos (8%) e pais (3%). Enquanto as irmãs e filhas do paciente índice têm maior risco de ter doença celíaca (uma em cada sete e uma em cada oito, respectivamente), o risco é de um em cada 13 filhos, um em cada 16 irmãos, uma em cada 32 mães e um em cada 33 em pães. O risco de ter doença celíaca é maior nos parentes de segundo grau (2,3%) dos pacientes, em comparação com a população geral [69].
- Tipificação HLA para todos os parentes de primeiro grau; não fazer mais exames naqueles que são negativos para HLA-DQ2/8. O risco de casos positivos para HLA-DQ2 /-DQ8 varia segundo os alelos presentes com o maior risco para indivíduos homozigotos para DQ2. A soroconversão anual acumulada para anticorpos positivos foi estimada em menos de 1%, com a maior taxa de incidência entre os 12 e 36 meses [44].
5.3 Diferenças nos critérios diagnósticos da doença celíaca
Os critérios diagnósticos para a doença celíaca podem diferir em algumas partes do mundo devido a vários fatores.
- Os títulos de corte para a maioria dos testes sorológicos são baseados em dados de populações caucasianas. O título de corte para um teste positivo, sensibilidade e especificidade pode variar com a idade, etnia e região de residência.
- Embora a doença celíaca seja a causa predominante de anomalias vilositárias nas populações caucasianas, em muitos países o espru tropical, as infecções parasitárias e as doenças imunoproliferativas do intestino delgado também são causas importantes de anomalias vilositárias.
5.4 Testes diagnósticos
5.4.1 Endoscopia em pacientes com suspeita de doença celíaca
Embora a endoscopia não seja suficientemente sensível nem específica [70] para detectar a doença celíaca, os seguintes achados endoscópicos [71] devem levantar suspeita:
- Pregas duodenais serrilhadas
- Fissuras nas pregas e um padrão de mosaico na mucosa
- Pregas achatadas
- Pregas de tamanho reduzido e/ou que desaparecem com máxima insuflação
- Ausência de vilosidades na ampliação
- Aparência granular do bulbo duodenal
As biópsias da mucosa intestinal sempre devem ser obtidas quando for observada qualquer uma das características endoscópicas acima expostas. Também devem ser obtidas biopsias endoscópicas, apesar das pregas endoscópicas parecerem normais, se há suspeita clínica da doença, uma vez que muitos pacientes com doença celíaca podem ter pregas aparentemente normais. A ausência de achados endoscópicos tem baixo valor preditivo para excluir a possibilidade de doença celíaca em populações de baixo risco. [64,70].
5.4.2 Biopsia intestinal e histologia
A combinação de anomalias vilositárias observadas nas biopsias intestinais, juntamente com um teste sorológico positivo, é o critério diagnóstico padrão ouro para a doença celíaca. Uma classificação de Marsh modificada para anomalias vilositárias, é muito utilizada hoje em dia para avaliar a gravidade da atrofia vilositária na prática clínica. [63,72,73].
Embora as alterações histológicas observadas na doença celíaca sejam consideradas características, elas não são patognomônicas, porque alterações semelhantes podem ser observadas em várias outras afecções, como espru tropical, infecção parasitária, imunodeficiência comum variável, enteropatia pelo vírus da imunodeficiência humana (VIH) e drogas e enteropatia induzida por alergia alimentar (como o leite de vaca).
A doença celíaca afeta predominantemente a mucosa do intestino delgado proximal, com danos diminuindo gradualmente em intensidade em direção ao intestino delgado distal, embora em casos graves as lesões possam se estender para áreas mais distais [20].
As lesões no duodeno/jejuno superior podem ser irregulares, e podem passar desapercebidas se a amostragem da mucosa for insuficiente. Devem ser tomadas quatro a seis amostras de biopsia [3] da segunda parte do duodeno e do bulbo duodenal. Em pacientes com doença celíaca ultracurta, a anatomia patológica pode se limitar ao bulbo duodenal, o que ressalta a importância das biopsias nessa área [74]. As biopsias devem ser tomadas quando os pacientes estão em dieta contendo glúten (pelo menos 3g de glúten por dia durante 2 semanas) [75]. Um diagnóstico histológico negativo pode justificar uma segunda biopsia em pacientes selecionados com anticorpos positivos, como anticorpos anti-tTG, anti-DGP e/ou endomísio elevados.
As amostras para biopsia tomadas do duodeno proximal, acima da ampola de Vater, podem apresentar artefatos (por exemplo, estiramento das vilosidades) produzidos pelas glândulas submucosas de Brunner, que podem ser interpretadas falsamente como mucosa plana.
Sob microscopia óptica, os achados histológicos mais característicos [20] em pacientes com doença celíaca que estão ingerindo glúten são:
- Maior densidade de linfócitos intraepiteliais (> 25/100 células epiteliais)
- Hiperplasia das criptas, com diminuição da relação vilosidade/cripta
- Vilosidades aplainadas ou atrofiadas
- Infiltração de células mononucleares na lâmina própria
- Alterações epiteliais, incluindo anomalias estruturais nas células epiteliais
É altamente recomendado que o relatório do patologista descreva as alterações seguindo um formato estruturado incluindo as histológicas acima mencionadas, contagem de linfócitos intraepiteliais e interpretação em termos da classificação de Marsh modificada. Os patologistas também devem comentar a qualidade das biopsias. Se as biopsias são de baixa qualidade, com pequenos fragmentos não orientados, o patologista deve abster-se de fazer um diagnóstico. Nestes casos, a endoscopia com biopsias múltiplas deve ser repetida antes da restrição do glúten.
Uma série de estudos bem elaborados por Marsh [20] permitiud interpretar a ampla gama de danos na mucosa induzidos pelo glúten, com as alterações histológicas celíacas variando de mucosa normal até atrofia vilositária subtotal/total em pacientes com doença celíaca. A classificação de Marsh modificada é muito utilizada na prática clínica [73,76]. Outra classificação mais simples foi proposta para minimizar a variabilidade intraobservador [77].

5.5 Testes de anticorpos séricos
Dois grupos principais de marcadores sorológicos doença celíaca não tratada demonstraram ser altamente sensíveis e específicos: [78,79]:
- Autoanticorpos dirigidos contra autoantígeno
— Anticorpos antiendomísio (AAE) e antitransglutaminase tecidual (anti-tTG)
- Anticorpos dirigidos contra agente agressor (gliadina)
— Anticorpos contra peptídeos de gliadina deaminados sintéticos (anti-DGPs)
Todos esses anticorpos são baseados na imunoglobulina A (IgA) ou imunoglobulina G (IgG). Especificamente, os testes baseados em IgG são úteis para detectar a doença celíaca em pacientes selecionados com deficiência de IgA.
- Pacientes com baixo título de anticorpos e mucosa intestinal normal podem ter um teste falso positivo O teste sorológico deve ser repetido após 6 meses quando o paciente estiver ingerindo uma dieta contendo glúten. Se o teste tornar negativo, isso pode ser considerado como uma soropositividade transitória. Existem poucos dados sobre o seguimento desses pacientes a longo prazo.
- Se a sorologia permanecer positiva, esses pacientes podem ter doença celíaca potencial e devem ser controlados e a biopsia original revisada. A maioria dos pacientes com doença celíaca potencial desenvolvem mais tarde a doença.
- Também, 30% dos pacientes com dermatite herpetiforme com achados sorológicos positivos têm histologia normal. No entanto, é recomendada uma DSG/ddf mesmo com histologia negativa, pois restaura a sorologia positiva e as lesões cutâneas.
- As pessoas assintomáticas com títulos justo no nível de corte (limite) devem voltar a fazer o teste após 3-6 meses com uma dieta normal (sem restrição nem redução do glúten). Os indivíduos sintomáticos com sorologia limite devem se submeter a uma biopsia de todos modos, possivelmente após aumentar a quantidade de glúten em sua dieta.
- Os testes de anticorpos contra a gliadina nativa (AGA-IgA ou AGA-IgG) não são sensíveis nem específicos para a doença celíaca e não devem ser usados [62].
- Os testes para medir os anticorpos celíacos específicos em fezes, urina e saliva têm um desempenho inferior aos testes sanguíneos e não devem ser usados na prática clínica.
5.5.1 IgA AAE
Os anticorpos endomísio IgA se unem ao endomísio, o tecido conjuntivo localizado ao redor do músculo liso, produzindo um padrão de coloração característico que pode ser visualizado com imunofluorescência indireta [80]. Os testes devem ser titulados, se possível; os títulos séricos positivos de anticorpos endomísio IgA no soro, mesmo baixos, são específicos da doença celíaca. O teste é caro, depende do observador, exige muita mão-de-obra e um especialista para fazer uma interpretação correta. O antígeno alvo foi identificado como transglutaminase-2 tecidual. O teste do anticorpo endomísio IgA é moderadamente sensível (cerca de 80%) e tem a maior especificidade de todos os testes específicos para doença celíaca (com cerca de 100% de especificidade, se realizado por operadores experientes) para doença celíaca não tratada (ativa) [62,78].
5.5.2 IgA anti-tTG
Os anticorpos anti-tTG são muito sensíveis e específicos para o diagnóstico da doença celíaca [81]. Os testes de ensaio de imunoabsorção ligado à enzima (ELISA) para anticorpos IgA anti-tTG são muito utilizados na prática clínica atual. Eles estão amplamente disponíveis e são simples de executar; a interpretação dos resultados depende menos do observador e são menos caros do que o ensaio de imunofluorescência necessário para detectar anticorpos anti endomísio IgA [78,79]. Curiosamente, tTG tem como alvo o mesmo autoantígeno (tTG) que AAE. A precisão diagnóstica dos ensaios de IgA anti-tTG foi melhorada com o uso de tTG humana em vez das preparações tTG não humanas (com pior precisão diagnóstica) usadas em kits de imunoensaio anteriores. Embora os anticorpos anti-tTG sejam utilizados em todo o mundo, ainda existem diferenças substanciais no desempenho de diferentes kits comerciais [79].
5.5.3 Anticorpos IgA e IgG anti-DGP
Um ELISA baseado na detecção de peptídeos de gliadina deaminados (DGPs) desenvolvidos de forma sintética foi introduzido há alguns anos, e a pesquisa clínica mostrou que este ensaio tem um nível muito elevado de precisão diagnóstica em populações de alto e baixo risco. Isso foi confirmado em estudos recentes [82].
Os anti-DGP de classe IgG têm melhores resultados do que os testes DGP baseados em IgA para diagnosticar a doença celíaca [82–84].
5.5.4 Escolha do teste sorológico mais adequado em diferentes contextos clínicos
Os testes sorológicos específicos para a doença celíaca são importantes para os dois propósitos a seguir [78,85]:
1. Confirmar a dependência do glúten em pacientes com enteropatia (diagnóstico).
- IgA AAE, IgA anti-tTG, e IgG anti-DGP e IgA têm desempenho semelhante, oferecendo os substitutos mais valiosos para a dependência do glúten.
- Os testes baseados em IgG (anti-DGP, AAE e tTG) parecem ser muito úteis em pacientes com deficiência de IgA negativos para os testes baseados em IgA.
2. Selecionar os pacientes para a biopsia duodenal
Para reduzir a necessidade de biopsias duodenais e considerando a diferente precisão dos testes sorológicos, uma série de algoritmos sorológicos é usada para selecionar os pacientes para biopsia em diferentes contextos clínicos.
Escolha do teste sorológico para triagem da população geral:
- O IgA anti-tTG, combinado com IgA total e um teste baseado em IgG (naqueles indivíduos com deficiência de IgA) constitui o algoritmo de primeira linha mais utilizado para a triagem, graças a sua alta sensibilidade e ótima especificidade.
- O valor preditivo positivo em populações de baixo risco depende do nível de titulação [86,87]. Os indivíduos assintomáticos com títulos baixos (por exemplo, menos de três vezes os valores de corte) devem ser testados novamente após 3-6 meses de uma dieta com alto teor de glúten antes de considerar a endoscopia e as biopsias.
- Um algoritmo sorológico, com ensaios seriados de triagem mais específicos (por exemplo, AAE) foi muito utilizado para melhorar a precisão diagnóstica na população geral [86,88].
- Uma combinação de testes pode melhorar a detecção de casos. Se os testes forem simultaneamente positivos, a doença celíaca será o diagnóstico mais provável [85,89,90].
O teste AAE requer observadores experientes. Os testes baseados em ELISA / radioimunoensaio para a detecção de IgA anti-tTG ou IgG anti-DGP devem, portanto, ser recomendados em lugares com pouca experiência.
5.6 Determinação de genótipos HLA-DQ2/-DQ8
A determinação do genótipo HLA-DQ2/-DQ8 pode ser importante no diagnóstico de doenças soronegativas e para excluir a doença celíaca antes de iniciar uma provocação formal com glúten.
5.7 Dieta presuntiva sem glúten
Em algumas áreas geográficas, como na África intertropical, onde as instalações de diagnóstico são insuficientes ou inacessíveis, uma dieta presuntiva sem glúten pode ser uma ferramenta diagnóstica indireta, se a melhoria clínica for radical [29]. Como tal, é fácil introduzir em muitas áreas da África um tratamento de baixo custo e sem risco. A principal dificuldade é convencer os pais a introduzir uma dieta na criança desnutrida e, especialmente, a duração da dieta ao longo da vida (embora essa dificuldade não seja específica dos trópicos).
Embora essa estratégia seja relevante em áreas isoladas, onde pode ser a única maneira de confirmar e tratar a doença celíaca, é altamente recomendável que ela seja aplicada nos locais onde a sorologia estiver disponível.
Em todas as pessoas que iniciam uma dieta sem glúten (por qualquer motivo, por exemplo, alergia ao trigo, estilo de vida, SII), é obrigatório excluir a doença celíaca mediante um teste negativo para anticorpos celíacos específicos antes de iniciar a dieta.
5.8 Diagnóstico diferencial
As manifestações clínicas da doença celíaca são variadas e elas podem imitar os conjuntos de sintomas de muitas outras doenças gastrointestinais. Além disso, as lesões histológicas sugestivas de doença celíaca também estão presentes em muitas outras afecções, tais como:
- Espru tropical
- Estados de imunodeficiência combinada
- Giardíase
- Enteropatia induzida por fármacos (olmesartan, micofenolato)
- Enteropatia pelo HIV
- Dano por radiação
- Quimioterapia recente
- Doença do enxerto contra hospedeiro
- Isquemia crônica
- Cólera
- Doença de Crohn
- Infecção pela Helicobacter pylori
- Gastroenterite eosinofílica
- Enteropatia causada por alergia alimentar (em crianças pequenas)
- Enteropatia autoimune
- Desnutrição severa
5.9 Por que deve ser detectada a doença celíaca?
A introdução de uma DSG nos pacientes com doença celíaca sintomática pode melhorar de forma significativa os sintomas, os parâmetros bioquímicos anormais e a qualidade de vida [91]. O tratamento ao longo da vida também reduz o risco de complicações malignas e não malignas. Segue havendo preocupação sobre as consequências a longo prazo nos pacientes assintomáticos, e se manter uma DSG durante toda a vida é necessário para todos os pacientes. Vários estudos sugerem que os pacientes que têm a doença detectada durante a triagem, a maioria dos quais pode ser assintomática, podem melhorar sua qualidade de vida a longo prazo com uma DSG [92,93].
Os pacientes com doença celíaca (não tratada a longo prazo) têm risco elevado de complicações benignas e malignas, e de mortalidade [64,94,95].
- Câncer — maior risco nos primeiros anos após o diagnóstico – diminui para risco (quase) normal no quinto ano [96]; o incremento geral do risco é 1,35
- Linfomas malignos
- Adenocarcinoma do intestino delgado
- Tumores orofaríngeos
- Infertilidade inexplicada (12%)
- Saúde e crescimento dos ossos prejudicados (osteoporose 30-40%)
- Fraturas ósseas: risco aumentado 35% para pacientes com DC sintomática clássica [97,98]
- O risco de mortalidade é elevado em pacientes celíacos adultos, devido a um maior risco de neoplasia fatal (índice de risco, 1,31; intervalos de confiança de 95%: 1,13 a 1,51 em um estudo) [64]
- Resultado adverso da gravidez [99]
O único tratamento para a doença celíaca, hoje, é uma dieta estritamente livre de glúten por toda a vida [20,66,100,101]. Nenhum alimento ou medicamento contendo glúten de trigo, centeio e cevada ou derivados pode ser ingerido. Pequenas quantidades de glúten podem ser prejudiciais.
- Eliminação do glúten (redução a <20 mg/dia de glúten) da dieta dos pacientes celíacos leva a uma remissão sintomática, sorológica e histológica na maioria dos pacientes [84,93].
- Aproximadamente 70% dos pacientes relata uma melhoria dos sintomas nas 2 semanas posteriores ao início da dieta sem glúten [93].
- Crescimento e desenvolvimento das crianças se normalizam com adesão à dieta sem glúten. Muitas complicações podem ser prevenidas com dieta sem glúten [102,103].
- Com controle dietético estrito, os títulos dos anticorpos específicos da doença celíaca se normalizam.
- Embora as alterações vilositárias comecem a melhorar nos meses posteriores ao início da dieta sem glúten, a resolução histológica completa pode levar anos e pode não ser alcançada em todos os pacientes [104,105]. Existe evidência de que a falta de resolução histológica pode depender do consumo persistente de glúten [64].
O limite seguro de ingestão de glúten varia de paciente para paciente e foi considerado de 10 a 100 mg/dia, embora um estudo recente tenha indicado que o limite superior não deveria ser maior a 50 mg/dia [106].
- Aveia pura e não contaminada não é tóxica em mais de 95% dos pacientes com doença celíaca e foi utilizada como parte das DSG em alguns países (como a Finlândia) em adultos e crianças durante mais de 15 anos sem um risco aumentado de enteropatia. Há um subgrupo muito pequeno (<5%) para os quais a aveia não é segura [107,108]. Em alguns países há relutância em recomendar o uso liberal da aveia, por causa das dificuldades em garantir que a aveia comercialmente disponível não esteja contaminada com outros grãos. Portanto, é possível recomendar uma dieta sem aveia, pelo menos durante os primeiros meses de tratamento.
- Arroz e milho podem ser incluídos na dieta sem glúten.
Embora a maioria dos pacientes tenha uma resposta clínica rápida a uma dieta sem glúten, a velocidade da resposta varia. Os pacientes graves podem requerer hospitalização, reposição de líquidos e eletrólitos, nutrição intravenosa, ferro, vitaminas e, às vezes, corticoides [109].
Os pacientes devem ser encorajados a ingerir alimentos naturais ricos em ferro e folato, especialmente se houver deficiência comprovada destes minerais. Os pacientes devem consultar um/a nutricionista conhecedor/a das dietas sem glúten, especialmente durante o primeiro ano após o diagnóstico. Nem todos os nutricionistas estão familiarizados com a complexidade de uma dieta sem glúten, e os grupos de apoio locais ou nacionais, em geral, podem oferecer a maior parte da informação necessária.
O apoio ao paciente e a educação no momento do diagnóstico são muito importantes e devem fazer parte do tratamento [110].
Adolescentes com doença celíaca devem passar por um processo de transição formal, com educação e uma transferência estruturada para o sistema de cuidados de adultos [111].
6.1 Recomendações após o diagnóstico
No seguimento da doença celíaca, é importante considerar as seguintes recomendações para avaliar a DSG:
- Os testes sorológicos não podem detectar a ingestão mínima de glúten (traços), portanto, uma abordagem interdisciplinar é necessária para uma avaliação detalhada da situação clínica e da DSG. Essa avaliação deve ser feita por médicos especialistas e nutricionistas [93,112].
- A necessidade de repetidas biópsias duodenais para avaliar a cicatrização e avaliar a adesão a uma GFD é um assunto controverso entre os especialistas. Embora essa abordagem seja frequentemente usada na prática, não está claro se é necessário que os pacientes que respondem clinicamente à DCG tenham níveis negativos ou reduzidos de anticorpos Entre os especialistas que recomendam repetir as biopsias, não está bem definido qual é o melhor momento para obter as amostras. A cicatrização completa da mucosa intestinal também é frequentemente lenta ou incompleta, especialmente em adultos. As biopsias intestinais devem ser consideradas obrigatórias em pacientes com sintomas persistentes apesar da evidência de uma DSG estrita.
- A causa mais provável em pacientes que não respondem ao tratamento é o consumo contínuo de quantidades elevadas de glúten, ou de traços de glúten (intencionais ou despercebidos) [108,113,114].
A seguir, um resumo das recomendações para seguimento após diagnóstico e ferramentas para monitorar a adesão a uma dieta sem glúten [9] durante o primeiro ano após o diagnóstico:
Avaliação clínica: verificar sintomas e fazer exames laboratoriais (como hemograma completo, estado do ferro, vitamina B12, sorologia celíaca, cálcio, vitamina D) e testes sorológicos para doença celíaca (os melhores preditores até agora: determinação quantitativa de IgA anti-tTG e IgA anti-DGP) [84,104,115].
- Crianças e adolescentes devem ser monitorados anualmente (antropometria, desenvolvimento puberal, sorologia celíaca específica) por um pediatra ou gastroenterologista pediátrico até alcançarem sua altura final.
- A densitometria óssea pode ser feita para ter um valor de referência da massa óssea [116].
- Vacinação contra pneumococos, Haemophilus influenzae, meningococos [117].
- Consulta com nutricionista: avaliação do estado nutricional e da adesão a uma dieta livre de glúten com base em entrevista, diário de alimentação e frequência do consumo (coincidindo com controle médico na visita clínica).
- O paciente deve ser ajudado a participar de grupos de apoio com experiência comprovada em doença celíaca; os níveis de adesão à dieta sem glúten estão associados à participação em grupos de apoio e acompanhamento nutricional regular [118,119].
- Se for necessário e/ou solicitado, deve ser oferecida uma consulta psicológica [120].
6.2 Dieta sem glúten
6.2.1 Alimentos não permitidos na dieta sem glúten
Grãos, amidos e farinha não permitidos em dietas sem glúten [101,121]:
- Cevada
- Farelo
- Bulgur
- Cuscuz
- Farinha durum
- Einkorn (Triticum monococcum)*
- Emmer (Triticum dicoccum)*
- Faro*
- Glúten, farinha de glúten
- Farinha de Graham
- Kamut™ (trigo Khorasan)*
- Malte, extrato de malte, aromatizante de malte, xarope de malte
- Aveia, farelo de aveia, xarope de aveia - não rotulado como livre de glúten
- Centeio
- Sêmola (trigo duro) *
- Espelta (trigo dinkel, Triticum spelta)
- Triticale
- Germe de trigo, amido de trigo, farelo de trigo
- Qualquer produto com trigo, cevada ou centeio
* Variedades de trigo
Aveia pura sem contaminar está disponível em alguns países, mas permitida em determinada quantidade. Embora muitos estudos indiquem que os pacientes com doença celíaca podem consumir aveia sem problemas em quantidades moderadas, existe preocupação pela possível contaminação da aveia com trigo e cevada na fase de processamento dos cereais.
6.2.2 Alimentos permitidos na dieta sem glúten
Grãos, farinhas e amidos sem glúten permitidos na dieta livre de glúten:
- Amaranto
- Araruta
- Farinhas de feijão
- Trigo sarraceno
- Milho
- Grão de bico
- Sementes
- Painço
- Farinha Montina (arroz indiano)
- Farinha de frutos secos
- Aveia (não contaminada, etiquetada como livre de glúten)
- Farinha de batata, amido de batata
- Quinoa
- Arroz, todas as formas (integral ou moreno, branco, doce, silvestre, jasmine, basmati, arroz glutinoso, arroz polido, farelo de arroz)
- Farinha de sorgo
- Farinha de soja
- Tapioca
- Farinha de Teff
Embora esses cereais, farinhas e amidos sem glúten sejam permitidos na DSG, pode haver problemas com a contaminação cruzada com trigo e cevada. Portanto, é preciso analisar os amidos e farinhas para uma detecção preliminar de glúten antes de permitir seu uso na dieta dos pacientes celíacos. Alguns países publicam periodicamente listas atualizadas de produtos sem glúten na internet. Os alimentos na lista foram analisados para detectar o teor de glúten [122,123].
6.2.3 Outros alimentos para uma dieta básica sem glúten
- Laticínios
- Todas as carnes frescas e em conserva sem glúten.
- Mariscos
- Ovos
- Legumes secos: lentilhas, grão de bico, ervilhas, feijão, nozes, sementes: envasadas, não soltas
- Frutas (frescas, congeladas, enlatadas) e sucos naturais.
- Legumes (frescos, congelados, enlatados) e sucos de vegetais simples.
- Óleos vegetais líquidos.
6.2.4 Artigos vários permitidos na dieta sem glúten
- Doces: mel, xarope de milho, açúcar (mascavo e branco)
- Lanches: pipoca, nozes (frutos secos), picles, azeitonas, batatas fritas sem glúten (batatinhas fritas)
- Condimentos: ervas naturais, pimenta-do-reino negra pura, vinagres (maçã, uva ou vinho)
Cozimento e preparação de alimentos: os pacientes devem ser instruídos a não contaminar alimentos sem glúten, por exemplo, usando utensílios de cozinha, superfícies de cozimento e torradeiras separados.
A maioria dos alimentos produzidos industrialmente contêm ingredientes não permitidos. É importante prestar atenção ao rotulado e conferir quais alimentos estão permitidos nas listas disponíveis. É muito importante poder integrar um grupo de apoio.
A dieta sem glúten é pobre em fibras. Os pacientes devem ser aconselhados a ingerir uma dieta rica em fibra complementada com arroz integral, milho, batata e abundantes vegetais. Qualquer deficiência dietética como ferro, ácido fólico, cálcio e (muito raramente) vitamina B12 deve ser corrigida.
6.3 Prevenção — triagem
Atualmente, não existem medidas definitivas para a prevenção primária da doença celíaca com base no tempo de introdução do glúten para lactentes ou na duração da amamentação. Ensaios controlados randomizados falharam em induzir a tolerância administrando pequenas quantidades de glúten [48] ou retrasando a introdução do glúten até depois dos 12 meses de idade [49]. Ainda se discute se a quantidade de glúten administrada é importante [51,124,125]. A detecção precoce e o tratamento são os métodos mais válidos para a prevenção secundária da doença celíaca [126].
No debate sobre como melhorar a detecção dos transtornos relacionados ao glúten, alguns recomendam mudar de um caso de alto risco para uma política ativa de testes sorológicos da doença celíaca na população geral [68,127].
6.4 Novas opções de tratamento
Como os passos envolvidos na imunopatogênese da doença celíaca têm sido gradualmente desvendados, muitos alvos imunopatogenéticos estão sendo explorados para tratamentos alternativos/adjuntos, como a digestão intraluminal de glúten, a melhora nas funções de barreira e os imunomoduladores. Muitas das novas opções atingiram a fase dos ensaios clínicos, mas nenhuma delas está disponível ainda para uso clínico.
6.5 Seguimento
6.5.1 Avaliação de laboratório
A sorologia celíaca pode ser útil, mas a diminuição das concentrações de anticorpos celíacos específicos indica redução do glúten e têm capacidade limitada para definir a adesão completa. Uma vez que os anticorpos tenham se normalizado, um subsequente aumento no nível é considerado um bom indicador da ingestão de glúten. A medida definitiva de adesão é a demonstração da cicatrização intestinal, mas isso pode não ocorrer inclusive em pacientes que evitarem estritamente o glúten.
Intervalo de avaliação: a cada 3-6 meses, até que os exames basais anormais sejam corrigidos ou até a estabilização clínica; depois, a cada 1-2 anos.
- Estudos recentes sugerem que a realização de testes periódicos para IgA anti-tTG ou IgA anti-DGP constitui o método preferido para monitorar a adesão.
- Embora estes testes não identifiquem indiscrições dietéticas secundárias - os títulos normais são insensíveis à exposição contínua ao glúten ou à enteropatia - uma redução contínua nas concentrações séricas ajuda a avaliar a adesão à dieta.
- Os títulos limítrofes persistentes, elevados ou crescentes, indicam exposição significativa ao glúten [64].
6.5.2 Consulta com nutricionista
Frequência: idealmente a cada 3-6 meses até normalização clínica; depois, a cada 1-2 anos. Isto é especialmente importante em mulheres em idade fértil e durante a gravidez. Um nutricionista especializado deve ser consultado para:
- Avaliar o estado nutricional atual do paciente.
- Identificar a ingestão de macronutrientes e/ou micronutrientes e detectar deficiências e/ou excessos.
- É importante que os pacientes com doença celíaca consultem um especialista e que consumam uma dieta balanceada incluindo vitaminas, cálcio e fibras.
- Analisar hábitos alimentares e possíveis fatores que afetam o acesso à dieta.
- Fornecer informação e iniciar a dieta sem glúten.
- Fornecer educação sobre a dieta.
- Fazer seguimento e avaliar a adesão à dieta e reforçar a orientação nutricional.
Os pacientes que não conseguem aderir à dieta podem precisar de apoio com ajuda psicológica.
6.5.3 Persistência dos sintomas
A persistência dos sintomas quase sempre é provocada pela ingestão contínua de glúten. Uma dificuldade comum com a dieta sem glúten é a contaminação cruzada e a presença de glúten suspeitado nos alimentos processados e/ou medicamentos. O glúten é amplamente usado em alimentos processados; pode ser um ingrediente oculto, por isso, é prudente que os pacientes verifiquem sempre a lista de ingredientes antes de comprar os produtos. Se a resposta a uma dieta sem glúten for subótima, a ingestão intencional ou inadvertida de glúten deve ser considerada. Nestes casos, a persistência de sorologia positiva pode identificar intervalos importantes e contínuos na adesão à dieta.
Lista de causas de persistência dos sintomas em pacientes com doença celíaca:
- Síndrome do intestino irritável, sobreposta ou ingestão inadvertida de glúten (causas mais comuns)
- Diagnóstico errado
- Intolerância primária à lactose
- Alergias alimentares que não sejam trigo
- Insuficiência pancreática
- Colite microscópica
- Supercrescimento bacteriano
- Doença intestinal inflamatória
- Jejunite ulcerativa*
- Linfoma de células T associado a enteropatia*
- Doença celíaca refratária*
* As três últimas podem ser consideradas complicações de doença celíaca prolongada
6.6 Transferência de cuidados desde a infância até a idade adulta
Adolescentes/jovens adultos com doença celíaca correm o risco de abandono “médico” antes e durante a transferência para o sistema de cuidados de saúde de adultos [128,129]. Em geral, os adultos com doença celíaca estão acostumados a cuidar de sua dieta e aprendem rapidamente o que podem comer. No entanto, os adolescentes geralmente ainda são ajudados pelos pais e cuidadores e podem não ser autônomos em lidar com a doença. Não existem diretrizes precisas para preencher a lacuna entre os serviços pediátrico e adulto para a doença celíaca, e agora o que é recomendado é dar uma atenção médica de transição. A clínica de transição deve se concentrar na educação (problemas dietéticos e de saúde), na necessidade de monitorar a doença além de lidar com os problemas psicológicos que possam surgir [111].
6.7 Doença celíaca refratária
A doença celíaca refratária é definida como a persistência (ou recorrência) de sintomas clínicos e anomalias histopatológicas associadas a sintomas clínicos, apesar da excelente adesão à DSG durante pelo menos 12 meses [108]. Isto pode ocorrer na apresentação (primária) ou após uma resposta inicial à dieta sem glúten (secundária) [130]. A doença celíaca refratária deve ser considerada especialmente em pacientes celíacos diagnosticados após os 50 anos.
Há dois subtipos de doença celíaca refratária:
- Tipo I, com linfócitos intraepiteliais fenotipicamente normais
- Tipo II, com expansão clonal de linfócitos intraepiteliais e um fenótipo aberrante com déficit de receptores de células CD3, CD8 e células T de superfície
A doença de tipo II é considerada uma forma de linfoma intraepitelial de baixo grau, revelada por má absorção severa que não responde à dieta sem glúten. Esta é a forma mais grave e está associada a uma alta taxa de mortalidade [].
7.1 Abreviações

7.2 Diretrizes padrão ouro
- 2016:
Transition from childhood to adulthood in coeliac disease: the Prague consensus report. (Transição da infância para a idade adulta na doença celíaca: relatório de consenso de Praga). Ludvigsson et al. Gut 2016;65:1242–51 [111].
- 2014:
Diagnosis and management of adult coeliac disease: guidelines from the British Society of Gastroenterology. (Diagnóstico e tratamento da doença celíaca em adultos: diretrizes da Sociedade Británica de Gastroenterologia). Ludvigsson et al. Gut 2014;63:1210–28 [63].
- 2013:
ACG clinical guidelines: diagnosis and management of celiac disease. (Diretrizes clínicas da ACG: diagnóstico e manejo da doença celíaca). Rubio-Tapia et al. Am J Gastroenterol 2013;108:656–76; quiz 677. doi: 10.1038/ajg.2013.79 [132].
- 2012:
European Society for Pediatric Gastroenterology, Hepatology, and Nutrition guidelines for the diagnosis of coeliac disease. (Diretrizes para o diagnóstico da doença celíaca da Sociedade Europeia de Gastroenterologia, Hepatologia e Nutrição Pediátrica). Husby et al. J Pediatr Gastroenterol Nutr 2012;54:136–60 [87].
- 2005:
Guideline for the diagnosis and treatment of celiac disease in children: recommendations of the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition. (Diretriz para o diagnóstico e tratamento da doença celíaca em crianças: recomendações da Sociedade Norteamericana de Gastroenterologia, Hepatologia e Nutrição Pediátrica). Hill et al. J Pediatr Gastroenterol Nutr 2005;40:1–19 [67].
7.3 Referências
1. Stern M, Ciclitira PJ, van Eckert R, Feighery C, Janssen FW, Méndez E, et al. Analysis and clinical effects of gluten in coeliac disease. Eur J Gastroenterol Hepatol 2001;13(6):741–7.
2. Jabri B, Sollid LM. Mechanisms of disease: immunopathogenesis of celiac disease. Nat Clin Pract Gastroenterol Hepatol 2006;3(9):516–25.
3. Ludvigsson JF, Leffler DA, Bai JC, Biagi F, Fasano A, Green PHR, et al. The Oslo definitions for coeliac disease and related terms. Gut 2013;62(1):43–52.
4. Cianferoni A. Wheat allergy: diagnosis and management. J Asthma Allergy 2016;13.
5. Sapone A, Bai JC, Ciacci C, Dolinsek J, Green PHR, Hadjivassiliou M, et al. Spectrum of gluten-related disorders: consensus on new nomenclature and classification. BMC Med 2012;10:13.
6. Carroccio A, Mansueto P, Iacono G, Soresi M, D’Alcamo A, Cavataio F, et al. Non-celiac wheat sensitivity diagnosed by double-blind placebo-controlled challenge: exploring a new clinical entity. Am J Gastroenterol 2012;107(12):1898–906.
7. Biesiekierski JR, Newnham ED, Irving PM, Barrett JS, Haines M, Doecke JD, et al. Gluten causes gastrointestinal symptoms in subjects without celiac disease: a double-blind randomized placebo-controlled trial. Am J Gastroenterol 2011;106(3):508–14.
8. Biesiekierski JR, Peters SL, Newnham ED, Rosella O, Muir JG, Gibson PR. No effects of gluten in patients with self-reported non-celiac gluten sensitivity after dietary reduction of fermentable, poorly absorbed, short-chain carbohydrates. Gastroenterology 2013;145(2):320–328.e3.
9. Di Sabatino A, Volta U, Salvatore C, Biancheri P, Caio G, De Giorgio R, et al. Small amounts of gluten in subjects with suspected nonceliac gluten sensitivity: a randomized, double-blind, placebo-controlled, cross-over trial. Clin Gastroenterol Hepatol 2015;13(9):1604–1612.e3.
10. Shahbazkhani B, Sadeghi A, Malekzadeh R, Khatavi F, Etemadi M, Kalantri E, et al. Non-celiac gluten sensitivity has narrowed the spectrum of irritable bowel syndrome: a double-blind randomized placebo-controlled trial. Nutrients 2015;7(6):4542–54.
11. Carroccio A, D’Alcamo A, Mansueto P. Nonceliac wheat sensitivity in the context of multiple food hypersensitivity: new data from confocal endomicroscopy. Gastroenterology 2015;148(3):666–7.
12. Guandalini S, Polanco I. Nonceliac gluten sensitivity or wheat intolerance syndrome? J Pediatr 2015;166(4):805–11.
13. Lohi S, Mustalahti K, Kaukinen K, Laurila K, Collin P, Rissanen H, et al. Increasing prevalence of coeliac disease over time. Aliment Pharmacol Ther 2007;26(9):1217–25.
14. Choung RS, Ditah IC, Nadeau AM, Rubio-Tapia A, Marietta EV, Brantner TL, et al. Trends and racial/ethnic disparities in gluten-sensitive problems in the United States: findings from the National Health and Nutrition Examination Surveys from 1988 to 2012. Am J Gastroenterol 2015;110(3):455–61.
15. Fasano A, Catassi C. Current approaches to diagnosis and treatment of celiac disease: an evolving spectrum. Gastroenterology 2001;120(3):636–51.
16. Fasano A, Berti I, Gerarduzzi T, Not T, Colletti RB, Drago S, et al. Prevalence of celiac disease in at-risk and not-at-risk groups in the United States: a large multicenter study. Arch Intern Med 2003;163(3):286–92.
17. Lionetti E, Catassi C. New clues in celiac disease epidemiology, pathogenesis, clinical manifestations, and treatment. Int Rev Immunol 2011;30(4):219–31.
18. Tortora R, Zingone F, Rispo A, Bucci C, Capone P, Imperatore N, et al. Coeliac disease in the elderly in a tertiary centre. Scand J Gastroenterol 2016;51(10):1179–83.
19. Smecuol E, Mauriño E, Vazquez H, Pedreira S, Niveloni S, Mazure R, et al. Gynaecological and obstetric disorders in coeliac disease: frequent clinical onset during pregnancy or the puerperium. Eur J Gastroenterol Hepatol 1996;8(1):63–89.
20. Marsh MN. Gluten, major histocompatibility complex, and the small intestine. A molecular and immunobiologic approach to the spectrum of gluten sensitivity (“celiac sprue”). Gastroenterology 1992;102(1):330–54.
21. Gomez JC, Selvaggio GS, Viola M, Pizarro B, la Motta G, de Barrio S, et al. Prevalence of celiac disease in Argentina: screening of an adult population in the La Plata area. Am J Gastroenterol 2001;96(9):2700–4.
22. Gandolfi L, Pratesi R, Cordoba JC, Tauil PL, Gasparin M, Catassi C. Prevalence of celiac disease among blood donors in Brazil. Am J Gastroenterol 2000;95(3):689–92.
23. Parada A, Araya M, Pérez-Bravo F, Méndez M, Mimbacas A, Motta P, et al. Amerindian mtDNA haplogroups and celiac disease risk HLA haplotypes in mixed-blood Latin American patients. J Pediatr Gastroenterol Nutr 2011;53(4):429–34.
24. Barada K, Abu Daya H, Rostami K, Catassi C. Celiac disease in the developing world. Gastrointest Endosc Clin N Am 2012;22(4):773–96.
25. Brar P, Lee AR, Lewis SK, Bhagat G, Green PHR. Celiac disease in African-Americans. Dig Dis Sci 2006;51(5):1012–5.
26. Catassi C, Rätsch IM, Gandolfi L, Pratesi R, Fabiani E, El Asmar R, et al. Why is coeliac disease endemic in the people of the Sahara? Lancet 1999;354(9179):647–8.
27. Sood A, Midha V, Sood N, Avasthi G, Sehgal A. Prevalence of celiac disease among school children in Punjab, North India. J Gastroenterol Hepatol 2006;21(10):1622–5.
28. Aziz S, Muzaffar R, Zafar MN, Mehnaz A, Mubarak M, Abbas Z, et al. Celiac disease in children with persistent diarrhea and failure to thrive. J Coll Physicians Surg Pak 2007;17(9):554–7.
29. Diallo I, Coton T. Celiac disease: a challenging disease uneasy to diagnose in Sub-Saharan Africa. J Gastroenterol Hepatol Res [Internet] 2013;2(8):753–6. Available at: http://www.ghrnet.org/index.php/joghr/article/view/459.
30. Ageep AK. Celiac disease in the Red Sea state of Sudan. Trop Gastroenterol 2012;33(2):118–22.
31. Mohammed IM, Karrar ZEA, El-Safi SH. Coeliac disease in Sudanese children with clinical features suggestive of the disease. East Mediterr Health J 2006;12(5):582–9.
32. Wu J, Xia B, von Blomberg BME, Zhao C, Yang XW, Crusius JBA, et al. Coeliac disease: emerging in China? Gut 2010;59(3):418–9.
33. Singh P, Arora S, Singh A, Strand TA, Makharia GK. Prevalence of celiac disease in Asia: a systematic review and meta-analysis. J Gastroenterol Hepatol 2016;31(6):1095–101.
34. Vázquez H, de la Paz Temprano M, Sugai E, Scacchi SM, Souza C, Cisterna D, et al. Prevalence of celiac disease and celiac autoimmunity in the Toba native Amerindian community of Argentina. Can J Gastroenterol Hepatol 2015;29(8):431–4.
35. Lionetti E, Gatti S, Pulvirenti A, Catassi C. Celiac disease from a global perspective. Best Pract Res Clin Gastroenterol 2015;29(3):365–79.
36. Catassi C, Kryszak D, Bhatti B, Sturgeon C, Helzlsouer K, Clipp SL, et al. Natural history of celiac disease autoimmunity in a USA cohort followed since 1974. Ann Med 2010;42(7):530–8.
37. Mäki M, Mustalahti K, Kokkonen J, Kulmala P, Haapalahti M, Karttunen T, et al. Prevalence of Celiac disease among children in Finland. N Engl J Med 2003;348(25):2517–24.
38. Green PHR. The many faces of celiac disease: clinical presentation of celiac disease in the adult population. Gastroenterology 2005;128(4 Suppl 1):S74-78.
39. Dickey W, McMillan SA, Hughes DF. Identification of coeliac disease in primary care. Scand J Gastroenterol 1998;33(5):491–3.
40. Collin P, Huhtala H, Virta L, Kekkonen L, Reunala T. Diagnosis of celiac disease in clinical practice: physician’s alertness to the condition essential. J Clin Gastroenterol 2007;41(2):152–6.
41. Rostami-Nejad M, Romanos J, Rostami K, Ganji A, Ehsani-Ardakani MJ, Bakhshipour AR, et al. Allele and haplotype frequencies for HLA-DQ in Iranian celiac disease patients. World J Gastroenterol 2014;20(20):6302–8.
42. Gutierrez-Achury J, Zhernakova A, Pulit SL, Trynka G, Hunt KA, Romanos J, et al. Fine mapping in the MHC region accounts for 18% additional genetic risk for celiac disease. Nat Genet 2015;47(6):577–8.
43. Romanos J, van Diemen CC, Nolte IM, Trynka G, Zhernakova A, Fu J, et al. Analysis of HLA and non-HLA alleles can identify individuals at high risk for celiac disease. Gastroenterology 2009;137(3):834–40, 840–3.
44. Liu E, Lee HS, Aronsson CA, Hagopian WA, Koletzko S, Rewers MJ, et al. Risk of pediatric celiac disease according to HLA haplotype and country. N Engl J Med 2014;371(1):42–9.
45. Polvi A, Arranz E, Fernandez-Arquero M, Collin P, Mäki M, Sanz A, et al. HLA-DQ2-negative celiac disease in Finland and Spain. Hum Immunol 1998;59(3):169–75.
46. Spurkland A, Sollid LM, Polanco I, Vartdal F, Thorsby E. HLA-DR and -DQ genotypes of celiac disease patients serologically typed to be non-DR3 or non-DR5/7. Hum Immunol 1992;35(3):188–92.
47. Abadie V, Sollid LM, Barreiro LB, Jabri B. Integration of genetic and immunological insights into a model of celiac disease pathogenesis. Annu Rev Immunol 2011;29:493–525.
48. Vriezinga SL, Auricchio R, Bravi E, Castillejo G, Chmielewska A, Crespo Escobar P, et al. Randomized feeding intervention in infants at high risk for celiac disease. N Engl J Med 2014;371(14):1304–15.
49. Lionetti E, Castellaneta S, Francavilla R, Pulvirenti A, Tonutti E, Amarri S, et al. Introduction of gluten, HLA status, and the risk of celiac disease in children. N Engl J Med 2014;371(14):1295–303.
50. Aronsson CA, Lee HS, Liu E, Uusitalo U, Hummel S, Yang J, et al. Age at gluten introduction and risk of celiac disease. Pediatrics 2015;135(2):239–45.
51. Andrén Aronsson C, Lee HS, Koletzko S, Uusitalo U, Yang J, Virtanen SM, et al. Effects of gluten intake on risk of celiac disease: a case-control study on a Swedish birth cohort. Clin Gastroenterol Hepatol 2016;14(3):403–409.e3.
52. Szajewska H, Shamir R, Chmielewska A, Pieścik-Lech M, Auricchio R, Ivarsson A, et al. Systematic review with meta-analysis: early infant feeding and coeliac disease—update 2015. Aliment Pharmacol Ther 2015;41(11):1038–54.
53. Ferguson A, Arranz E, O’Mahony S. Clinical and pathological spectrum of coeliac disease—active, silent, latent, potential. Gut 1993;34(2):150–1.
54. Green PHR, Jabri B. Coeliac disease. Lancet 2003;362(9381):383–91.
55. Santonicola A, Iovino P, Cappello C, Capone P, Andreozzi P, Ciacci C. From menarche to menopause: the fertile life span of celiac women. Menopause 2011;18(10):1125–30.
56. Sbai W, Bourgain G, Luciano L, Brardjanian S, Thefenne L, Al Shukry A, et al. Celiac crisis in a multi-trauma adult patient. Clin Res Hepatol Gastroenterol 2016;40(3):e31–2.
57. Korpimäki S, Kaukinen K, Collin P, Haapala A-M, Holm P, Laurila K, et al. Gluten-sensitive hypertransaminasemia in celiac disease: an infrequent and often subclinical finding. Am J Gastroenterol 2011;106(9):1689–96.
58. Nachman F, Mauriño E, Vázquez H, Sfoggia C, Gonzalez A, Gonzalez V, et al. Quality of life in celiac disease patients: prospective analysis on the importance of clinical severity at diagnosis and the impact of treatment. Dig Liver Dis 2009;41(1):15–25.
59. Lindfors K, Koskinen O, Kaukinen K. An update on the diagnostics of celiac disease. Int Rev Immunol 2011;30(4):185–96.
60. Kinos S, Kurppa K, Ukkola A, Collin P, Lähdeaho ML, Huhtala H, et al. Burden of illness in screen-detected children with celiac disease and their families. J Pediatr Gastroenterol Nutr 2012;55(4):412–6.
61. Kurppa K, Paavola A, Collin P, Sievänen H, Laurila K, Huhtala H, et al. Benefits of a gluten-free diet for asymptomatic patients with serologic markers of celiac disease. Gastroenterology 2014;147(3):610–617.e1.
62. Giersiepen K, Lelgemann M, Stuhldreher N, Ronfani L, Husby S, Koletzko S, et al. Accuracy of diagnostic antibody tests for coeliac disease in children: summary of an evidence report. J Pediatr Gastroenterol Nutr 2012;54(2):229–41.
63. Ludvigsson JF, Bai JC, Biagi F, Card TR, Ciacci C, Ciclitira PJ, et al. Diagnosis and management of adult coeliac disease: guidelines from the British Society of Gastroenterology. Gut 2014;63(8):1210–28.
64. Kelly CP, Bai JC, Liu E, Leffler DA. Advances in diagnosis and management of celiac disease. Gastroenterology 2015;148(6):1175–86.
65. Catassi C, Fasano A. Celiac disease diagnosis: simple rules are better than complicated algorithms. Am J Med 2010;123(8):691–3.
66. Ciclitira PJ, King AL, Fraser JS. AGA technical review on Celiac Sprue. American Gastroenterological Association. Gastroenterology 2001;120(6):1526–40.
67. Hill ID, Dirks MH, Liptak GS, Colletti RB, Fasano A, Guandalini S, et al. Guideline for the diagnosis and treatment of celiac disease in children: recommendations of the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition. J Pediatr Gastroenterol Nutr 2005;40(1):1–19.
68. Ludvigsson JF, Card TR, Kaukinen K, Bai J, Zingone F, Sanders DS, et al. Screening for celiac disease in the general population and in high-risk groups. United Eur Gastroenterol J 2015;3(2):106–20.
69. Singh P, Arora S, Lal S, Strand TA, Makharia GK. Risk of celiac disease in the first- and second-degree relatives of patients with celiac disease: a systematic review and meta-analysis. Am J Gastroenterol 2015;110(11):1539–48.
70. Oxentenko AS, Grisolano SW, Murray JA, Burgart LJ, Dierkhising RA, Alexander JA. The insensitivity of endoscopic markers in celiac disease. Am J Gastroenterol 2002;97(4):933–8.
71. Niveloni S, Fiorini A, Dezi R, Pedreira S, Smecuol E, Vazquez H, et al. Usefulness of videoduodenoscopy and vital dye staining as indicators of mucosal atrophy of celiac disease: assessment of interobserver agreement. Gastrointest Endosc 1998;47(3):223–9.
72. Marsh MN, W Johnson M, Rostami K. Mucosal histopathology in celiac disease: a rebuttal of Oberhuber’s sub-division of Marsh III. Gastroenterol Hepatol Bed Bench 2015;8(2):99–109.
73. Oberhuber G, Granditsch G, Vogelsang H. The histopathology of coeliac disease: time for a standardized report scheme for pathologists. Eur J Gastroenterol Hepatol 1999;11(10):1185–94.
74. Mooney PD, Kurien M, Evans KE, Rosario E, Cross SS, Vergani P, et al. Clinical and immunologic features of ultra-short celiac disease. Gastroenterology 2016;150(5):1125–34.
75. Leffler D, Schuppan D, Pallav K, Najarian R, Goldsmith JD, Hansen J, et al. Kinetics of the histological, serological and symptomatic responses to gluten challenge in adults with coeliac disease. Gut 2013;62(7):996–1004.
76. Rostami K, Kerckhaert J, Tiemessen R, von Blomberg BM, Meijer JW, Mulder CJ. Sensitivity of antiendomysium and antigliadin antibodies in untreated celiac disease: disappointing in clinical practice. Am J Gastroenterol 1999;94(4):888–94.
77. Corazza GR, Villanacci V. Coeliac disease. J Clin Pathol 2005;58(6):573–4.
78. Rostom A, Dubé C, Cranney A, Saloojee N, Sy R, Garritty C, et al. The diagnostic accuracy of serologic tests for celiac disease: a systematic review. Gastroenterology 2005;128(4 Suppl 1):S38-46.
79. Leffler DA, Schuppan D. Update on serologic testing in celiac disease. Am J Gastroenterol 2010;105(12):2520–4.
80. Chorzelski TP, Beutner EH, Sulej J, Tchorzewska H, Jablonska S, Kumar V, et al. IgA anti-endomysium antibody. A new immunological marker of dermatitis herpetiformis and coeliac disease. Br J Dermatol 1984;111(4):395–402.
81. Dieterich W, Ehnis T, Bauer M, Donner P, Volta U, Riecken EO, et al. Identification of tissue transglutaminase as the autoantigen of celiac disease. Nat Med 1997;3(7):797–801.
82. Sugai E, Moreno ML, Hwang HJ, Cabanne A, Crivelli A, Nachman F, et al. Celiac disease serology in patients with different pretest probabilities: is biopsy avoidable? World J Gastroenterol 2010;16(25):3144–52.
83. Bufler P, Heilig G, Ossiander G, Freudenberg F, Grote V, Koletzko S. Diagnostic performance of three serologic tests in childhood celiac disease. Z Gastroenterol 2015;53(2):108–14.
84. Nachman F, Sugai E, Vázquez H, González A, Andrenacci P, Niveloni S, et al. Serological tests for celiac disease as indicators of long-term compliance with the gluten-free diet. Eur J Gastroenterol Hepatol 2011;23(6):473–80.
85. Weile B, Hansen BF, Hägerstrand I, Hansen JP, Krasilnikoff PA. Interobserver variation in diagnosing coeliac disease. A joint study by Danish and Swedish pathologists. APMIS 2000;108(5):380–4.
86. Webb C, Norström F, Myléus A, Ivarsson A, Halvarsson B, Högberg L, et al. Celiac disease can be predicted by high levels of anti-tissue transglutaminase antibodies in population-based screening. J Pediatr Gastroenterol Nutr 2015;60(6):787–91.
87. Husby S, Koletzko S, Korponay-Szabó IR, Mearin ML, Phillips A, Shamir R, et al. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition guidelines for the diagnosis of coeliac disease. J Pediatr Gastroenterol Nutr 2012;54(1):136–60.
88. Sandström O, Rosén A, Lagerqvist C, Carlsson A, Hernell O, Högberg L, et al. Transglutaminase IgA antibodies in a celiac disease mass screening and the role of HLA-DQ genotyping and endomysial antibodies in sequential testing. J Pediatr Gastroenterol Nutr 2013;57(4):472–6.
89. Sugai E, Hwang HJ, Vázquez H, Moreno ML, Costa F, Longarini G, et al. Should ESPGHAN guidelines for serologic diagnosis of celiac disease be used in adults? A prospective analysis in an adult patient cohort with high pretest probability. Am J Gastroenterol 2015;110(10):1504–5.
90. Oyaert M, Vermeersch P, De Hertogh G, Hiele M, Vandeputte N, Hoffman I, et al. Combining antibody tests and taking into account antibody levels improves serologic diagnosis of celiac disease. Clin Chem Lab Med 2015;53(10):1537–46.
91. Newnham ED, Shepherd SJ, Strauss BJ, Hosking P, Gibson PR. Adherence to the gluten-free diet can achieve the therapeutic goals in almost all patients with coeliac disease: a 5-year longitudinal study from diagnosis. J Gastroenterol Hepatol 2016;31(2):342–9.
92. Kurppa K, Collin P, Mäki M, Kaukinen K. Celiac disease and health-related quality of life. Expert Rev Gastroenterol Hepatol 2011;5(1):83–90.
93. Nachman F, del Campo MP, González A, Corzo L, Vázquez H, Sfoggia C, et al. Long-term deterioration of quality of life in adult patients with celiac disease is associated with treatment noncompliance. Dig Liver Dis 2010;42(10):685–91.
94. Cranney A, Rostom A, Sy R, Dubé C, Saloogee N, Garritty C, et al. Consequences of testing for celiac disease. Gastroenterology 2005;128(4 Suppl 1):S109–20.
95. Brousse N, Meijer JWR. Malignant complications of coeliac disease. Best Pract Res Clin Gastroenterol 2005;19(3):401–12.
96. Anderson LA, Gadalla S, Morton LM, Landgren O, Pfeiffer R, Warren JL, et al. Population-based study of autoimmune conditions and the risk of specific lymphoid malignancies. Int J Cancer 2009;125(2):398–405.
97. Corazza GR, Di Stefano M, Mauriño E, Bai JC. Bones in coeliac disease: diagnosis and treatment. Best Pract Res Clin Gastroenterol 2005;19(3):453–65.
98. Olmos M, Antelo M, Vazquez H, Smecuol E, Mauriño E, Bai JC. Systematic review and meta-analysis of observational studies on the prevalence of fractures in coeliac disease. Dig Liver Dis 2008;40(1):46–53.
99. Saccone G, Berghella V, Sarno L, Maruotti GM, Cetin I, Greco L, et al. Celiac disease and obstetric complications: a systematic review and metaanalysis. Am J Obstet Gynecol 2016;214(2):225–34.
100. Green PHR, Cellier C. Celiac disease. N Engl J Med 2007;357(17):1731–43.
101. Ciacci C, Ciclitira P, Hadjivassiliou M, Kaukinen K, Ludvigsson JF, McGough N, et al. The gluten-free diet and its current application in coeliac disease and dermatitis herpetiformis. United Eur Gastroenterol J 2015;3(2):121–35.
102. Collin P. Should adults be screened for celiac disease? What are the benefits and harms of screening? Gastroenterology 2005;128(4 Suppl 1):S104–8.
103. Hoffenberg EJ. Should all children be screened for celiac disease? Gastroenterology 2005;128(4 Suppl 1):S98–103.
104. Sugai E, Nachman F, Váquez H, González A, Andrenacci P, Czech A, et al. Dynamics of celiac disease-specific serology after initiation of a gluten-free diet and use in the assessment of compliance with treatment. Dig Liver Dis 2010;42(5):352–8.
105. Moreno M de L, Cebolla Á, Muñoz-Suano A, Carrillo-Carrion C, Comino I, Pizarro Á, et al. Detection of gluten immunogenic peptides in the urine of patients with coeliac disease reveals transgressions in the gluten-free diet and incomplete mucosal healing. Gut 2015 Nov 25. doi: 10.1136/gutjnl-2015-310148 [Epub ahead of print].
106. Forbes GM. If only my celiac patients and I knew that…. Clin Gastroenterol Hepatol 2015;13(3):614–5.
107. Pulido OM, Gillespie Z, Zarkadas M, Dubois S, Vavasour E, Rashid M, et al. Introduction of oats in the diet of individuals with celiac disease: a systematic review. Adv Food Nutr Res 2009;57:235–85.
108. Akobeng AK, Thomas AG. Systematic review: tolerable amount of gluten for people with coeliac disease. Aliment Pharmacol Ther 2008;27(11):1044–52.
109. Ciacci C, Maiuri L, Russo I, Tortora R, Bucci C, Cappello C, et al. Efficacy of budesonide therapy in the early phase of treatment of adult coeliac disease patients with malabsorption: an in vivo/in vitro pilot study. Clin Exp Pharmacol Physiol 2009;36(12):1170–6.
110. Ludvigsson JF, Card T, Ciclitira PJ, Swift GL, Nasr I, Sanders DS, et al. Support for patients with celiac disease: a literature review. United Eur Gastroenterol J 2015;3(2):146–59.
111. Ludvigsson JF, Agreus L, Ciacci C, Crowe SE, Geller MG, Green PHR, et al. Transition from childhood to adulthood in coeliac disease: the Prague consensus report. Gut 2016;65(8):1242–51.
112. Haines ML, Anderson RP, Gibson PR. Systematic review: the evidence base for long-term management of coeliac disease. Aliment Pharmacol Ther 2008;28(9):1042–66.
113. Leffler DA, Edwards George JB, Dennis M, Cook EF, Schuppan D, Kelly CP. A prospective comparative study of five measures of gluten-free diet adherence in adults with coeliac disease. Aliment Pharmacol Ther 2007;26(9):1227–35.
114. Hollon JR, Cureton PA, Martin ML, Puppa ELL, Fasano A. Trace gluten contamination may play a role in mucosal and clinical recovery in a subgroup of diet-adherent non-responsive celiac disease patients. BMC Gastroenterol 2013;13:40.
115. Ciacci C, Cavallaro R, della Valle N, d’Argenio G. The use of serum tTG-ab assay in patients on gluten-free diet as a measure of dietetic compliance. Gastroenterology 2002;122(2):588.
116. García-Manzanares A, Tenias JM, Lucendo AJ. Bone mineral density directly correlates with duodenal Marsh stage in newly diagnosed adult celiac patients. Scand J Gastroenterol 2012;47(8–9):927–36.
117. Zingone F, Abdul Sultan A, Crooks CJ, Tata LJ, Ciacci C, West J. The risk of community-acquired pneumonia among 9803 patients with coeliac disease compared to the general population: a cohort study. Aliment Pharmacol Ther 2016;44(1):57–67.
118. Hall NJ, Rubin G, Charnock A. Systematic review: adherence to a gluten-free diet in adult patients with coeliac disease. Aliment Pharmacol Ther 2009;30(4):315–30.
119. Leffler DA, Edwards-George J, Dennis M, Schuppan D, Cook F, Franko DL, et al. Factors that influence adherence to a gluten-free diet in adults with celiac disease. Dig Dis Sci 2008;53(6):1573–81.
120. Ciacci C, Iavarone A, Siniscalchi M, Romano R, De Rosa A. Psychological dimensions of celiac disease: toward an integrated approach. Dig Dis Sci 2002;47(9):2082–7.
121. Niewinski MM. Advances in celiac disease and gluten-free diet. J Am Diet Assoc 2008;108(4):661–72.
122. Pinto-Sanchez MI, Verdu EF, Gordillo MC, Bai JC, Birch S, Moayyedi P, et al. Tax-deductible provisions for gluten-free diet in Canada compared with systems for gluten-free diet coverage available in various countries. Can J Gastroenterol Hepatol 2015;29(2):104–10.
123. Republic of Argentina. National Ministry of Health. [Clinical practice guidelines on diagnosis and treatment of celiac disease. Detection and National Celiac Disease Control. Official Gazette No. 32148]. May 2011. [Internet]. Available at: http://www.msal.gob.ar.
124. Chmielewska A, Pieścik-Lech M, Szajewska H, Shamir R. Primary prevention of celiac disease: environmental factors with a focus on early nutrition. Ann Nutr Metab 2015;67 Suppl 2:43–50.
125. Szajewska H, Shamir R, Mearin L, Ribes-Koninckx C, Catassi C, Domellöf M, et al. Gluten introduction and the risk of coeliac disease: a position paper by the European Society for Pediatric Gastroenterology, Hepatology, and Nutrition. J Pediatr Gastroenterol Nutr 2016;62(3):507–13.
126. Mearin ML. The prevention of coeliac disease. Best Pract Res Clin Gastroenterol 2015;29(3):493–501.
127. Catassi C, Fasano A. Coeliac disease. The debate on coeliac disease screening—are we there yet? Nat Rev Gastroenterol Hepatol 2014;11(8):457–8.
128. O’Leary C, Wieneke P, Healy M, Cronin C, O’Regan P, Shanahan F. Celiac disease and the transition from childhood to adulthood: a 28-year follow-up. Am J Gastroenterol 2004;99(12):2437–41.
129. Mozer-Glassberg Y, Zevit N, Rosenbach Y, Hartman C, Morgenstern S, Shamir R. Follow-up of children with celiac disease—lost in translation? Digestion 2011;83(4):283–7.
130. Cellier C, Delabesse E, Helmer C, Patey N, Matuchansky C, Jabri B, et al. Refractory sprue, coeliac disease, and enteropathy-associated T-cell lymphoma. French Coeliac Disease Study Group. Lancet 2000;356(9225):203–8.
131. Rubio-Tapia A, Murray JA. Classification and management of refractory coeliac disease. Gut 2010;59(4):547–57.
132. Rubio-Tapia A, Hill ID, Kelly CP, Calderwood AH, Murray JA. ACG clinical guidelines: diagnosis and management of celiac disease. Am J Gastroenterol 2013;108(5):656–76.