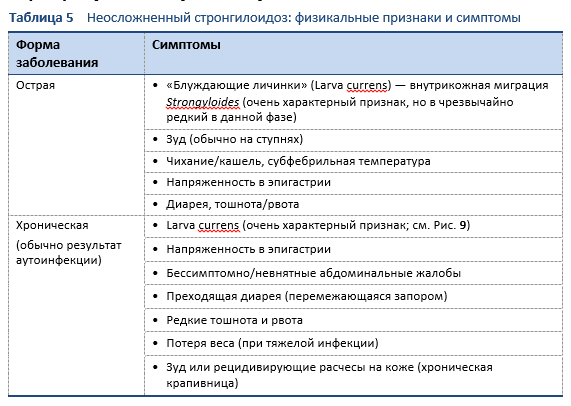
Стронгилоидоз – это инфекция круглым червем Strongyloides stercoralis (Рис. 1), которая широко распространена в тропических и субтропических областях, но также встречается и в странах с умеренным климатом (Таблица 3).
- Человеческий стронгилоидоз вызывается видами паразитической нематоды Strongyloides. Из них S. stercoralis – наиболее частый патоген для человека; S. fuelleborni спорадически выявляется в Африке и Папуа - Новой Гвинее.
- Личинки инфекционного S. stercoralis могут реплицироваться в кишечнике и напрямую аутоинфицировать зараженных пациентов – аутоинфекция является главным признаком, отличающим стронгилоидоз от других гельминтозных макропаразитарных инфекций, передающихся через почву. Основные типы таких гельминтов, инфицирующих человека – это круглые черви (Ascaris lumbricoides), власоглав (Trichuris trichiura) и анкилостомы (Necator americanus и Ancylostoma duodenale) [1].
- Взрослый червь мужского пола обнаруживается только в почве. Он не является тканевым паразитом и не существует в организме человека-хозяина.
- Взрослый червь женского пола очень маленького размера, почти прозрачный. Его длина - приблизительно 2.2–2.5 мм, с диаметром 50 µm, и он обитает в туннелях между эритроцитами в тонком кишечнике человека.
- Инфекционная личинка может реплицироваться в зараженной почве и заражать человека при контакте с землей.
Стронгилоидоз отличается от других гельминтозных инфекций, передающихся через почву, тем, что из яиц, отложенных особью женского пола путем партеногенеза, и все еще находящихся в кишечнике, выводятся рабдитоформные личинки.
- Личинки обычно выводятся с фекалиями, но некоторые могут дорасти до филяриформной стадии и реинфицировать хозяина, пенетрируя в нижних отделах кишечника или в кожу перианальной области (аутоинфекционный цикл).
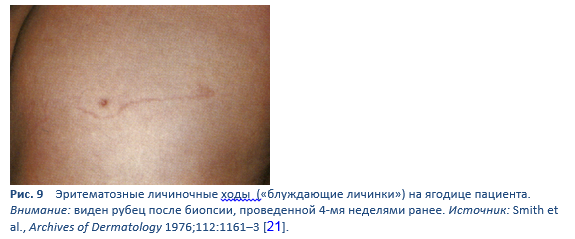
- В зависимости от иммунного статуса хозяина это может привести к диссеминации и гиперинфекции (Таблица 4).


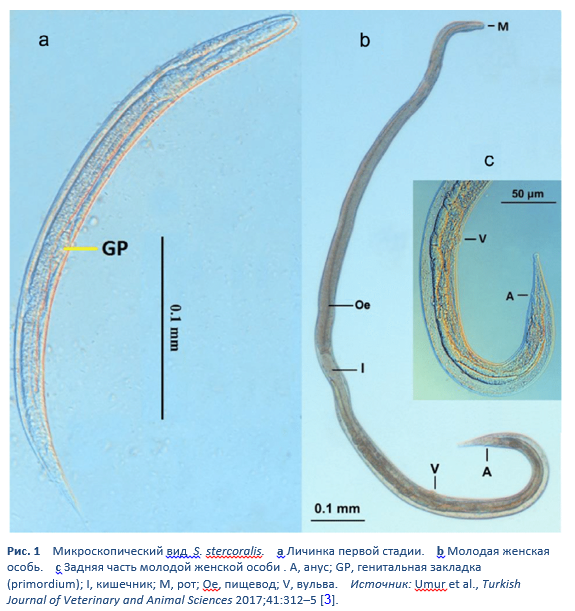
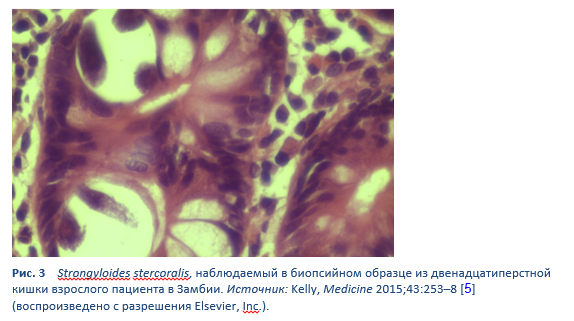
В жизненном цикле червя существуют две важные стадии: рабдитоформная и филяриформная (Рис. 2, 3).
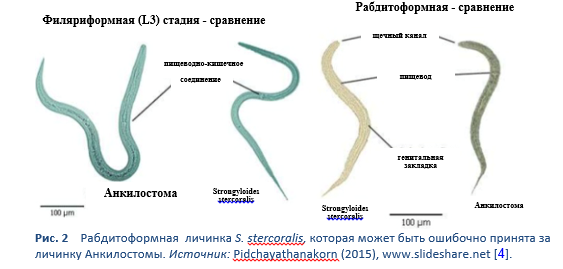
2.1 Гельминтозы, передающиеся через почву, и стронгилоидоз
Хотя стронгилоидоз имеет сходный с другими гельминтозами, передающимися через почву, путь заражения, для его диагностики кроме микроскопии требуются дополнительные методы и он требует другого лечения. В областях, где проводилась профилактическая антигельминтная химиотерапия ивермектином для контроля над онхоцеркозом или лимфатическим филяриозом, отмечалось заметное уменьшение распространенности стронгилоидоза [6–10]. Комитет по жизненно необходимым медицинским препаратам ВОЗ включил в список ивермектин, а также его комбинацию с альбендазолом, для лечения стронгилоидоза. Около 900 миллионов человек в настоящее время получают эту комбинацию в рамках программы борьбы с тропическими заболеваниями (NTD) [11].
2.2 Патофизиология
Strongyloides stercoralis имеет уникальный и комплексный жизненный цикл. Рисунок 4 подчеркивает уникальные пути репликации S. stercoralis.
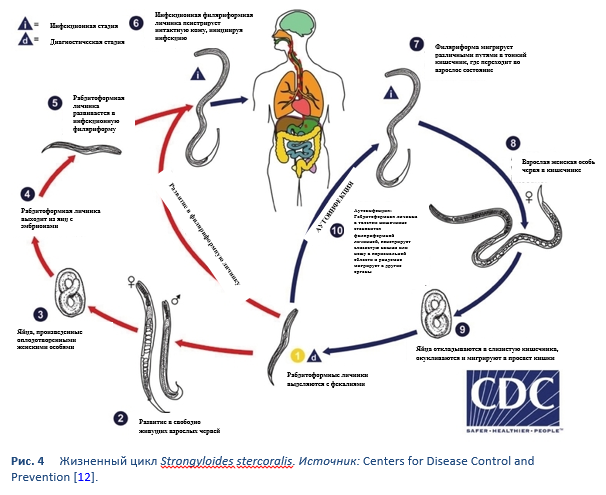
Жизненный цикл Strongyloides с его переходом между свободно живущим и паразитическим циклами и потенциалом к аутоинфекции и размножении в организме хозяина, более сложен, чем у большинства нематод. Два типа цикла:
- Свободно живущий цикл. Рабдитоформные личинки, попадая в фекалии, могут либо дважды пройти линьку и стать инфекционной филяриформной личинкой (прямое развитие), либо пройти линьку четыре раза и превратиться во взрослых особей мужского и женского пола, которые спариваются и откладывают яйца, из которых выходят рабдитоформные личинки. Последние, в свою очередь, могут либо развиваться в новое поколение свободно живущих взрослых, либо в инфекционные филяриформные личинки. Филяриформные личинки пенетрируют кожу человека-хозяина и инициируют паразитический цикл.
Свободно живущая стадия жизненного цикла нематоды ограничена максимум одним поколением [13]. Это уникальная черта стронгилоидоза, которая имеет важное значение как для лечения инфицированных пациентов, так и для контроля окружающей среды в целях профилактики заражения. Это означает, что эрадикационная терапия должна быть высоко эффективной для уничтожения всех жизненных форм паразита в организме инфицированного человека.
- Паразитический цикл. Филяриформная личинка из зараженной почвы пенетрирует кожу человека и транспортируется в легкие, где проникает в альвеолярные пространства; через бронхиальное дерево она попадает в глотку, проглатывается и достигает тонкого кишечника. Там личинка дважды линяет и становится взрослой особью червя мужского или женского пола. Женские особи живут, прикрепившись к эпителию тонкого кишечника, и посредством партеногенеза производят яйца, из которых выходят рабдитоформные личинки. Рабдитоформная личинка может либо попасть в фекалии (см. «свободно живущий цикл» выше), либо может развиваться далее и вызывать аутоинфекцию. При аутоинфекции рабдитоформная личинка становится инфекционной филяриформной личинкой, которая может пенетрировать либо в слизистую оболочку кишечника (внутренняя аутоинфекция), либо в кожу перианальной области (внешняя аутоинфекция). В любом случае филяриформная личинка может либо следовать по ранее описанному пути, успешно переносясь в легкие, бронхиальное дерево, глотку и в тонкий кишечник, где она развивается во взрослую форму, либо личинки могут широко диссеминировать в организме зараженного человека. К настоящему времени появление аутоинфекции у человека обнаружено только при инфекциях Strongyloides stercoralis и Capillaria philippinensis. S. stercoralis распространен значительно шире. При стронгилоидозе аутоинфекция объясняет существование инфекций, персистирующих у людей, которые не находились в эндемичных зонах в течение многих лет (текущий рекорд – 65 лет), и жизнеугрожающую заболеваемость гиперинфекцией у иммунокомпроментированных лиц – и то и другое нехарактерно для инфекций другими гельминтами.
2.3 Бремя болезни и эндемичность
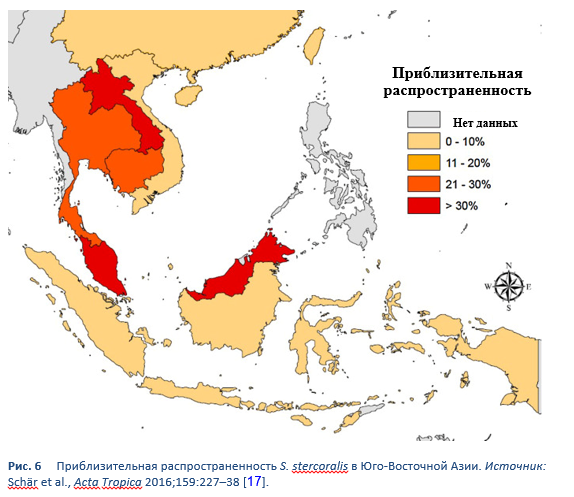
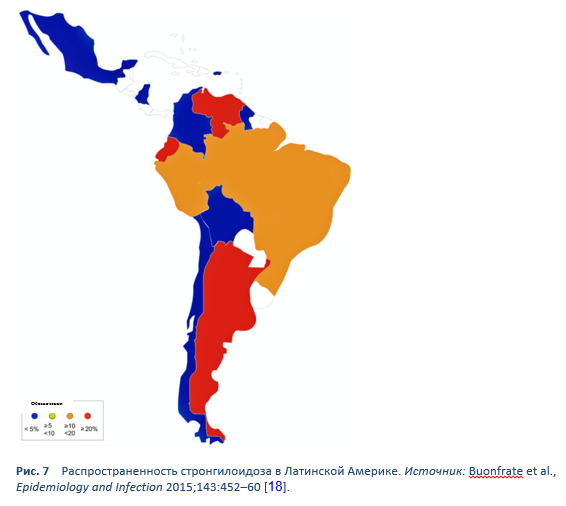
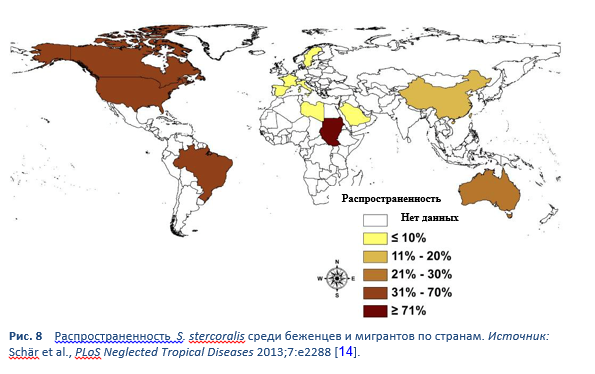
Стронгилоидоз эндемичен для тропических и субтропических регионов (Рис. 5–8), и его распространенность вероятно гораздо выше ранее упоминавшихся 100 миллионов человек: наиболее высокой опубликованной цифрой является 370 миллионов человек [2]. Он также широко распространен в Восточной Европе, и также сообщалось об отдельных очагах инфекции среди пожилых людей в Средиземноморском регионе.
Мы мало знаем о распространенности инфекции и еще меньше о клиническом бремени заболеваемости. Если заболевание действительно широко распространено, то риск ятрогенной гиперинфекции (при иммуносупрессивной терапии) представляет собой медицинский вызов. Предполагается, что стронгилоидозом заражено до 40% населения некоторых областей тропиков и субтропиков [14].
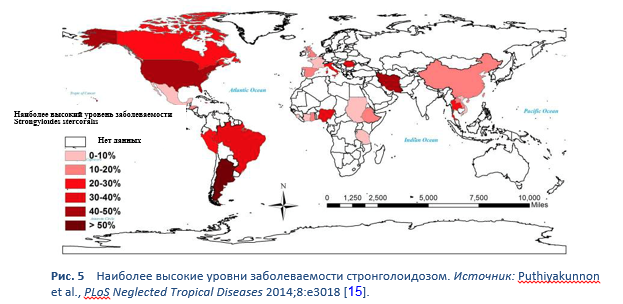
Важные замечания: В Австралии, как и в других развитых странах, имеются «горячие точки» Strongyloides, которые не показаны на карте (в особенности инфекцией страдают некоторые мигранты из эндемичных районов, но инфекция также эндемична среди некоторых аборигенских популяций на севере Австралии) [13,16].
Рисунок иллюстрирует, насколько скудны данные. Невероятно, чтобы Strongyloides отсутствал на большей части территории Африки и Азии. Возможно, могли бы быть процитированы другие исследования, которые показывают широкое распространение инфекции Strongyloides. Также невероятно, что в некоторых странах распространенность в популяции показана выше 50%; необходимо учитывать предвзятость выбора.
Инфекция среди мигрантов может возникнуть в любой стране и представлять собой глобальную угрозу. Заболевание может быть выявлено в кабинете врача в любом месте мира.
2.4 Факторы риска и особые группы риска инфекции
В целом наибольшим фактором риска являются социоэкономические неблагоприятные условия в соответствующей окружающей среде, эндемичной по Strongyloides.
- Бедность, плохое жилье, плохая санитария; хождение босиком, проживание в окружении, в котором происходит открытая дефекация
- Военнопленные
- Статус беженца — беженцы из стран, эндемичных по стронгилоидозу
- Путешествующие в эндемичные зоны и из них
- Некоторые исследования называют факторами риска мужской пол, пожилой возраст, трансмиссию «животное-человек» и влажный, сырой климат в тропиках и субтропиках [17]
2.5 Факторы риска и особые группы риска диссеминированной инфекции
- Иммуносупрессивная терапия — особенно кортикостероиды, но также такролимус и химиотерапевтические средства
- Пациенты с измененным клеточным иммунитетом
- Инфекция Т-лимфотропным вирусом человека тип 1
- Новообразования, особенно злокачественные гематологические (лимфома, лейкемия)
- Трансплантация органов (реципиенты почечного аллотрансплантата)
- Второстепенные/возможные факторы риска: коллагеновая сосудистая болезнь, состояние мальабсорбции и мальнутриции, заболевание почек в терминальной стадии, сахарный диабет, местные факторы хозяина, дивертикулярные и слепые петли (персистирующий стронгилоидоз в слепой петле в кишечнике)
2.6 Стронгилоидоз и иммуносупрессивные пациенты
Формы стронгилоидоза варьируют от бессимптомной до тяжелой и могут привести к развитию синдрома гиперинфекции и диссеминированному заболеванию, связанному с высоким уровнем смертности у пациентов с пониженным иммунитетом.
В тропиках имеется большое количество пациентов с ревматоидным артритом, бронхиальной астмой и гломерулонефритом, которые получают длительное лечение стероидами. Пациенты могут приобретать стероидные препараты непосредственно в аптеках без рецептов.
Стронгилоидоз не является важной оппортунистической инфекцией, связанной со СПИД, но по отношению к Т-лимфотропному вирусу человека тип I (HTLV-I) - это оппортунистическая инфекция [19]. Хотя у пациентов с вирусом иммунодефицита человека/синдромом приобретенного иммунодефицита (ВИЧ/СПИД) может наблюдаться диссеминированный стронгилоидоз или синдром гиперинфекции, обсервационные исследования не показывают повышенного риска в данной популяции [20].
2.7 Смертность и заболеваемость
Острый стронгилоидоз часто протекает бессимптомно и может оставаться незамеченным десятилетиями. У иммунокомпетентных пациентов инфекция может протекать бессимптомно в течение всей жизни, если не проводится лечение.
Хронические инфекции - это потенциально важная причина смертности по неизвестным причинам. Также играет свою роль отсутствие эффективных диагностических средств, а те, которые имеются, часто неудобны в применении и обладают низкой чувствительностью, поэтому истинные показатели частоты инфекции и смертность неизвестны. Так как стронгилоидоз рассматривается как необычное заболевание, в диагностические или эпидемиологические исследования, особенно у детей, вкладывается мало средств.
Клинически проявляющийся стронгилоидоз может приводить к развитию кожных, желудочно-кишечных и легочных симптомов.
Имеющиеся доказательства показывают необходимость обследования пациентов с эозинофилией, даже когда в анамнезе отсутствуют данные о проживании или поездках в эндемичные области [22].
За прошедшие годы были разработаны несколько диагностических процедур, и их использование зависит от местной доступности и имеющегося у персонала опыта: струнные тесты, дуоденальные аспираты, дуоденальная биопсия, бронхоальвеолярный лаваж (БАЛ), иммунодиагностические исследования и повторные анализы свежего кала различными методами.
Глобальная распространенность инфекции Strongyloides stercoralis долгое время недооценивалась. Это вероятно связано с доверием к результатам прямой микроскопии кала и методу Като – Каца, которые широко применялись в исследованиях по распространенности, но неадекватны в выявлении S. stercoralis [23]. Широко применяемые исследования кала обладают очень низкой чувствительностью. Данные микроскопии могут быть улучшены исследованием нескольких образцов кала, а также методами обогащения [24], но чувствительность все равно остается низкой.
Как в странах с низким и средним уровнем доходов, так и в развитых странах количество персонала, хорошо обученного микроскопической идентификации паразитов по всей видимости снижается.
- Ожидается, что в паразитологии возрастет применение молекулярных исследований, в настоящее время все еще отстающих от вирусологии и бактериологии.
- Молекулярный диагноз инфекции S. stercoralis еще должен продемонстрировать оптимальную чувствительность.
- Маловероятно, что молекулярный диагноз полностью заменит другие диагностические методы.
- В настоящий момент серологические исследования показывают наибольшую чувствительность и являются важным инструментом для скрининга S. stercoralis и оценки результатов лечения [23].
Lodh et al. [25] представили результаты исследования, показывающие, что ДНК S. stercoralis может быть определена в моче. Когда такие исследования мочи станут широко доступны и докажут свою чувствительность, они могут стать удобным способом диагностики, поскольку они менее трудо- и ресурсоемкие, а также представляют меньший риск для здоровья исследователя, чем анализ свежего кала [25].
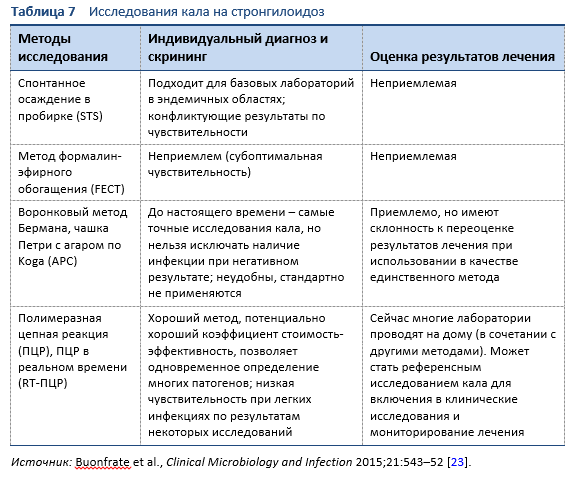
4.1 Исследования кала
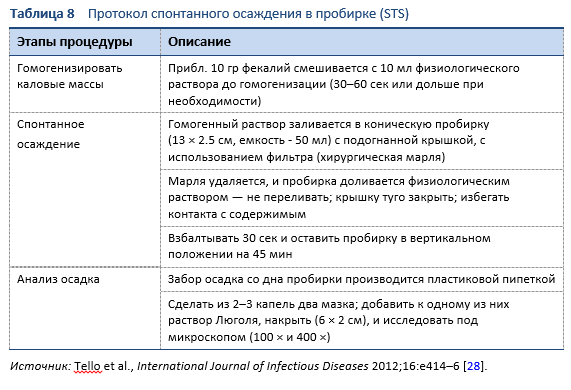
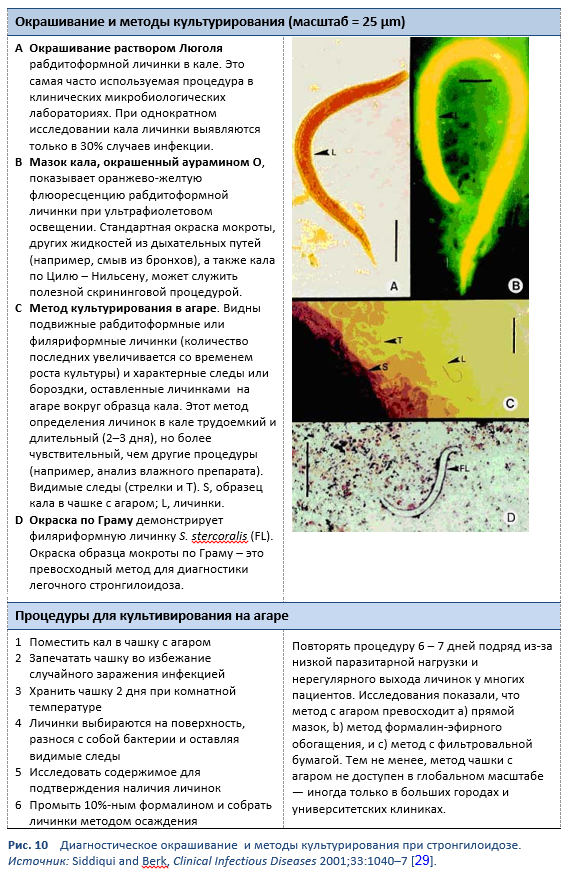
Обнаружение личинок в фекалиях, дуоденальном содержимом или иногда в других тканях и жидкостях средствами микроскопии позволяет установить точный диагноз стронгилоидоза (Таблицы 7, 8; Рис. 10, 11). Тем не менее, из-за низкой плотности тела личинки, однократное исследование нечувствительно [26].
Для идентификации личинок в кале с помощью микроскопии используется несколько методов:
- Микроскопия после обогащения
- Воронковый метод Бермана (все еще считается золотым стандартом)
- Метод формалин-эфирного обогащения (FECT)
- Микроскопия после культурирования
- Метод Харада – Мори с фильтровальной бумагой
- Чашечный метод на агаре по Koga
- Использование препаровального микроскопа для визуализации личинок в чашке Петри с агаром
- Прямой мазок фекалий с окрашиванием Люголем
Использование этих методов зависит от местной доступности и, особенно, от опыта специалиста по микроскопии.
Исследования кала на Strongyloides с применением воронкового метода Бермана и чашечного метода на агаре по Koga – это лучшие диагностические методы, которые применяются в полевых условиях. Эти методы позволяют определить паразита с большей чувствительностью, чем другие методы исследования кала.
- ПЦР выглядит обещающе, но методика пока еще не стандартизирована; существуют определенные сомнения о чувствительности ПЦР, поскольку в различных исследованиях этот показатель варьирует.
- Anamnart et al. [27] исследовали стимуляцию выведения личинок S. stercoralis со стулом посредством орального приема однократной дозы альбендазола 400 мг и высказали предположение о том, что применение альбендазола плюс модифицированный метод формалин-эфирного обогащения (MFECT) может применяться у пациентов с подозрением на бессимптомный стронгилоидоз – включая больных с необъяснимой хронической диареей, лиц, вернувшихся из эндемичный на стронгилоидоз районов, и пациентов с негативными результатами других паразитологических методов обследования [27].

4.2 Серодиагноз стронгилоидоза
По сравнению с методом Бермана и культурой на агаре, серологические тесты обладают большей чувствительностью, хотя некоторые авторы сомневаются в их специфичности [20].
- Многие серологические тесты перекрестно реагируют на филяриальных паразитов, шистосом и Ascaris lumbricoides, что снижает специфичность исследований.
- Могут возникать сложности в различии активных и анамнестических случаев, поскольку антитела могут персистировать в течение некоторого времени.
- Более специфичные серологические тесты с применением рекомбинантных антигенов уже разработаны или продолжают разрабатываться и доступны в специализированных лабораториях.
- Серологические тесты обычно показывают значительное снижение титра через 6 – 12 месяцев после эрадикации паразита, таким образом, они могут быть использованы для оценки проведенного лечения [20].
Наиболее убедительным и широко применяемым серологическим методом для выявления сывороточного иммуноглобулина G (IgG) по сравнению с примитивным извлечением филяриформной личинки является иммуноферментный анализ (ELISA). ELISA – трудоемкий метод, требующий наличия определенного уровня лабораторной инфраструктуры для его проведения и интерпретации результатов, что препятствует доступности исследования, особенно в эндемичных по Strongyloides районах [26]. Более того, серология имеет ограниченную ценность для динамического наблюдения после лечения, учитывая возможность развития реинфекции.
4.3 Дифференциальный диагноз
Существует множество состояний, вызывающих сходные симптомы, включая причины острой и хронической диареи и мальабсорбции, другие причины эозинофилии и тяжелой грам-негативной септицемии. При дифференциальном диагнозе необходимо помнить о следующих состояниях:
- Кишечные инфекции — амебиаз, бактериальный колит, Shigella, Campylobacter, Yersinia, Clostridium difficile; см. Глобальные Практические Рекомендации ВГО по острой диарее, Таблица 4 [30].
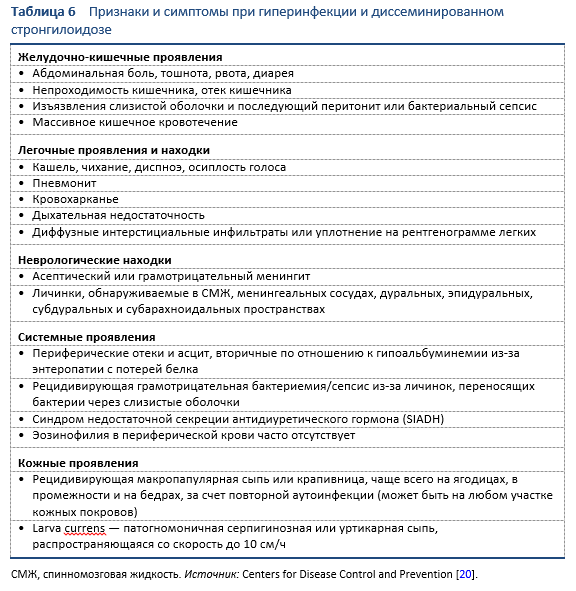
- Нечеловеческая анкилостомная инфекция, продуцирующая кожные «блуждающие личинки» — отличающиеся от тех, которые появляются при S. stercoralis, отсутствием струпьев, быстрой миграцией, перианальным вовлечением и широким спектров уртикарии.
- Воспалительная болезнь кишечника.
- Синдром раздраженного кишечника.
- Функциональные абдоминальные расстройства.
- Лекарственные препараты — нестероидные противовоспалительные препараты (РПВП) и многие другие — возможные причины эозинофилии.
Ключевым в диагностике является необходимость помнить о стронгилоидозе как возможном диагнозе и идентифицировать паразита, как прямыми методами, так и с помощью серологических/молекулярных тестов.
- Спонтанное излечение невозможно из-за уникального аутоинфекционного жизненного цикла паразита.
- Необходимо лечить всех пациентов со стронгилоидозом, даже в отсутствии симптомов, из-за риска развития гиперинфекции – потенциально смертельного осложнения.
- Перед назначением иммуносупрессивной терапии пациентам в группе риска нужно провести достоверную диагностику и при необходимости лечение стронгилоидоза. Это же применимо в отношении пациентов с HTLV-I или ВИЧ-инфекцией.
- Если возникает необходимость в неотложной иммуносупрессивной терапии пациента с ранее недиагностированным стронгилоидозом, а проведение диагностических тестов невозможно (только в очень редких лечебных учреждениях можно получить результаты серологии в тот же день), необходимо рассматривать возможность назначения профилактического лечения инвермектином.
- Излечение может быть достигнуто приемом однократной дозы ивермектина.
- Неэффективность терапии ивермектином в основном происходит из-за нарушений иммунитета пациента (часто у пациентов с инфекцией HTLV-I) [26,31].
5.1 Неосложненный стронгилоидоз
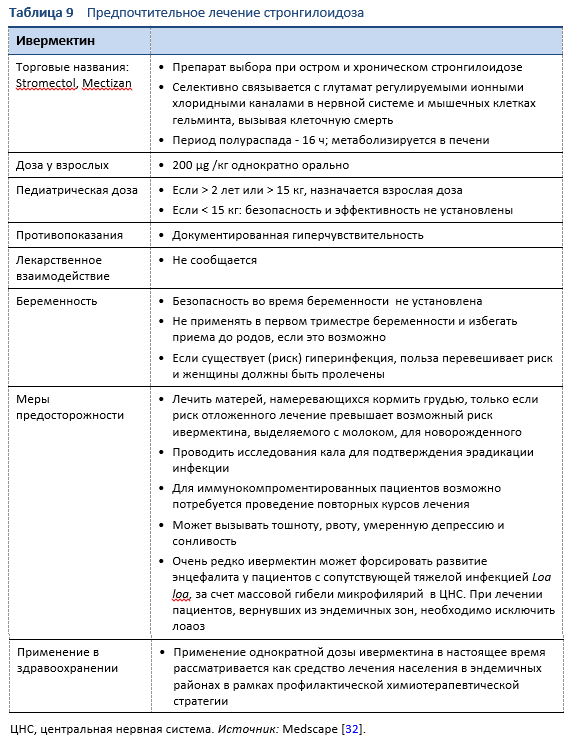
Лечение стронгилоидоза (Таблица 9) кажется сложным по контрасту с другими гельминтными инфекциями, так как паразитарная нагрузка Strongyloides должна быть эрадицирована полностью.
- В полной эрадикации сложно удостовериться из-за небольшого количества гельминтов и нерегулярного выхода личинок.
- Уверенность в окончательном излечивании не может быть получена только на основании однократного негативного динамического исследования кала — требуется также наличие снижения как серологических титров, так и эозинофилии в анализах крови.
- Однократный анализ кала на стронгилоидоз оказывается негативным в 70% подтвержденных случаев инфекции Strongyloides. Достоверные результаты требуют проведения повторных исследований кала, вероятно, как минимум три раза с применением соответствующего метода.
- Динамическое наблюдение пациентов в тропиках представляет собой проблему, и если доступна возможность только исследования кала, то оно становится методом выбора.
- Альбендазол (400 мг 2 раза в день в течение 3 дней) иногда применяется как альтернативный или компромиссный вариант [33,34]. Тем не менее, было показано, что эффективность альбендазола по сравнению с ивермектином очень низка, и, следовательно, он может применяться только в отсутствии альтернативы [35].
5.2 Гиперинфекция или диссеминированная инфекция
Хотя некоторые авторы заявляют, что эти термины описывают два различных аспекта инфекционного процесса (гиперинфекция: высокий уровень присутствия личинок в типичных частях тела; диссеминация: личинки присутствуют в любой части тела, обычно не включенной в паразитарный цикл), вероятно, они могут использоваться взаимозаменяемо. Действительно, оба термина относятся к очень высокой паразитарной нагрузке и быстрому распространению инфекции — обычно у пациентов с иммуносупрессией и часто связаны с кортикостероидной терапией. Гиперинфекция несет в себе высокий риск развития грам-негативной септицемии, поэтому обычно назначаются антибиотики широкого спектра, в частности с целью предотвращения бактериального менингита.
У критических пациентов с гиперинфекцией или диссеминированным стронгилоидозом, неспособных получать оральную терапию, эффективно подкожное введение ивермектина [36]. Таким пациентам ивермектин назначается ежедневно в течение минимум 14 дней; общая длительность терапии зависит от того, когда позитивный результат микроскопического исследования жидкостей организма на наличие личинок сменится на отрицательный (в случаях гиперинфекции это может быть кал, моча или другие жидкости) [37].
5.3 Профилактика и контроль заболевания
Инфекцию можно предотвратить, исключив прямой контакт кожи с почвой, зараженной инфекционными личинками. Лица в группе риска, особенно дети, в районах с зараженной почвой должны носить обувь. Пациенты, входящие в группу риска, должны быть идентифицированы и перед назначением иммуносупрессивной терапии им должны быть проведены соответствующие диагностические тесты.
Лица, контактирующие с пациентами в быту, не рискуют заразиться инфекцией. Правильное удаление экскрементов значительно снижает распространенность стронгилоидоза.
Не существует общепринятых режимов профилактики и не имеется вакцины.
К пациентам, госпитализированным с диагнозом стронгилоидоза, применяются стандартные меры профилактики. Лицам, потенциально вступающим в контакт с фекалиями пациента, необходимо носить перчатки, халаты и тщательно соблюдать гигиену рук [20].
- Раннее выявление и эффективное лечение инфекции S. stercoralis.
- Скрининг пациентов, входящих в группу риска заболевания стронгилоидозом перед началом иммуносупрессивной терапии, особенно кортикостероидами.
- Пока еще нет рекомендаций ВОЗ по профилактической химиотерапии (ПХ) инфекции S. stercoralis, также она не включена в стратегию контроля за гельминтами, передающимися через почву. Тем не менее, при использовании повторной ПХ ивермектином/альбендазолом или только ивермектином в рамках программ по элиминации лимфатического филяриоза и онхоцеркоза также был отмечен значительный эффект на распространенность S. stercoralis [38].
- Правильная оценка результатов анализов кала (с использованием таких высоко чувствительных методов как метод Бермана, культурирование с фильтровальной бумагой, культурирование на агаре) и специфического серологического исследований IgG при динамическом наблюдении 1–2 года [39].
- Предположительные программы по лечению популяций беженцев из стран, эндемичных по кишечным паразитам (анкилостома, Trichuris trichiura, Ascaris lumbricoides и Strongyloides stercoralis) [40].
- Установка и использование безопасных систем по утилизации отходов все еще остается важным фактором [41].
- Ношение обуви могло бы прервать передачу стронгилоидоза, но культурная приемлемость обуви низка, особенно в жарком климате, поэтому на вооружение должны быть взяты методы контроля окружающей среды [42]. У людей, не имеющих обуви, также часто нет и стульев, поэтому их ягодичные области являются дополнительной мишенью для паразитов.
- Определять противогельминтную резистентность на ранней стадии. Для оценки эффективности противогельминтных лекарственных средств доступны различные методы in vivo и in vitro, а для подтверждения подозрения на резистентность к препаратам в этой области могут быть привлечены специфические лаборатории – например, как описано в исследовательских рекомендациях и практических рекомендациях Всемирной Ассоциации Развития Ветеринарной Паразитологии (WAAVP) [43–45].
Исследование Forrer et al. [46] показало, что поголовное лечение однократной дозой ивермектина S. stercoralis в поселении плюс санитарная обработка эффективно снижает риск инфекции в деревенских районах Камбоджи, где более 85% жителей оставались негативными в отношении паразита через год после лечения. Контроль инфекции достижим и высоко эффективен, особенно в комбинации с улучшением санитарных условий [46].
Khieu et al. [47] показали, что лица, имеющие домашний туалет, значительно реже были инфицированы S. stercoralis, по сравнению с теми, кто его не имел. Расчетный популяционный соотнесенный риск мог бы снизиться на 39%, если бы все участвующие в исследовании для дефекации использовали туалет [17,47].
Croker and She обратили внимание на то, что высокая распространенность эозинофилии среди лиц с латентной инфекцией Strongyloides в округе Лос-Анджелес указывает на важность скрининга тех пациентов, типичная причина эозинофилии у которых была отклонена [48].
StrongNet [38], международная сеть улучшения диагностики, лечения и контроля стронгилоидоза, ратует за более точную и привязанную к местности диагностику заболевания, а также на масштабную доступность ивермектина в эндемичных районах. Благодаря усилиям этой сети ивермектин недавно был включен в Список жизненно необходимых лекарственных препаратов ВОЗ, со стронгилоидозом как показанием к применению; конечной целью является развитие стратегии здравоохранения и включение S. stercoralis профилактическую химиотерапевтическую программу ВОЗ для гельминтозов, передающихся через почву.
5.4 Прогноз
Острый и хронический стронгилоидоз имеют хороший прогноз. Тем не менее, нелеченая инфекция может персистировать в течение всей жизни пациента за счет аутоинфекции. Длительное отсутствие пациента в эндемичных областях не гарантирует свободу от инфекции. Тяжелая диссеминированная инфекция часто является смертельной, и часто не отвечает на проводимое лечение.
При хроническом стронгилоидозе иммуносупрессия представляет собой риск ускоренной аутоинфекции. Это может привести к сепсисоподобному синдрому, гиперинфекции S. stercoralis, и диссеминации личинок в отдаленные органы, такие как центральная нервная система, вызывая S. stercoralis–ассоциированный менингит [49].
6.1 Сокращения

6.2 Практические рекомендации золотого стандарта
6.3 Ссылки
1. World Health Organization. Soil-transmitted helminth infections [Internet]. Geneva: World Health Organization; 2017 [accessed 2018 Mar 13]. Available from: http://www.who.int/mediacentre/factsheets/fs366/en/.
2. Bisoffi Z, Buonfrate D, Montresor A, Requena-Méndez A, Muñoz J, Krolewiecki AJ, et al. Strongyloides stercoralis: a plea for action. PLoS Negl Trop Dis 2013 May 9;7(5):e2214.
3. Umur Ş, Meral Y, Bölükbaş CS, Gürler AT, Açici M. First clinical Strongyloides stercoralis case in a dog in Turkey. Turk J Vet Anim Sci 2017;41:312–5.
4. Pidchayathanakorn P. Nemathelminthes [46 slides] [Internet] 2015 [accessed 2018 Mar 13]. Available from: https://www.slideshare.net/PaemikaPidchayathana/nemathelminthes-review.
5. Kelly P. Infectious diarrhoea. Med Abingdon 2015 May;43(5):253–8.
6. Knopp S, Mohammed KA, Rollinson D, Stothard JR, Khamis IS, Utzinger J, et al. Changing patterns of soil-transmitted helminthiases in Zanzibar in the context of national helminth control programs. Am J Trop Med Hyg 2009 Dec;81(6):1071–8.
7. Anselmi M, Buonfrate D, Guevara Espinoza A, Prandi R, Marquez M, Gobbo M, et al. Mass administration of ivermectin for the elimination of onchocerciasis significantly reduced and maintained low the prevalence of Strongyloides stercoralis in Esmeraldas, Ecuador. PLoS Negl Trop Dis 2015 Nov;9(11):e0004150.
8. Barda B, Albonico M, Buonfrate D, Ame SM, Ali S, Speich B, et al. Side benefits of mass drug administration for lymphatic filariasis on Strongyloides stercoralis. Prevalence on Pemba Island, Tanzania. Am J Trop Med Hyg 2017 Sep;97(3):681–3.
9. Bisoffi Z. Human strongyloidiasis: time to act? Paper presented at the 27th European Congress of Clinical Microbiology And Infectious Diseases (ECCMID), Vienna, April 2017. Basel, Switzerland: European Society of Clinical Microbiology and Infectious Diseases; 2017. (ESCMID eLibrary). Available from: www.escmid.org/escmid_publications/escmid_elibrary/material/?mid=44339.
10. World Health Organization. What are intestinal worms (soil transmitted helminthiasis)? [Internet]. Geneva: World Health Organization; [accessed 2018 Mar 13]. Available from: http://www.who.int/intestinal_worms/disease/en/.
11. Bundy DAP, Appleby LJ, Bradley M, Croke K, Hollingsworth TD, Pullan R, et al. Mass deworming programs in middle childhood and adolescence. In: Bundy DAP, de Silva N, Horton S, Jamison DT, Patton GC, editors. Child and Adolescent Health and Development [Internet]. 3rd ed. Washington, DC: International Bank for Reconstruction and Development / World Bank Group; 2017. p. 165–82. (Disease Control Priorities; vol. 8). Available from: http://dcp-3.org/chapter/2437/deworming.
12. Centers for Disease Control and Prevention. Parasites — Strongyloides [Internet]. Atlanta, GA: Centers for Disease Control and Prevention; 2015 [accessed 2018 Mar 13]. Available from: https://www.cdc.gov/parasites/strongyloides/biology.html.
13. Ross KE, Bradbury RS, Garrard TA, O’Donahoo FJ, Shield JM, Page W, et al. The National Strongyloides Working Group in Australia 10 workshops on: commendations and recommendations. Aust N Z J Public Health 2017 Jun;41(3):221–3.
14. Schär F, Trostdorf U, Giardina F, Khieu V, Muth S, Marti H, et al. Strongyloides stercoralis: global distribution and risk factors. PLoS Negl Trop Dis 2013;7(7):e2288.
15. Puthiyakunnon S, Boddu S, Li Y, Zhou X, Wang C, Li J, et al. Strongyloidiasis — an insight into its global prevalence and management. PLoS Negl Trop Dis 2014 Aug;8(8):e3018.
16. Kearns TM, Currie BJ, Cheng AC, McCarthy J, Carapetis JR, Holt DC, et al. Strongyloides seroprevalence before and after an ivermectin mass drug administration in a remote Australian Aboriginal community. PLoS Negl Trop Dis 2017 May;11(5):e0005607.
17. Schär F, Giardina F, Khieu V, Muth S, Vounatsou P, Marti H, et al. Occurrence of and risk factors for Strongyloides stercoralis infection in South-East Asia. Acta Trop 2016 Jul;159:227–38.
18. Buonfrate D, Mena MA, Angheben A, Requena-Mendez A, Muñoz J, Gobbi F, et al. Prevalence of strongyloidiasis in Latin America: a systematic review of the literature. Epidemiol Infect 2015 Feb;143(3):452–60.
19. Crompton DWT, Engels D, Savioli L, Montresor A, Neira M, editors. Preparing to control schistosomiasis and soil-transmitted helminthiasis in the twenty-first century [special double issue of journal]. Acta Trop 2003;86(2–3):121–347.
20. Centers for Disease Control and Prevention. Parasites — Strongyloides. Resources for health professionals [Internet]. Atlanta, GA: Centers for Disease Control and Prevention; 2016 [accessed 2018 Mar 13]. Available from: https://www.cdc.gov/parasites/strongyloides/health_professionals/index.html.
21. Smith JD, Goette DK, Odom RB. Larva currens. Cutaneous strongyloidiasis. Arch Dermatol 1976 Aug;112(8):1161–3.
22. Repetto SA, Ruybal P, Solana ME, López C, Berini CA, Alba Soto CD, et al. Comparison between PCR and larvae visualization methods for diagnosis of Strongyloides stercoralis out of endemic area: A proposed algorithm. Acta Trop 2016 May;157:169–77.
23. Buonfrate D, Formenti F, Perandin F, Bisoffi Z. Novel approaches to the diagnosis of Strongyloides stercoralis infection. Clin Microbiol Infect 2015 Jun;21(6):543–52.
24. Knopp S, Mgeni AF, Khamis IS, Steinmann P, Stothard JR, Rollinson D, et al. Diagnosis of soil-transmitted helminths in the era of preventive chemotherapy: effect of multiple stool sampling and use of different diagnostic techniques. PLoS Negl Trop Dis 2008;2(11):e331.
25. Lodh N, Caro R, Sofer S, Scott A, Krolewiecki A, Shiff C. Diagnosis of Strongyloides stercoralis: detection of parasite-derived DNA in urine. Acta Trop 2016 Nov;163:9–13.
26. van Doorn HR, Koelewijn R, Hofwegen H, Gilis H, Wetsteyn JCFM, Wismans PJ, et al. Use of enzyme-linked immunosorbent assay and dipstick assay for detection of Strongyloides stercoralis infection in humans. J Clin Microbiol 2007 Feb;45(2):438–42.
27. Anamnart W, Pattanawongsa A, Intapan PM, Maleewong W. Albendazole stimulates the excretion of Strongyloides stercoralis larvae in stool specimens and enhances sensitivity for diagnosis of strongyloidiasis. J Clin Microbiol 2010 Nov;48(11):4216–20.
28. Tello R, Terashima A, Marcos LA, Machicado J, Canales M, Gotuzzo E. Highly effective and inexpensive parasitological technique for diagnosis of intestinal parasites in developing countries: spontaneous sedimentation technique in tube. Int J Infect Dis 2012 Jun;16(6):e414-416.
29. Siddiqui AA, Berk SL. Diagnosis of Strongyloides stercoralis infection. Clin Infect Dis 2001 Oct 1;33(7):1040–7.
30. World Gastroenterology Organisation. Acute diarrhea in adults and children: a global perspective [Internet]. Milwaukee, WI: World Gastroenterology Organisation; 2012 [accessed 2018 Mar 13]. Available from: http://www.worldgastroenterology.org/guidelines/global-guidelines/acute-diarrhea/acute-diarrhea-english.
31. Varatharajalu R, Kakuturu R. Strongyloides stercoralis: current perspectives. Rep Parasitol 2016;(5):23–33.
32. Medscape. Ivermectin (Rx). Brand and other names: Stromectol. Dosage forms & strengths. [Internet]. Medscape; [accessed 2018 Mar 13]. Available from: https://reference.medscape.com/drug/stromectol-ivermectin-342657.
33. Horton J. Albendazole: a review of anthelmintic efficacy and safety in humans. Parasitology 2000;121 Suppl:S113-132.
34. Venkatesan P. Albendazole. J Antimicrob Chemother 1998 Feb;41(2):145–7.
35. Henriquez-Camacho C, Gotuzzo E, Echevarria J, White AC, Terashima A, Samalvides F, et al. Ivermectin versus albendazole or thiabendazole for Strongyloides stercoralis infection. Cochrane Database Syst Rev 2016 Jan 18;(1):CD007745.
36. Chiodini PL, Reid AJ, Wiselka MJ, Firmin R, Foweraker J. Parenteral ivermectin in Strongyloides hyperinfection. Lancet 2000 Jan 1;355(9197):43–4.
37. Boulware DR. Strongyloides infection. BMJ Best Pract [Internet]. Available from: http://bestpractice.bmj.com/best-practice/monograph/907/treatment/step-by-step.html.
38. Albonico M, Becker SL, Odermatt P, Angheben A, Anselmi M, Amor A, et al. StrongNet: An international network to improve diagnostics and access to treatment for strongyloidiasis control. PLoS Negl Trop Dis 2016 Sep;10(9):e0004898.
39. Luvira V, Watthanakulpanich D, Pittisuttithum P. Management of Strongyloides stercoralis: a puzzling parasite. Int Health 2014 Dec;6(4):273–81.
40. Maskery B, Coleman MS, Weinberg M, Zhou W, Rotz L, Klosovsky A, et al. Economic analysis of the impact of overseas and domestic treatment and screening options for intestinal helminth infection among US-bound refugees from Asia. PLoS Negl Trop Dis 2016 Aug;10(8):e0004910.
41. Nelson GS. [Review of D.I. Grove, A history of human helminthology (1990).]. J Helminthol 1991;65(2):120.
42. Ross KE, O’Donahoo FJ, Garrard TA, Taylor MJ. Simple solutions to Strongyloides stercoralis infection. BMJ Clin Res Ed 2013 Oct 22;347:f6294.
43. European Medicines Agency Committee for Medicinal Products for Veterinary Use (CVMP). Reflection paper on anthelmintic resistance [Internet]. London: European Medicines Agency; 2017 [accessed 2018 Mar 13]. Available from: http://www.ema.europa.eu/ema/index.jsp?curl=pages/regulation/general/general_content_001563.jsp&mid=WC0b01ac058002ddc2.
44. Wood IB, Amaral NK, Bairden K, Duncan JL, Kassai T, Malone JB, et al. World Association for the Advancement of Veterinary Parasitology (W.A.A.V.P.) second edition of guidelines for evaluating the efficacy of anthelmintics in ruminants (bovine, ovine, caprine). Vet Parasitol 1995 Jun;58(3):181–213.
45. Coles GC, Bauer C, Borgsteede FH, Geerts S, Klei TR, Taylor MA, et al. World Association for the Advancement of Veterinary Parasitology (W.A.A.V.P.) methods for the detection of anthelmintic resistance in nematodes of veterinary importance. Vet Parasitol 1992 Sep;44(1–2):35–44.
46. Forrer A, Khieu V, Schindler C, Schär F, Marti H, Char MC, et al. Ivermectin treatment and sanitation effectively reduce Strongyloides stercoralis infection risk in rural communities in Cambodia. PLoS Negl Trop Dis 2016 Aug;10(8):e0004909.
47. Khieu V, Schär F, Forrer A, Hattendorf J, Marti H, Duong S, et al. High prevalence and spatial distribution of Strongyloides stercoralis in rural Cambodia. PLoS Negl Trop Dis 2014 Jun;8(6):e2854.
48. Croker C, She R. Increase in reports of Strongyloides infection — Los Angeles County, 2013–2014. MMWR Morb Mortal Wkly Rep 2015 Aug 28;64(33):922–3.
49. Keiser PB, Nutman TB. Strongyloides stercoralis in the immunocompromised population. Clin Microbiol Rev 2004 Jan;17(1):208–17.
50. World Health Organization. World Health Assembly adopts resolution on neglected tropical diseases [Internet]. Geneva: World Health Organization; 2013 [accessed 2018 Mar 13]. Available from: http://www.who.int/neglected_diseases/WHA_66_seventh_day_resolution_adopted/en/.