1. Introducción
El estreñimiento (o constipación) es un problema crónico en muchos pacientes del mundo. En algunos grupos de pacientes, tales como los añosos, el estreñimiento constituye un problema sanitario importante; sin embargo, en la mayoría de los casos el estreñimiento crónico es un motivo de consulta que provoca molestia pero que no amenaza la vida ni debilita al individuo. Habitualmente puede ser manejada a nivel de atención primaria con control costo-efectivo de los síntomas.
La terminología vinculada al estreñimiento es problemática. Hay dos fisiopatologías que en principio difieren pero que se superponen: los trastornos del tránsito y los trastornos de la evacuación. Los primeros pueden surgir secundariamente a los segundos, y los segundos en ocasiones pueden presentarse después de los primeros.
Esta guía se refiere a los pacientes adultos y no analiza específicamente ni a niños ni a grupos especiales de pacientes (como aquellos que presentan lesión raquídea).
1.1 Cascadas—un abordaje sensible a los recursos
En las regiones y países donde se disponga de toda la gama de exámenes diagnósticos y opciones de tratamiento médico para el manejo de todos los tipos y subtipos de estreñimiento es factible utilizar un enfoque de patrón oro.
Cascada: conjunto jerárquico de opciones diagnósticas, terapéuticas y de manejo para lidiar con el riesgo y la enfermedad, catalogados según los recursos disponibles.
2. Definición y patogenia
La palabra “estreñimiento” tiene varios significados y la manera como se la utiliza puede diferir no solo entre los pacientes sino también entre las diferentes culturas y religiones. En un estudio poblacional sueco se encontró que el concepto más común de estreñimiento era la necesidad de ingerir laxantes (57% de quienes respondieron). En el mismo estudio, las mujeres (41%) tuvieron el doble de probabilidades que los hombres (21%) de considerar a los movimientos intestinales infrecuentes como representativos de estreñimiento, mientras que igual proporción de hombres y mujeres entendían por estreñimiento a las deposiciones duras (43%), el esfuerzo al defecar (24%), y el dolor al defecar (23%). Dependiendo de diversos factores—la definición diagnóstica, factores demográficos, y el muestreo de los grupos- las encuestas sobre estreñimiento muestran una prevalencia que va de 1% a más de 20% en las poblaciones occidentales. En estudios de poblaciones añosas, hasta 20% de los individuos que habitan en comunidad y 50% de las personas añosas institucionalizadas relataron síntomas.
Habitualmente se define el estreñimiento funcional como un trastorno caracterizado por una dificultad persistente para defecar o una sensación de que la defecación es aparentemente incompleta y/o movimientos intestinales infrecuentes (cada 3–4 días o con menor frecuencia) en ausencia de síntomas de alarma o causas secundarias. Las diferencias en la definición médica y las variaciones entre los síntomas relatados dificultan la obtención de datos epidemiológicos confiables.
2.1 Patogenia y factores de riesgo
El estreñimiento funcional puede tener diferentes causas, yendo desde cambios en la dieta, actividad física o estilo de vida, hasta disfunciones motoras primarias producidas por miopatía o neuropatía colónica. El estreñimiento también puede ser secundaria a un trastorno de evacuación. El trastorno de evacuación puede además asociarse a una contracción paradójica o espasmo involuntario del esfínter anal, lo que puede responder a trastorno adquirido del comportamiento defecatorio en dos tercios de los pacientes.
Tabla 1 Fisiopatología del estreñimiento funcional
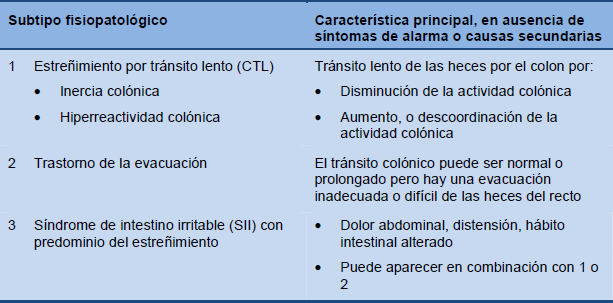
Si bien el ejercicio físico y la dieta rica en fibras pueden tener un efecto protector, los siguientes factores aumentan el riesgo de estreñimiento (la asociación puede no ser causal):
- Envejecimiento (pero el estreñimiento no es una consecuencia fisiológica del envejecimiento normal)
- Depresión
- Inactividad
- Baja ingesta calórica
- Bajos ingresos y bajo nivel educativo
- Cantidad de medicación que reciba (independientemente de los perfiles de efectos adversos)
- Abuso físico y sexual
- Sexo femenino— las mujeres relatan una mayor incidencia de estreñimiento que los hombres
2.2 Condiciones y medicamentos asociados
Tabla 2 Posibles causas y condiciones asociadas al estreñimiento

Tabla 3 Medicamentos que se asocian con estreñimiento

3. Diagnóstico
El estreñimiento es una afección común, y si bien los individuos que consultan constituyen sólo una minoría, en Estados Unidos sólo esta afección es responsable de varios millones de consultas médicas por año, mientras que en el Reino Unido en 2006 los médicos generales emitieron más de 13 millones de recetas para laxantes. La ayuda de un especialista gastroenterólogo debería concentrarse en aplicar los recursos sanitarios de manera eficiente, identificando a aquellos pacientes que tienen probabilidades de beneficiarse de evaluaciones diagnósticas y tratamientos especializados.
3.1 Criterios diagnósticos para el estreñimiento funcional
Un panel de expertos internacionales elaboró criterios uniformes para el diagnóstico de estreñimiento—los criterios de Roma III.
Tabla 4 Criterios de Roma III para estreñimiento funcional

3.2 Evaluación de los pacientes
La historia médica y el examen físico en los pacientes con estreñimiento deberían enfocarse hacia la identificación de las posibles condiciones causales y síntomas de alarma.
- Consistencia de las deposiciones. Esto es considerado como un mejor indicador del tránsito colónico que las frecuencias de las deposiciones (Figura. 1).
Figura. 1 La Escala de Forma de las Deposiciones de Bristol es una medida diseñada para ayudar a los pacientes a describir la consistencia de las materias fecales (reproducido con permiso de Lewis SJ y Heaton KW, et al, Scandinavian Journal of Gastroenterology 1997;32:920–4). ©1997 Informa Healthcare

- Descripción de los síntomas de estreñimiento del paciente; diario de síntomas:
- Distensión abdominal, dolor, malestar
- Naturaleza de las deposiciones
- Movimientos intestinales
- Esfuerzo defecatorio prolongado/excesivo
- Defecación insatisfactoria
- Uso de laxantes, pasado y actual; frecuencia y dosificación
- Condiciones actuales, historia médica, cirugía reciente, enfermedad psiquiátrica
- Estilo de vida del paciente, fibra en la dieta e ingesta de líquidos
- Uso de supositorios o enemas, otras medicaciones (de receta o de venta libre) Examen físico:
- Tumoración gastrointestinal
- Inspección anorectal: Impactación fecal
- Estenosis, prolapso rectal, rectocele
- Actividad paradójica o no relajante del músculo puborrectal
- Tumoración rectal
- De estar indicado: exámenes de sangre—perfil bioquímico, hemograma completo, calcio, glucosa, y función tiroidea
3.3 Síntomas de alarma
Tabla 5 Síntomas de alarma en el estreñimiento

3.4 Indicaciones para las pruebas de tamizaje
Sólo está indicado realizar estudios de laboratorio, imagenología o endoscopía y pruebas funcionales en los pacientes que presenten estreñimiento crónico severo o síntomas de alarma.
Tabla 6 Pruebas fisiológicas para estreñimiento crónico (reproducido con permiso de Rao
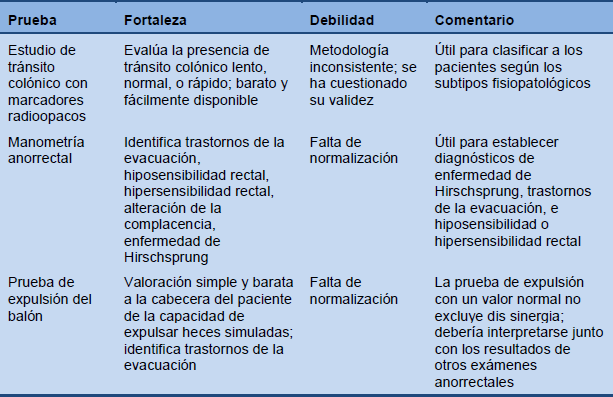
3.5 Medición del tránsito
El estudio de retención de marcador de 5 días es un método simple para medir el tránsito colónico. Se ingieren marcadores en una ocasión y 120 horas después se mide lo que queda de los marcadores en una radiografía simple de abdomen. Si se constata la persistencia de más del 20% de los marcadores en el colon, significa que el tránsito esta retardado. La acumulación distal de los marcadores puede indicar un trastorno de la evacuación, y en los casos típicos de estreñimiento por tránsito lento casi todos los marcadores se mantienen y se observan tanto en el colon derecho como en el izquierdo.
Varias compañías producen marcadores, pero estos también se pueden hacer de un tubo radiopaco que no implique riesgos para el paciente, cortándolo en pequeños trozos de 2–3 mm de longitud. Se puede colocar un número adecuado de marcadores (20–24) en cápsulas de gelatina para facilitar su ingestión.
3.6 Evaluación clínica
La clasificación del estreñimiento de los pacientes debería ser posible en base a la historia médica y un correcto examen y valoración de laboratorio.
Tabla 7 Categorías de estreñimiento en base a la evaluación clínica
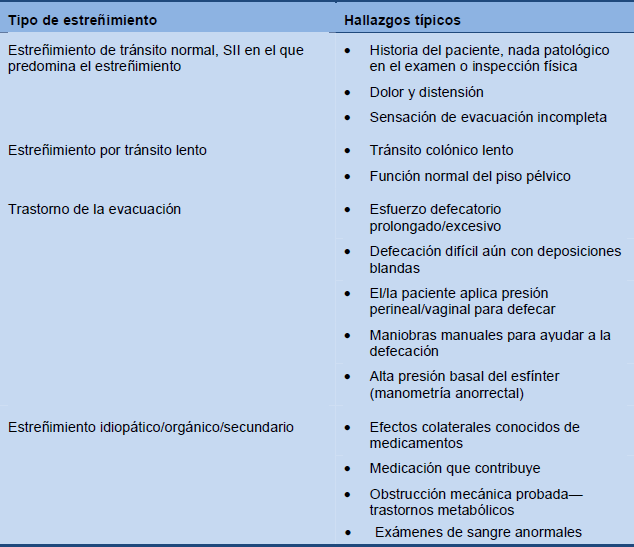
3.7 Opciones en cascada para investigar el estreñimiento severo y refractario al tratamiento
Nivel 1—Recursos limitados
- Anamnesis y examen físico general
- Examen ano rectal. Diario con registro de los movimientos intestinales durante 1 semana
- Estudio del tránsito usando marcadores radiopacos d) Prueba de expulsión del balón
Nivel 2—Recursos intermedios
- Anamnesis y examen físico general
- Examen ano rectal. Diario con registro de los movimientos intestinales durante 1 semana
- Estudio del tránsito usando marcadores radiopacos d) Prueba de expulsión del balón o defecografía
Nivel 3—Recursos amplios
- Anamnesis y examen físico general
- Examen ano rectal. Diario con registro de los movimientos intestinales durante 1 semana
- Estudio del tránsito usando marcadores radiopacos
- Defecografía o proctografía -resonancia magnética (RMN)
- Manometría anorrectal
- Electromiografía (EMG) del esfínter
4. Tratamiento
4.1 Esquema para el manejo general del estreñimiento
Tabla 8 Manejo general del estreñimiento
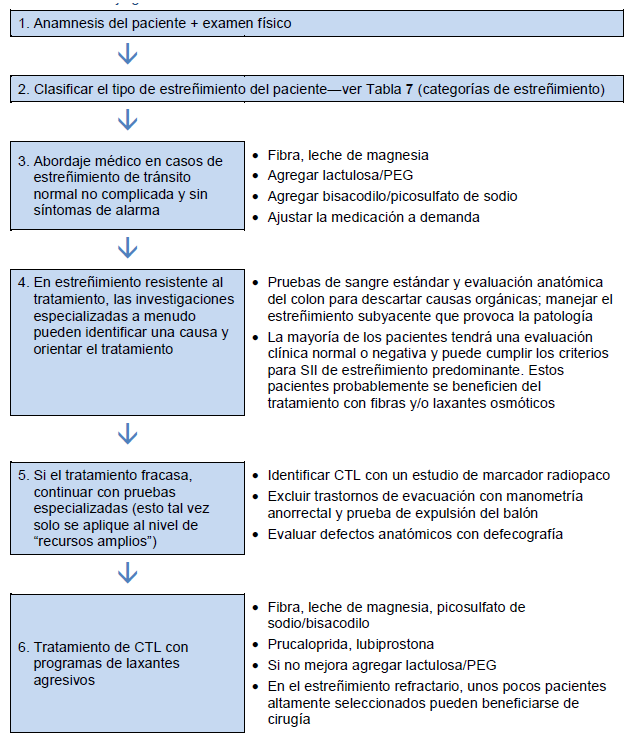
SII: síndrome de intestino irritable; PEG, polietilenglicol; CTL, estreñimiento por tránsito lento.
4.2 Abordaje sintomático
Una vez que se haya estudiado y descartado un estreñimiento orgánico y secundario, la mayoría de los casos pueden ser manejados adecuadamente con un abordaje sintomático.
- El abordaje graduado del tratamiento se basa en recomendar cambios en el estilo de vida y la dieta, interrumpiendo o reduciendo medicaciones que producen estreñimiento y administrando suplementos con fibra u otros agentes formadores de volumen. Generalmente se recomienda un aumento gradual de la fibra (ya sea como suplementos estandarizados o incorporada en la dieta) y un aumento de la ingesta de líquidos.
- El segundo paso en el abordaje graduado es agregar laxantes osmóticos. La mejor evidencia es utilizar polietilenglicol, pero también existe buena evidencia para la lactulosa. Las nuevas drogas lubiprostona y linaclotida actúan estimulando la secreción ileal y aumentando así el agua fecal. Prucaloprida también está aprobada en muchos países y en Europa.
- El tercer paso incluye laxantes estimulantes, enemas, y fármacos proquinéticos. Se pueden administrar laxantes estimulantes por vía oral o rectal para estimular la actividad motriz colorrectal. Los fármacos proquinéticos también buscan aumentar la actividad de propulsión del colon, pero a diferencia de los laxantes estimulantes, que deben tomarse ocasionalmente, estos están diseñados para administrarse a diario.
4.3 Dieta y sumplementos
- La modificación de la dieta puede consistir en agregar fibras para lograr una dieta rica en fibras (25 g de fibras) y suplementos de líquidos (hasta 1.5–2.0 L/día); puede mejorar la frecuencia de las deposiciones y disminuir la necesidad de laxantes.
- No existen evidencias que las medidas vinculadas a la dieta y al estilo de vida tengan ningún efecto sobra el estreñimiento en los individuos de edad, mientras que los suplementos de fibra y los laxantes osmóticos simples habitualmente constituyen un manejo adecuado para el estreñimiento en estos pacientes.
- En los pacientes con dilatación colónica debe evitarse la suplementación con fibras.
- Los suplementos con psilio y lactulosa pueden ser útiles para el tratamiento del estreñimiento crónico.
4.4 Medicación
- Los trastornos de evacuación responden mal a los programas de laxantes orales estándar. Si un trastorno de la evacuación interviene de manera considerable en el estreñimiento, debe considerarse biofeedback y entrenamiento de la musculatura pélvica. Entre los factores críticos para el éxito se encuentran el nivel de motivación del paciente, la frecuencia del programa de entrenamiento y la participación de un psicólogo conductista y un nutricionista.
- Si falla el abordaje de la dieta, se puede utilizar polietilenglicol (17 g de laxante PEG durante 14 días) o lubiprostona (24 mg dos veces por día) para promover la función intestinal en los pacientes con estreñimiento crónico.
- Los agentes proquinéticos (por ejemplo, prucaloprida un antagonista de los receptores 5-HT4) pueden utilizarse en el SII con predominancia del estreñimiento.
- Los agentes laxantes sencillos, como leche de magnesia, senna, bisacodilo, y los agentes que ablandan las heces son una elección razonable para tratar el estreñimiento.
4.5 Cirugía
- Si el tratamiento fracasa una y otra vez en el estreñimiento por tránsito lento, un grupo seleccionado de pacientes bien evaluados e informados pueden beneficiarse de una colectomía total con anastomosis ileorrectal. La indicación excepcional de colectomía debe establecerse en un centro terciario especializado y con experiencia. Pueden verse resultados decepcionantes, en los que el paciente puede quedar con incontinencia fecal y estreñimiento recurrente después de la cirugía, especialmente con trastornos de la evacuación.
- Son muy pocos los pacientes que se benefician de una colostomía (reversible) para tratar el estreñimiento.
4.6 Resumen basado en la evidencia
Tabla 9 Resumen: Base de evidencia para el tratamiento del estreñimiento (adaptado de Rao SS, Gastrointest Endosc Clin N Am 2009;19:117–39)
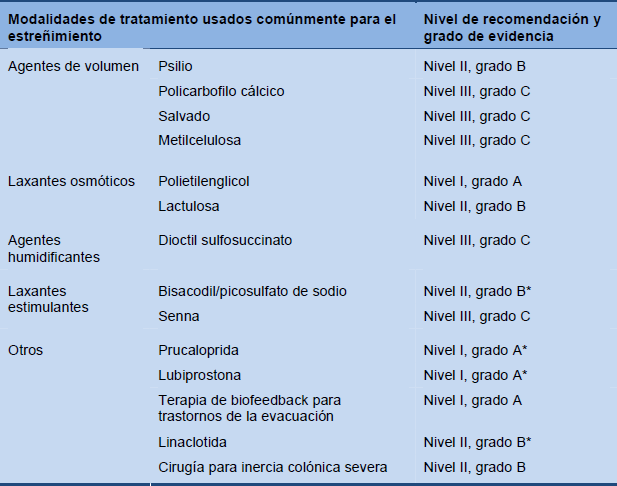
* Adaptado por el actual equipo de revisión de las guías de estreñimiento.
4.7 Opciones en cascada para el tratamiento del estreñimiento crónico
La siguiente cascada está destinada a pacientes con estreñimiento crónico sin síntomas de alarma y con poca o ninguna sospecha de un trastorno de la evacuación. Los principales síntomas serían deposiciones duras y/o movimientos intestinales infrecuentes.
Nivel 1— Recursos limitados
- Asesoramiento nutricional (fibra y líquidos)
- Suplementación con fibras
- Leche de magnesia (hidróxido de magnesio en una solución acuosa)
- Laxantes estimulantes (bisacodilo mejor que senna) de uso transitorio
Nivel 2— Recursos intermedios
- Asesoramiento nutricional (fibra y líquidos)
- Suplementación con fibras, psilio
- Leche de magnesia, lactulosa, macrogol d) Laxantes estimulantes de uso transitorio
Nivel 3— Recursos amplios
- Asesoramiento nutricional (fibra y líquidos)
- Psilio o lactulosa
- Macrogol o lubiprostona
- Proquinéticos (prucaloprida)
- Laxantes estimulantes (bisacodilo o picosulfato de sodio)
4.8 Opciones en cascada para el tratamiento de los trastornos de la evacuación
Esta cascada se aplica a pacientes con estreñimiento crónico sin síntomas de alarma pero con sospecha de un trastorno de la evacuación. Los principales síntomas serían esfuerzo defecatorio prolongado, sensación de evacuación incompleta, deposiciones finas, sensación de bloqueo (estar tapado), o falla del tratamiento por estreñimiento con materias duras.
Nivel 1— Recursos limitados
- Asesoramiento nutricional y comportamental (fibra, líquidos, entrenamiento intestinal con horarios)
- Terapia para el estreñimiento crónico
Nivel 2— Recursos intermedios
- Asesoramiento nutricional y comportamental (fibra, líquidos, entrenamiento intestinal con horarios)
- Terapia para el estreñimiento crónico
- Terapia de biofeedback
Nivel 3— Recursos amplios
- Asesoramiento nutricional y comportamental (fibra, líquidos, entrenamiento intestinal con horarios)
- Terapia para el estreñimiento crónico
- Terapia de biofeedback
- Evaluación quirúrgica














